Clear Sky Science · sv
Kombinera federated learning och en vandrande modell förbättrar prestanda och öppnar möjligheter för digital hälsojämlikhet
Varför det spelar roll att dela medicinska insikter utan att dela data
Modern medicin förlitar sig i allt högre grad på artificiell intelligens för att upptäcka mönster i avbildningar och journaldata. Men patientdata är känsliga och får ofta inte lämna det sjukhus där de samlades in. Det skapar en konflikt: hur kan sjukhus världen över samarbeta för att träna kraftfulla AI-verktyg utan att skicka rå patientdata över gränser eller till stora centrala servrar? Denna studie introducerar ett nytt sätt att göra just detta, med målet inte bara att förbättra noggrannheten utan också rättvisan mellan välutrustade sjukhus och mindre, resurssvaga kliniker.
Två sätt att lära en AI utan att flytta data
Idag finns två huvudstrategier som låter sjukhus träna AI tillsammans samtidigt som data stannar kvar lokalt. I federated learning tränar varje sjukhus sin egen lokala kopia av en modell parallellt; dessa lokala modeller kombineras sedan till en gemensam "global" modell på en central server. I en vandrande modell finns bara en modell som förflyttas från sjukhus till sjukhus och tränas på varje plats i tur och ordning. Båda metoderna skyddar integriteten, men båda har nackdelar. Federated learning kan ha svårt när vissa sjukhus har mycket lite data eller inte ser alla patienttyper; att kombinera svaga eller obalanserade lokala modeller kan leda till en dålig global modell som i huvudsak återspeglar stora, välbärgade centra. Den vandrande modellen är mer robust mot sådana obalanser men kan vara långsammare och svårare att hantera.
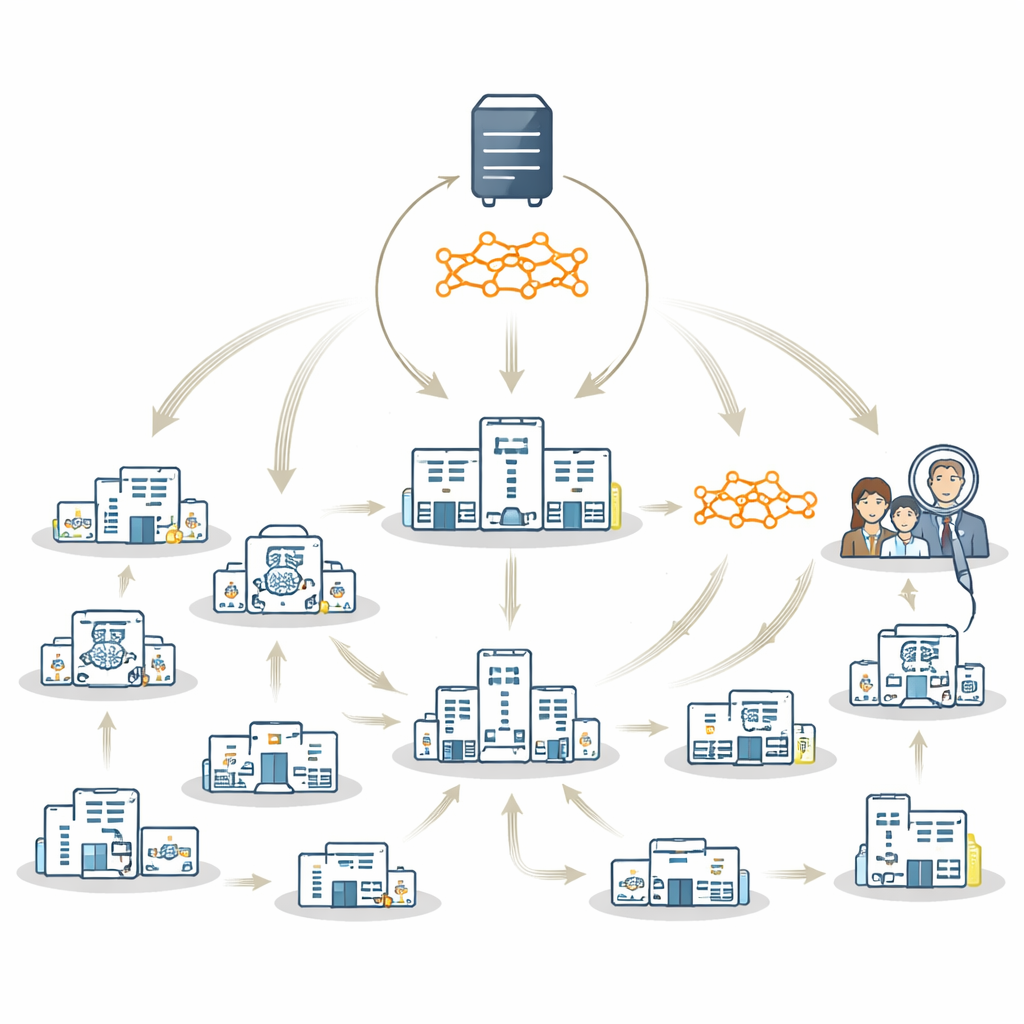
En hybridstrategi som använder det bästa från båda metoderna
Författarna föreslår FedTM, ett hybridträningsschema som blandar styrkorna hos federated learning och den vandrande modellen. Träningen sker i två faser. Först kommer en "uppvärmnings"-fas där endast de största sjukhusen, med mer fullständiga och balanserade dataset, tränar modellen parallellt med standardmetoder för federated learning. Detta skapar en stark startmodell. Därefter följer en "förfinings"-fas där denna uppvärmda modell besöker varje plats i följd, inklusive mycket små kliniker som kanske bara har några hjärnavbildningar eller till och med bara en patient. I denna andra fas uppdateras modellen successivt när den reser, och införlivar kunskap från varje plats utan att deras data någonsin behöver lämna lokal kontroll.
Test av metoden på hjärnavbildningar vid Parkinsons sjukdom
För att pröva FedTM använde forskarna 1 817 hjärn‑MRI-bilder från 83 bildgivande centra världen över för att träna ett AI-system att skilja personer med Parkinsons sjukdom från friska individer. Det här är en särskilt utmanande situation: mer än hälften av platserna bidrog med färre än tio bilder, endast omkring en tredjedel hade både patient- och kontrolldata, och skanningsprotokollen varierade stort. Under dessa verklighetsnära förhållanden klarade ren federated learning inte uppgiften särskilt väl, medan en ren vandrande modell presterade bättre men fortfarande lämnade rum för förbättring. FedTM, särskilt när uppvärmningen involverade de sju största och mest balanserade platserna, överträffade tydligt båda: arean under ROC‑kurvan, ett standardmått på klassificeringskvalitet, steg från 77 % med endast den vandrande modellen till cirka 82 % med FedTM, med liknande förbättringar i andra kliniskt viktiga mått som känslighet, specificitet och F1‑poäng.
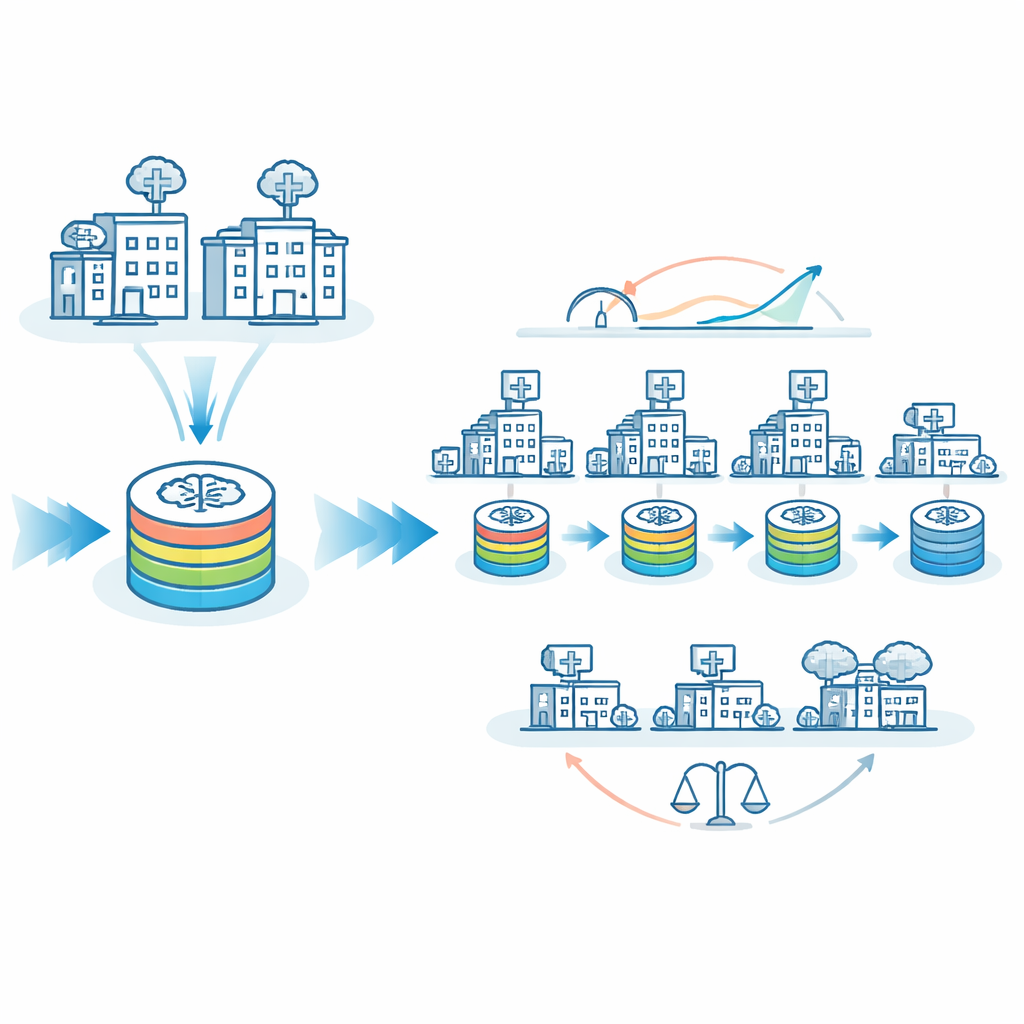
Göra AI rättvisare mellan stora och små sjukhus
En central fråga inom medicinsk AI är jämlikhet: fungerar en modell lika bra för patienter på små, landsbygds- eller resurssvaga sjukhus som för dem på stora akademiska centra? Teamet undersökte hur ofta AI:n gjorde felaktiga prognoser på "större" respektive "mindre" platser. Med endast den vandrande modellen skilde sig felklassificeringsfrekvenserna med cirka 8 procentenheter mellan dessa grupper. Med FedTM, rätt inställd, blev felklassificeringsfrekvenserna för större och mindre platser nästan identiska, runt 26 %. Med andra ord blev modellen inte bara mer exakt totalt sett, utan också mer jämlik. FedTM flyttade dessutom det mesta av den tunga beräkningen till uppvärmningsfasen vid bättre resurserade platser, vilket halverade antalet träningscykler som små platser behövde köra, samtidigt som den totala träningstiden förblev liknande.
Vad detta betyder för global digital hälsa
FedTM erbjuder en praktisk väg mot AI‑verktyg som respekterar integritet, förbättrar prestanda och fördelar nyttan mer rättvist globalt. Genom att låta även platser med mycket lite data påverka slutmodellen kan detta ramverk bidra till att människor i resurssvaga eller avlägsna miljöer inte hamnar på efterkälken när nya diagnostiska verktyg utvecklas. Trots att studien fokuserade på en typ av hjärnavbildning och en sjukdom kan angreppssättet i princip anpassas till många andra medicinska problem. I takt med att vårdsystem i större utsträckning tar till sig mobila enheter och wearables, och då regelverk betonar dataskydd och suveränitet, kan hybrida strategier som FedTM bli nyckeln till att bygga trovärdig, inkluderande och ansvarsfull medicinsk AI.
Citering: Souza, R., Stanley, E.A.M., Ohara, E.Y. et al. Combining federated learning and travelling model boosts performance and opens opportunities for digital health equity. npj Digit. Med. 9, 294 (2026). https://doi.org/10.1038/s41746-026-02483-y
Nyckelord: federated learning, travelling model, Parkinsons sjukdom, medicinsk bild‑AI, hälsojämlikhet