Clear Sky Science · sv
Fysikbegränsad grafneuralt nätverk för realtidsprognoser av hemodynamik vid intracerebrala aneurysm
Varför detta spelar roll för hjärnhälsan
Utbuktande svaga punkter i hjärnans artärer, så kallade intracerebrala aneurysm, kan spricka utan förvarning och orsaka livshotande blödningar. Läkare vet att hur blodet flyter över dessa sköra väggar påverkar om de förblir stabila eller brister, men dagens verktyg för att simulera detta flöde är så långsamma och specialiserade att de sällan används i vardaglig vård. Denna studie presenterar en snabb artificiell intelligens‑metod som kan efterlikna detaljerade blodflödessimuleringar på sekunder istället för timmar, vilket öppnar för snabbare och mer personanpassade beslut om vem som behöver behandling och hur.
Från statiska bilder till rörligt blod
I dag baseras de flesta beslut om aneurysm på vad som syns i bilder: utbuktningens storlek, form och läge, plus grundläggande riskfaktorer som ålder och högt blodtryck. Dessa ögonblicksbilder missar de osynliga krafterna i det strömmande blodet, till exempel hur hårt det sliter längs kärlväggen eller hur mycket den kraften förändras under varje hjärtslag. Traditionell datorberäknad fluiddynamik kan beräkna dessa storheter exakt, men kräver experter för uppsättning och långa körningar på kraftfulla datorer. Som en följd kan många sjukhus inte realistiskt använda dem när en läkare behöver svar inom ett mottagningsbesök eller under ett akut ingrepp.
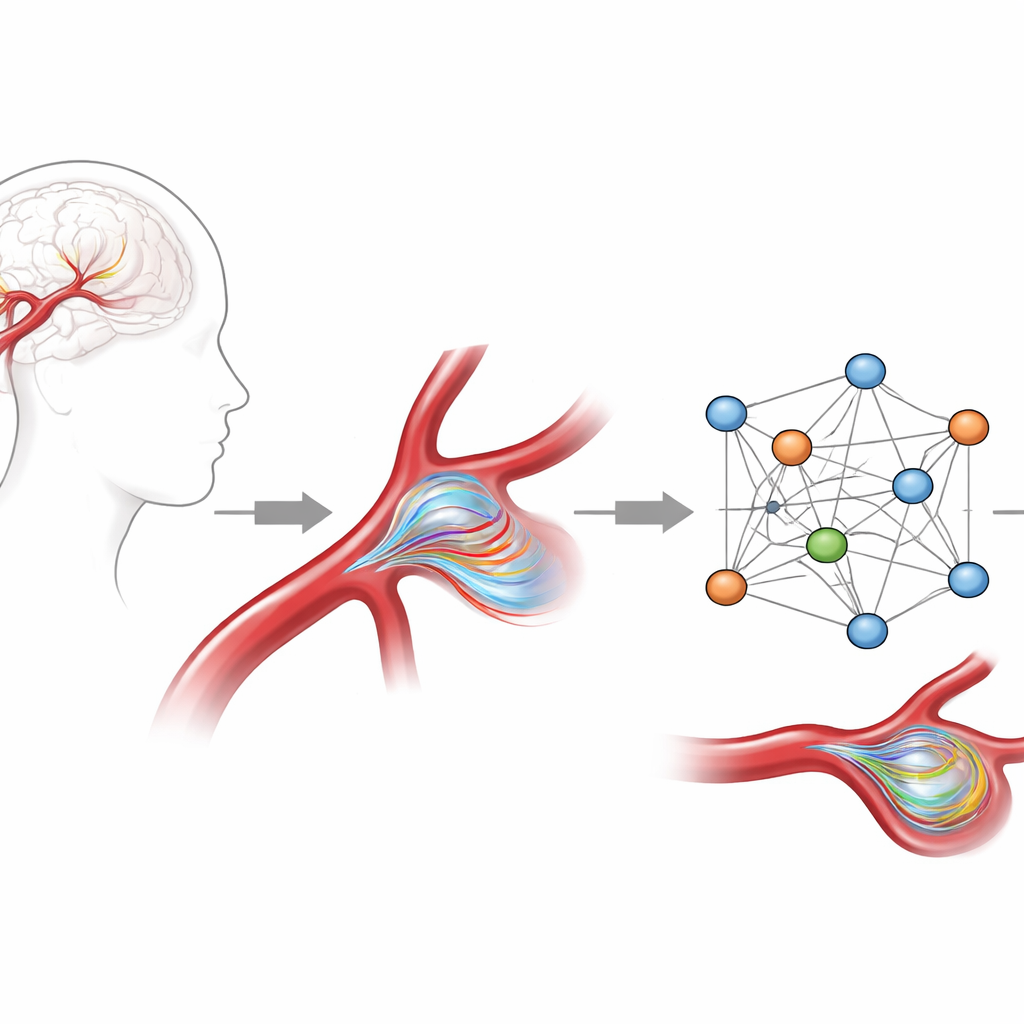
Att lära en AI att respektera fysiken
Forskarna byggde en AI‑modell baserad på grafneurala nätverk, en algoritmtyp som naturligt arbetar på förgrenade strukturer som kärlmesh snarare än på fyrkantiga bildrutor. De tränade modellen på högkvalitativa datorsimuleringar av blodflöde i 105 aneurysmmodeller hämtade från verkliga patientdata, med fokus på en vanlig position i en viktig hjärnartär. Varje fall innehöll fulla tredimensionella fält för hastighet och tryck över ett helt hjärtslag. För att ge modellen en stark känsla för den underliggande fysiken bad de den inte bara kopiera de simulerade hastigheterna: de lade till extra egenskaper som beskriver hur snabbt blodet går in i artären och hur snabbt det accelererar, och de straffade AI:n när dess prognoser bröt mot grundläggande fluidlagar som massans bevarande.
Att se in i en farlig utbuktning
Efter träning kunde AI:n ta en enskild bildruta med blodflödesinformation och snabbt rulla den fram i tiden, återskapa virvelmönster och återcirkulationszoner inne i aneurysmkapseln. Jämfört med de ursprungliga simuleringarna var dess kortsiktiga fel redan låga, men det verkliga testet var om dessa fel skulle växa när den förutsade tiotals steg framåt. Den förbättrade, fysikbegränsade versionen klarade detta test: över 50 prognossteg var dess misstag mer än sex gånger mindre än en enklare referensmodell, och den följde det förändrade flödet även under hjärtslagets mest turbulenta fas. När teamet omvandlade dessa hastighetsfält till kliniskt relevanta mått — såsom genomsnittlig väggskjuvning över aneurysmets kupol — höll sig AI:n inom cirka 10 procent av referensvärdena och reproducerade var de högsta skjuvningarna uppträdde.
Generaliserar utanför träningsmängden
En central fråga för all medicinsk AI är om den kan hantera patienter den aldrig sett tidigare. Teamet utmanade sin modell med två typer av okända situationer utan någon ytterligare träning. Först ändrade de inflödesvågformerna för att matcha mönster mätta i andra hjärnartärer. AI:n följde fortfarande den nya tajmingen och styrkan i varje puls, höll felen måttliga och fångade det omskapade flödet inne i utbuktningen. För det andra testade de modellen på fyra fullt patient‑specifika aneurysmgeometrier med olika storlekar, halsbredder och kärlbanor. Även om de exakta hastighetsnivåerna ibland var felaktiga återgav modellen de huvudsakliga flödesstrukturerna och påverkansområdena, vilket tyder på att den lärt sig det underliggande beteendet snarare än bara memorerat träningsformerna.
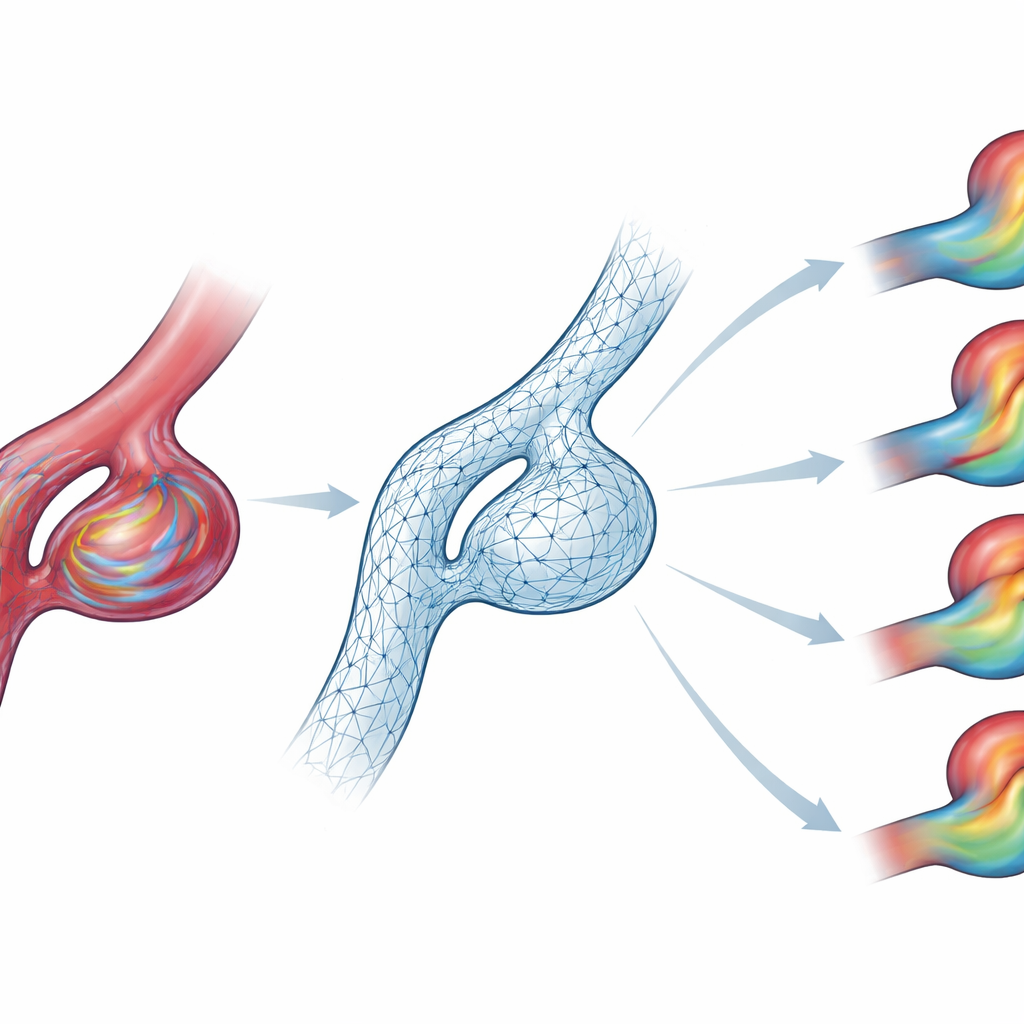
Snabbare svar vid sängkanten
Eftersom denna AI kör ungefär sextio gånger snabbare än de traditionella simuleringar den lärde sig från blir den mer effektiv än standardmetoder efter bara några dussin fall och skulle så småningom kunna leverera fulla fält‑prognoser av blodflödet på under en minut. Författarna poängterar att deras verktyg inte är en fristående rupturprognos; i stället är det en snabb motor för att generera fysikaliskt konsistenta flödeskartor och väggskjuvningar som andra riskmodeller kan använda. De publicerar också sin 105‑fallsmängd som en öppen benchmark så att andra grupper kan bygga och jämföra förbättrade modeller. Med vidare träning på mer realistiska kärlformer och patient‑specifika inflödesdata kan detta tillvägagångssätt hjälpa till att flytta sofistikerad blodflödesanalys från superdatorlabbet till vardaglig vård för människor som lever med hjärnaneurysm.
Citering: Lannelongue, V., Garnier, P., Jeken-Rico, P. et al. Physics constrained graph neural network for real time prediction of intracranial aneurysm hemodynamics. npj Digit. Med. 9, 212 (2026). https://doi.org/10.1038/s41746-026-02404-z
Nyckelord: hjärnaneurysm, blodflöde, grafneural nätverk, beräkningsmodellering, digital medicin