Clear Sky Science · sv
Avkodning av ERS–CAF immunregleringsaxeln via multimodal AI och dess prognostiska och terapeutiska prediktiva värde över cancerformer
Att betrakta tumörer utan skalpell
Cancerläkare inser i allt högre grad att vad som omger en tumör kan vara lika viktigt som tumören själv. Men att upprepade gånger provta detta dolda grannskap med biopsier är invasivt och ofta opraktiskt. Denna studie visar hur artificiell intelligens (AI) kan tolka rutinmässiga medicinska skanningar och mikroskopbilder för att härleda svårmätta immuna och ärrliknande processer inne i tumörer, vilket potentiellt förvandlar vardaglig bilddiagnostik till en sorts ”digital biopsi” som fungerar över olika cancerformer.
De dolda stödjecellerna som formar cancer
Många solida tumörer är inbäddade i ett hårt, fibröst skal som byggs upp av specialiserade stödjeceller kallade fibroblaster. När dessa celler utsätts för stress i cellens proteinfabrik (endoplasmatiska retiklet) antar de ett aggressivt, cancerunderstöddande tillstånd. I chordom, en sällsynt bencancer, bygger dessa stressade fibroblaster upp ett tätt matrix och bidrar till att hålla immunceller ute, vilket gör behandlingar mindre effektiva. Liknande fibrösa, immunsnåla miljöer syns i andra cancerformer som pankreas- och kolorektala tumörer, vilket tyder på att denna biologi inte är unik för en enda sjukdom. Utmaningen är att nuvarande metoder för att mäta dessa stressade fibroblaster och deras immunsperrande beteende förlitar sig på vävnadsprover och komplexa molekylära tester, som är svåra att upprepa och kan missa viktiga regioner av tumören.
Att lära AI se osynlig biologi
Forskarna undrade om standard-MRI före operation och rutinmässiga H&E-patologiskivor redan innehåller visuella ledtrådar om denna stressade fibroblast-immunsbarriär. De skapade tre numeriska ”referenspoäng” från tumör-RNA-sekvensering: en som fångar hur aktiv stressprogrammet i fibroblaster är, en som summerar hur starkt dessa celler verkar signalera till immunceller, och en som beskriver hur mångsidiga de omgivande immun- och stödjecellpopulationerna är. Istället för att förutsäga tusentals gener tränades deras AI att förutsäga endast dessa tre biologiskt meningsfulla poäng från bilder. För att göra detta kombinerade teamet två grenar: en som analyserar MRI-textur och formfunktioner, och en annan som skannar tusentals små regioner i den digitala snitten och använder en språkledd uppmärksamhetsmekanism för att fokusera på områden som matchar experters beskrivningar av fibrös, immunsnål vävnad.
Att blanda skanningar och snitt för starkare signaler
I 126 chordompatienter med matchande MRI, patologiska snitt, RNA-data och uppföljning slog den sammansatta AI-modellen modeller som använde endast MRI eller endast snitt. Dess förutsägelser av de tre molekylära poängen stämde väl överens med RNA-baserade mätningar och förblev välkalibrerade över olika sjukhus och scanners. När patologer oberoende markerade fibrösa och immunsiplerade regioner tenderade AI:ns ”hotspots” att lyser upp i samma områden, vilket antyder att den fångade verklig biologi snarare än enbart tumörstorlek. Modellen fångade också prognos: högre predikterade stress‑fibroblast‑ och signaleringspoäng kopplades till sämre överlevnad, medan större predikterad mångfald i mikro‑miljön erbjöd ett visst skydd. Att lägga till dessa AI‑härledda poäng till rutinmässiga kliniska faktorer förbättrade förmågan att över tid skilja mellan hög‑ och lågriskpatienter.
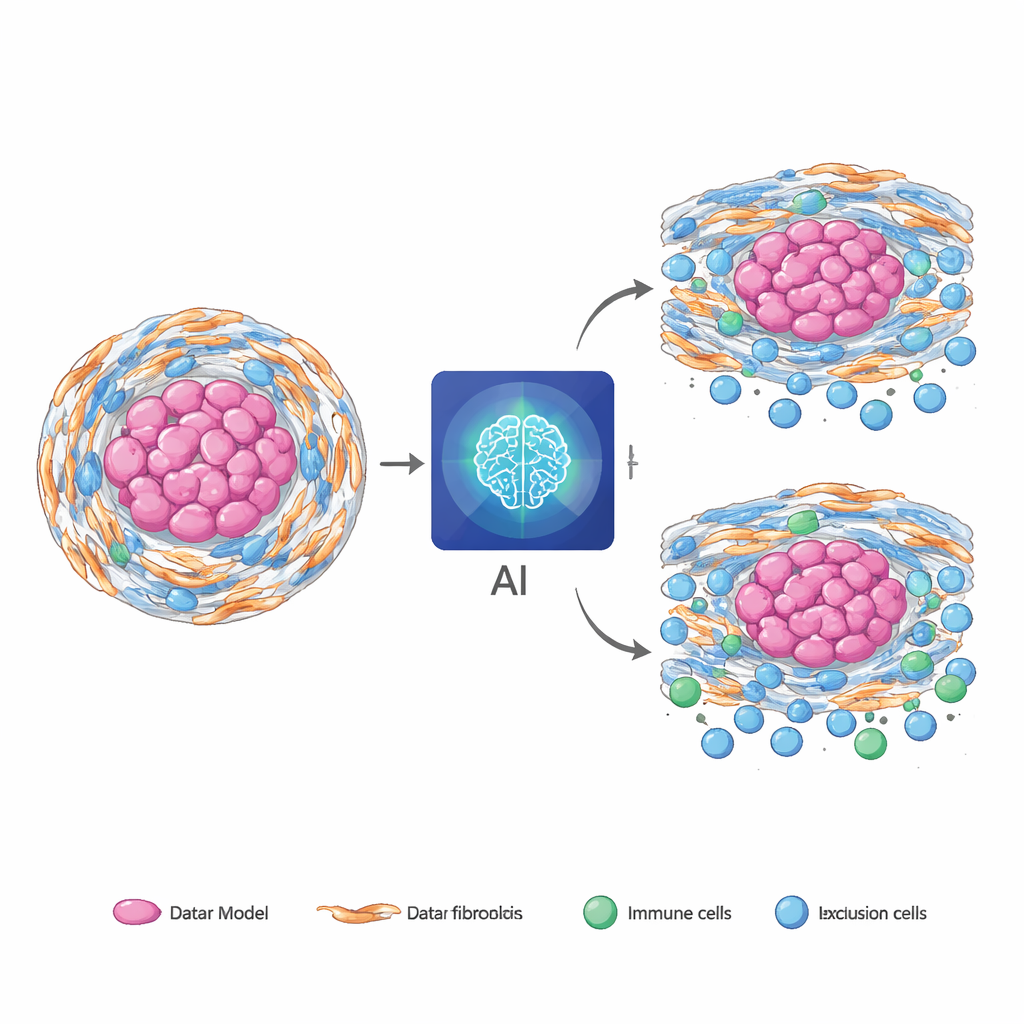
Från sällsynta tumörer till vanliga cancerformer
Ett viktigt test var om en modell som tränats helt i chordom kunde användas ”som den är” i andra, vanligare cancerformer. Tillämpad utan omskolning på pankreas-, magsäcks- och kolorektala tumörer från stora offentliga dataset visade modellens snitt‑endast-version fortfarande meningsfull överensstämmelse mellan dess bildbaserade förutsägelser och nyberäknade RNA‑baserade poäng. I vissa av dessa cancersjukdomar förbättrade AI‑poängen prognosförutsägelsen utöver standard klinisk information och hjälpte till att skilja vilka patienter som var mer benägna att dra nytta av kemoterapi. För att göra metoden lättare att distribuera där digital patologi är begränsad destillerade teamet den fulla multimodala modellen till en MRI‑endast‑version som behöll större delen av den prediktiva kraften samtidigt som den kördes snabbare och använde mindre beräkningsresurser.
Vad detta kan innebära för patienter
Sammantaget stödjer resultaten idén att rutinmässiga medicinska bilder tyst kodar information om stressade stödjeceller, immunexklusion och mikro‑miljöns mångfald — funktioner som normalt kräver dyra molekylära tester. Även om det nuvarande arbetet är retrospektivt och behöver prospektiv validering, pekar det mot en framtid där en standardundersökning och ett snitt icke-invasivt kan flagga tumörer med en fientlig, fibrös immunbarriär, vägleda vilka patienter som kan ha nytta av ytterligare tester eller skräddarsydda terapier, och göra detta över flera cancertyper utan extra påfrestning för patienterna.
Citering: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Nyckelord: tumörmikromiljö, canceravbildning, artificiell intelligens, fibroblaster, immunoterapi