Clear Sky Science · sv
Algoritmisk beslutstagning om antibiotika vid urinvägsinfektion med förskrivaranpassad prediktion av behandlingsnytta
Smartare antibiotika för vanliga infektioner
Urinvägsinfektioner (UVI) är en av de vanligaste anledningarna till att patienter får antibiotika. Att välja rätt läkemedel är dock en balansakt: läkare måste bota infektionen, undvika allvarliga biverkningar och skydda samhället mot förvärrad antibiotikaresistens. Denna studie presenterar en ny typ av beslutsalgoritm som syftar till att stödja kliniker genom att kombinera storskaliga sjukhusdata med läkarnas verkliga prioriteringar, och hjälpa till att välja antibiotika som både är effektiva för patienten och mer skonsamma för den bredare befolkningen.
Problemet med kraftfulla läkemedel
Modern medicin bygger på antibiotika, men överanvändning av bredspektrum—de så kallade "stora kanonerna"—driver en global kris med antimikrobiell resistens. FN har satt ett mål: till 2030 bör 70 % av antibiotikaanvändningen globalt komma från snävare, förstahandsmedel som WHO kallar "Access"-antibiotika. I praktiken lutar många kliniker mot bredare läkemedel, märkta som "Watch" eller "Reserve", eftersom de oroar sig för att ett smalare alternativ kan misslyckas mot resistenta bakterier, särskilt när patienterna är svårt sjuka. Som en följd byter vi ofta långsiktiga resistensrisker mot kortsiktig sinnesro, utan tydliga verktyg för att bedöma när en säkrare, snävare behandling faktiskt skulle fungera lika väl.
Lära en algoritm att tänka som en kliniker
Forskarna byggde en beslutstagandealgoritm för antibiotikabehandling vid UVI med hjälp av detaljerade elektroniska journaler från nästan 94 000 inlagda patienter i Boston. Först tränade de prediktionsmodeller för att uppskatta, för 13 olika antibiotika, hur sannolikt det var att de urinvägsframkallande bakterierna var känsliga, och hur stor risken var att behandlingen skulle utlösa problem som Clostridioides difficile-infektion eller allvarlig läkemedelstox icitet. Därefter bad de 49 kliniker i Storbritannien från flera specialiteter att genomföra en online-rankningsövning där de valde mellan fiktiva antibiotika som skiljde sig i egenskaper som biverkningsrisk, lämplighet för UVI, kostnad, om de var Access- eller Watch/Reserve-läkemedel, och om de gavs i tablettform eller intravenöst. Genom att analysera dessa rangordningar kvantifierade teamet hur starkt läkare värderade varje egenskap—till exempel hur mycket de föredrog UVI-riktade, lågtoxiska, orala läkemedel framför riskablare eller mer kraftfulla alternativ.
Lägga in en säkerhetskrock för mycket sjuka patienter
Den slutliga algoritmen blandade dessa två ingredienser: datadrivna prediktioner och klinikernas värdebedömningar. För varje patient beräknade den ett "behandlingsvärde" för varje antibiotikum, med hänsyn till den predikterade sannolikheten att läkemedlet skulle fungera, risken för allvarliga biverkningar, dess Access/Watch/Reserve-kategori och om det var oralt eller intravenöst. Avgörande var att algoritmen också byggde in en säkerhetsmekanism baserad på hur svårt sjuk patienten verkade i akutmottagningen. När sjukdomsgraden ökade gav algoritmen automatiskt större vikt åt att slå hårt mot infektionen och att ha en intravenös option tillgänglig. Med andra ord försökte den för lindrigt sjuka patienter gynna snäva, orala läkemedel, men i takt med att patienterna blev sjukare blev den successivt mer villig att använda starkare, intravenösa antibiotika för att skydda dem från behandlingsmisslyckande.
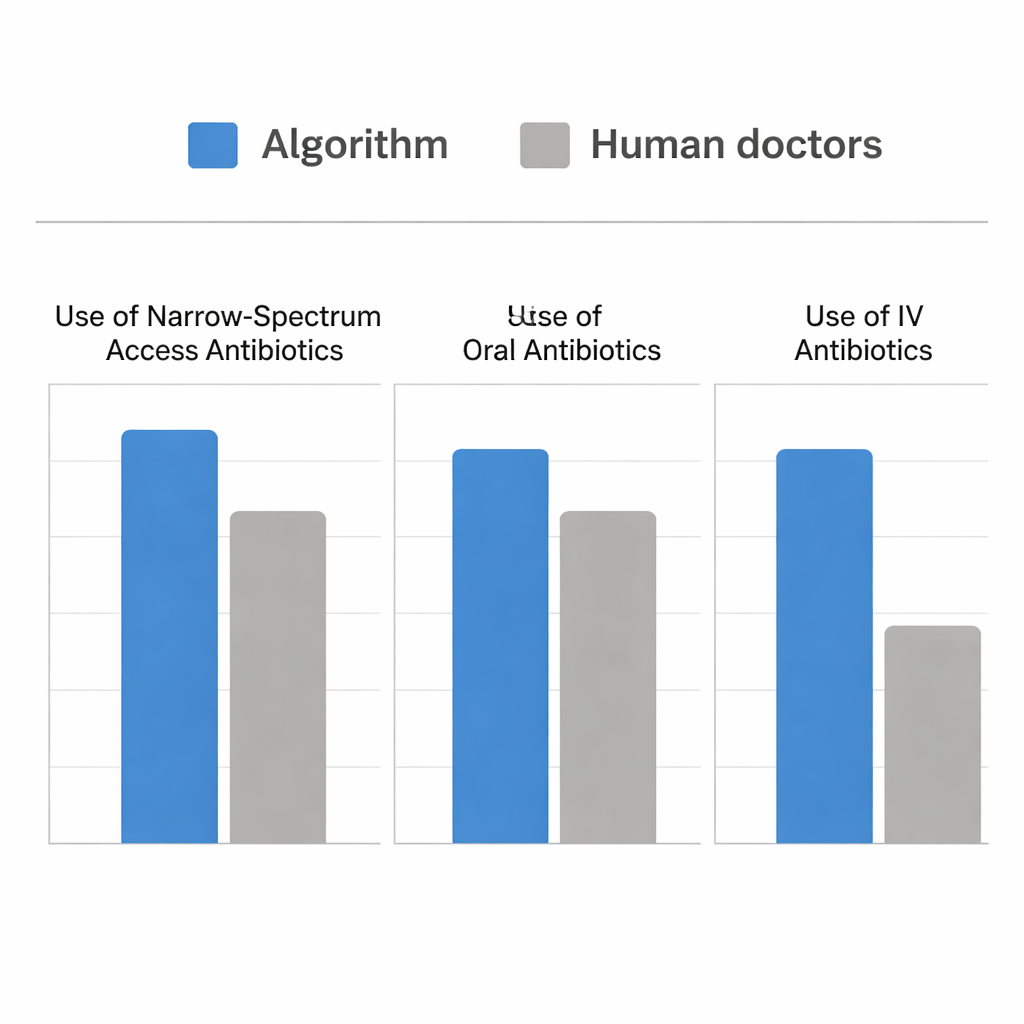
Hur algoritmen stod sig mot läkare
Teamet körde sedan en simulering med verkliga akutmottagningsfall där patienter hade UVI och urinodlingar. De jämförde de antibiotika som mänskliga kliniker faktiskt hade gett med de läkemedel algoritmen skulle ha valt i det ögonblick odlingen skickades. Båda tillvägagångssätten var lika bra på att välja ett antibiotikum som täckte patientens bakterier överhuvudtaget. Algoritmen gjorde det dock samtidigt som den valde betydligt fler snäva Access-läkemedel och fler orala behandlingar, samt använde färre intravenösa antibiotika. För sjukare patienter uppträdde algoritmen mycket likt mänskliga förskrivare och skiftade lämpligt mot intravenösa och mer kraftfulla läkemedel. Där den skilde sig var i att känna igen ytterligare möjligheter—särskilt hos måttligt sjuka patienter—att säkert behandla med orala Access-läkemedel såsom nitrofurantoin och ampicillin-sulbactam, istället för att som standard välja bredare alternativ.
Vad detta betyder för vardaglig vård
För en lekmannaläsare är huvudbudskapet att detta system inte ersätter läkare; istället fungerar det som en kalkylator för komplexa risk–nyttoavvägningar som kliniker redan bryr sig om men inte kan beräkna exakt i huvudet. Genom att förena klinikernas egna prioriteringar med storskalig evidens om hur antibiotika presterar kan algoritmen föreslå behandlingar som är minst lika effektiva för individen men skonsammare mot kroppen och för folkhälsan—att föredra tabletter framför dropp när det är säkert, och snävare läkemedel framför sista-hands-alternativ när så är möjligt. Om sådana verktyg valideras i fler miljöer kan de hjälpa sjukhus och vårdsystem att komma närmare globala mål för ansvarsfull antibiotikaanvändning, utan att offra säkerheten för personer som kommer in kritiskt sjuka med infektion.
Citering: Howard, A., Green, P.L., Zhong, Y. et al. Algorithmic antibiotic decision-making in urinary tract infection using prescriber-informed prediction of treatment utility. npj Digit. Med. 9, 136 (2026). https://doi.org/10.1038/s41746-026-02369-z
Nyckelord: urinvägsinfektion, antibiotikastyrning, kliniskt beslutsstöd, antimikrobiell resistens, maskininlärning i medicin