Clear Sky Science · sv
DARE-FUSE: domänanpassad, evidensstyrd inlärning för gemensam MR-segmentering och klassificering av hjärntumörer
Varför smartare hjärnavbildning spelar roll
Hjärntumörer är bland de mest fruktade diagnoserna inom medicinen, och magnetisk resonanstomografi (MR) är det främsta verktyget som läkare använder för att se var en tumör börjar och slutar. Även erfarna radiologer kan dock ha svårt att exakt avgränsa en tumör och bedöma hur den förändras över tid, särskilt när kanterna flyter ihop med svullen hjärnvävnad. Denna artikel presenterar DARE-FUSE, ett nytt artificiellt intelligenssystem utformat för att läsa hjärn-MR mer tillförlitligt, skapa skarpare tumörgränser och erbjuda tydligare förklaringar av sina beslut för att stödja kirurger, onkologer och patienter.
Sudda kanter och hektiska kliniker
I verkliga sjukhus är hjärn-MR-bilder röriga. Tumörer smälter ofta samman med omgivande svullnad, metalimplantat kan förvränga bilden och olika sjukhus använder något olika inställningar vid avbildningen. Radiologer måste manuellt bläddra genom hundratals bilder, markera tumören skiva för skiva och sedan avgöra hur den beter sig. Det arbetet är tidskrävande, utmattande och kan leda till meningsskiljaktigheter mellan experter. Befintliga AI-verktyg kan hjälpa till att avgränsa tumörer eller klassificera bilder som "tumör" eller "ingen tumör", men de flesta system hanterar dessa uppgifter separat, och många sviktar när bilderna kommer från nya centra eller innehåller subtil, oregelbunden tillväxt i kanterna.
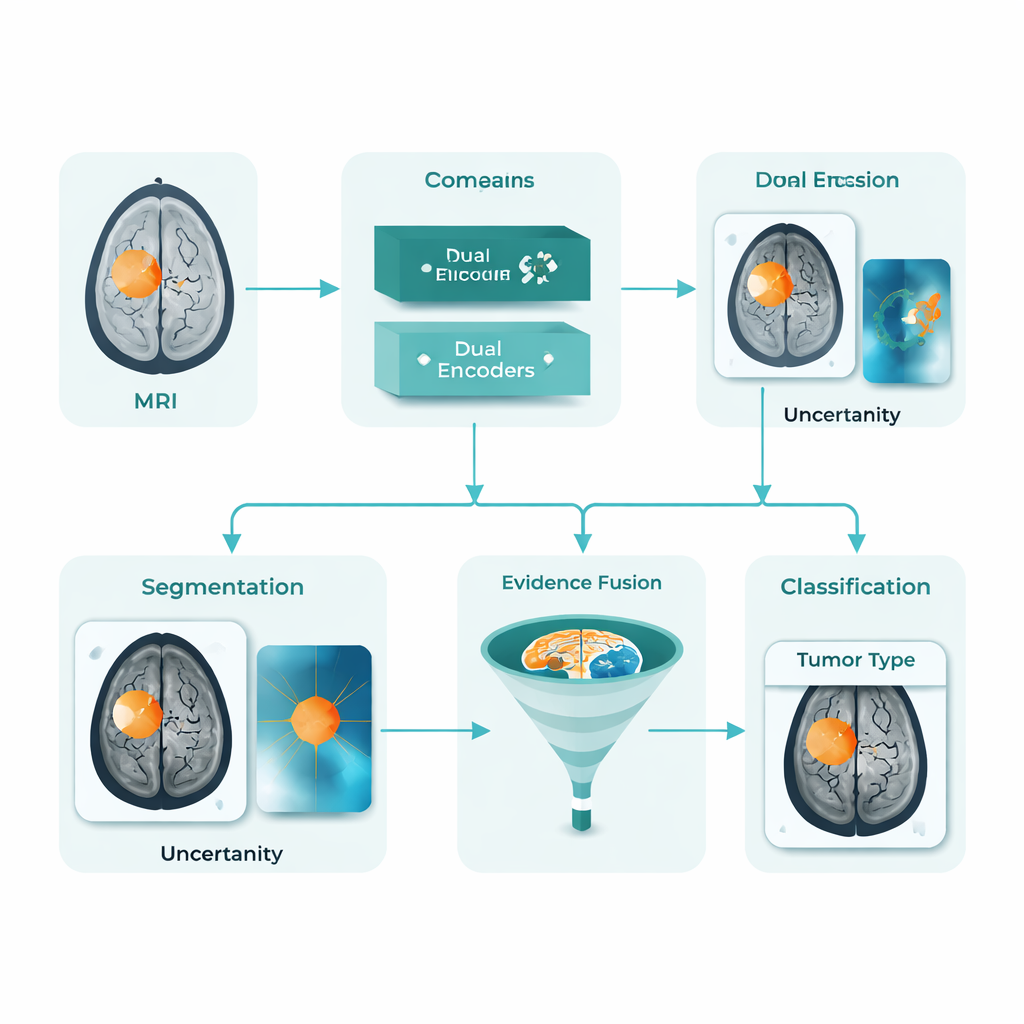
En enhetlig AI-assistent för tumörkartor och etiketter
DARE-FUSE tar itu med flera av dessa utmaningar samtidigt. Det är uppbyggt som en enda pipeline som både spårar tumören i varje MR-skiva (segmentering) och klassificerar hela bilder i diagnostiska grupper (klassificering). I kärnan finns två samverkande "vyer": ett nätverk inriktat på detaljerade former och gränser, och ett annat inriktat på globala mönster som skiljer olika tumörtyper åt. En särskild anpassningsmodul håller dessa vyer synkroniserade över sjukhus och skanners, så att kännetecken lärda från en datamängd inte försämrar prestandan på en annan. Systemet uppskattar också sin egen osäkerhet och flaggar i praktiken områden där det är mindre säkert på den exakta tumörkonturen, vilket är avgörande för säker klinisk användning.
Använda ledtrådar från värmekartor och "tumörfria" rekonstruktioner
I stället för att lita på en enda signal lär sig DARE-FUSE från flera typer av bevis. En gren producerar värmekartor som visar vilka delar av hjärnan som starkast stöder AI:ns klassificeringsbeslut. En annan gren använder en generativ modell för att föreställa sig hur samma skanning skulle se ut om tumören tagits bort, för att sedan jämföra den "tumörfria" versionen med originalet. Skillnaderna mellan de två framhäver subtila strukturella förändringar och kanter som kanske inte lyser upp tydligt i en standardvärmekarta. En fusionmodul kombinerar sedan dessa ledtrådar till en kontinuerlig "tumörprior"-karta: regioner där flera källor är ense behandlas som kärntumör, medan mindre säkra områden läggs till mer försiktigt och nedviktas när modellens osäkerhet är hög. Denna sammansatta prior vägleder slutkonturen och hjälper till att undvika både missade tumörcystor och felaktiga öar i frisk vävnad.
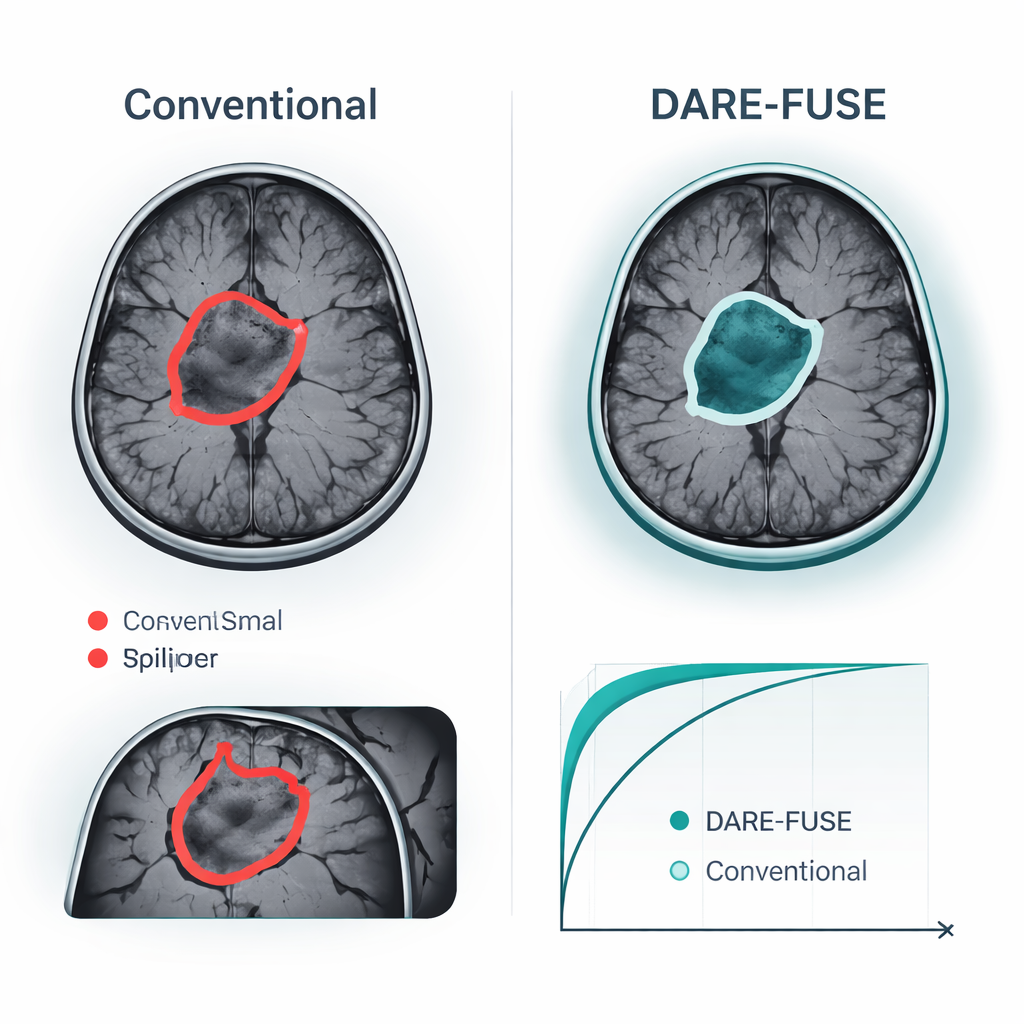
Visade förbättringar på offentliga hjärntumördatamängder
Författarna testade DARE-FUSE på sex stora, multicentriska hjärntumörutmaningar (BraTS-serien) och fyra öppna MR-samlingar som används för bildnivåklassificering. I samtliga BraTS-upplagor matchade eller överträffade systemet de bästa nyare djuplärandemodellerna, med något större overlap mellan sina förutsagda tumörmasker och experternas avritningar, och konsekvent mindre fel i den uppmätta tumörytan. Dessa förbättringar var mest påtagliga i svåra fall: små tumörer, lågkontrastkanter och komplexa, oregelbundna former. I klassificeringsuppgifterna — att avgöra exempelvis om en skanning visar en gliom, meningeom, hypofystumör eller ingen tumör — slagit DARE-FUSE även starka transformer- och svagt övervakade baslinjer vad gäller noggrannhet och ett standardmått för diskriminering (AUC). Viktigt är att när forskarna artificiellt minskade antalet detaljerade annoteringar försämrades det nya systemet gradvis och bibehöll ändå en fördel över semi- och svagt övervakade konkurrenter.
Vad detta kan betyda för patienter
För patienter och kliniker är DARE-FUSEs huvudsakliga löfte inte en spektakulär ny algoritm, utan mer pålitligt, tolkbart bildstöd. I praktiken skulle systemet kunna föreslå en tumörkontur, markera regioner där det är mindre säkert och visa värmekartor som förklarar vilka bildområden som driver dess klassificering. Läkare kan acceptera områden med låg osäkerhet som en startkontur och sedan rikta sin uppmärksamhet mot de flaggade regionerna istället för att rita om allt från början. Mer exakta och konsekventa mätningar av tumörvolym och form kan förbättra behandlingsplanering, målinriktning vid strålbehandling och uppföljning av behandlingssvar över tid. Författarna betonar att deras verktyg är en assistent — inte en ersättning — för expertbedömning, men deras resultat pekar mot AI-system som både kan se tumörer tydligare och kommunicera sin grad av säkerhet på sätt kliniker kan agera utifrån.
Citering: Liu, Y., Sun, C., Niu, Y. et al. DARE-FUSE: domain aligned evidence guided learning for joint brain tumor MRI segmentation and classification. npj Digit. Med. 9, 178 (2026). https://doi.org/10.1038/s41746-026-02365-3
Nyckelord: hjärntumör MR, medicinsk bildsegmentering, djuplärande inom radiologi, klinisk beslutsstöd, osäkerhetsmedveten AI