Clear Sky Science · sv
LLM-drivet samarbetsramverk för kunskapsförstärkt bedömning och hantering av cancersmärta
Varför smartare smärtvård spelar roll
Cancersmärta är inte bara en obehaglig biverkning — den kan dominera en persons sista månader eller år och försvåra sömn, rörelse och till och med enkla samtal. Trots att kraftfulla smärtstillande medel finns är det svårt att använda dem säkert och effektivt, särskilt när varje patient har olika cancerformer, andra sjukdomar och läkemedel. Denna artikel beskriver OncoPainBot, ett nytt artificiell intelligens-ramverk byggt på stora språkmodeller (LLM) som syftar till att hjälpa läkare att reda ut komplex journalinformation, följa uppdaterade riktlinjer och utforma säkrare, mer individualiserade smärtplaner för personer som lever med cancer.
Ett svårt problem i vardaglig cancervård
Cancersmärta kommer från många källor: tumörer som trycker mot ben eller nerver, operationer, kemoterapi och strålbehandling. Upp till 70 % av personer med avancerad cancer lever med betydande smärta, men lindringen är ofta ofullständig. Läkare måste balansera opioider, icke-opioida läkemedel och tilläggsbehandlingar samtidigt som de bevakar farliga biverkningar, särskilt hos patienter med nedsatt lever‑ eller njurfunktion. Nuvarande verktyg för smärtbedömning bygger tungt på korta skalor och fri text i journaler, vilket kan variera mellan vårdgivare och sjukhus. Som följd kan behandlingsbeslut skilja sig mycket åt och möjligheter att förbättra patientens välbefinnande missas.
Att omvandla medicinsk text till användbar insikt
LLM:er som ChatGPT och Claude kan läsa och sammanfatta långa, röriga dokument, vilket gör dem attraktiva för medicinskt arbete. Men vanliga ”chatbottar” är osäkra för cancersmärta eftersom de kan hitta på detaljer, missa läkemedelskonflikter eller ignorera de senaste riktlinjerna. OncoPainBot angriper dessa problem genom att kombinera LLM:er med en granskad kunskapsbas byggd från ledande cancerorganisationers smärtriktlinjer och genom att dela upp arbetet i fyra samarbetande ”agenter”, där varje agent motsvarar en verklig klinisk roll. En agent extraherar nyckelfakta om patientens smärta från elektroniska journaler, en annan resonerar om vilken typ av smärta som föreligger, en tredje utarbetar en behandlingsplan och en fjärde gör en säkerhetskontroll med fokus på läkemedelsinteraktioner, organfunktion och övervakningsbehov.
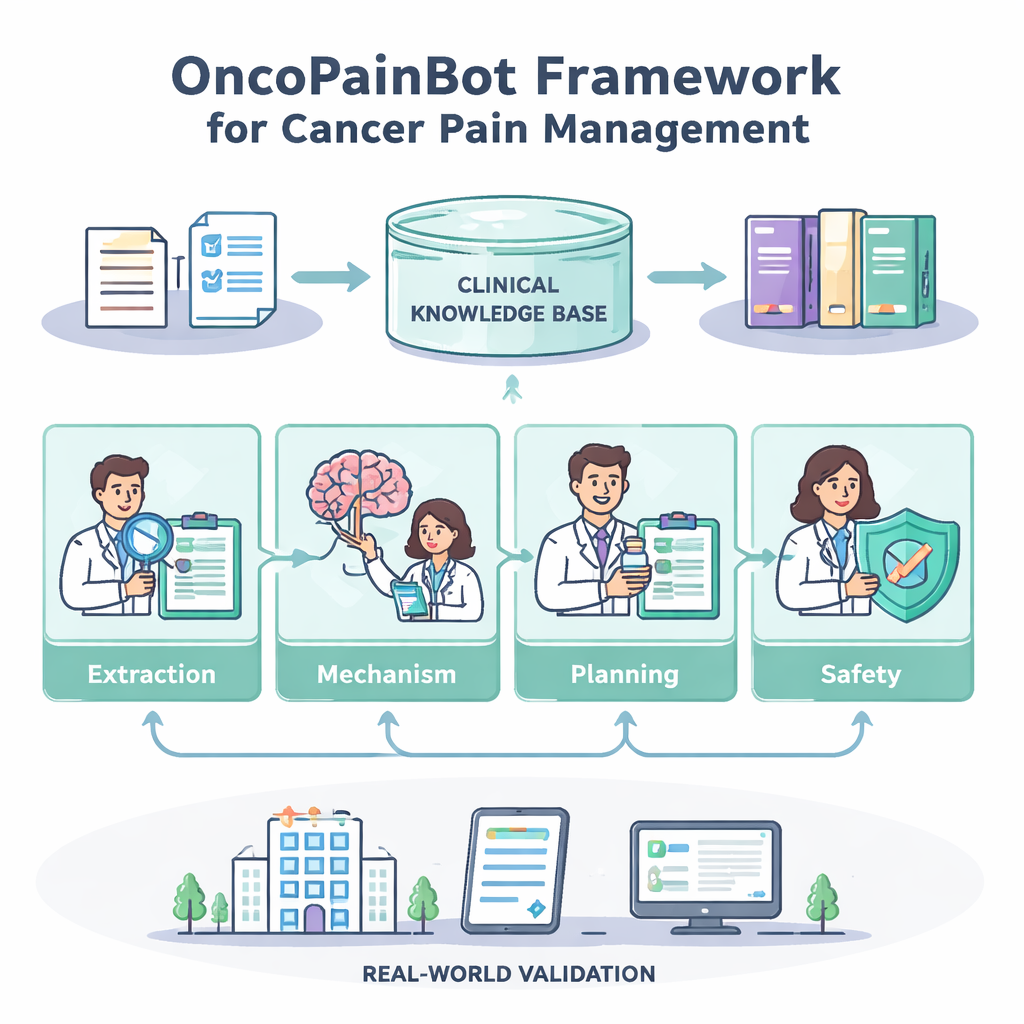
Hur fyragentlaget fungerar
Pain-Extraction-agenten läser fria textanteckningar och omvandlar dem till en strukturerad bild: var smärtan sitter, hur intensiv den är, vad som förvärrar eller lindrar den och vilka läkemedel som redan prövats. Pain-Mechanism Reasoning-agenten använder sedan denna bild för att sluta sig till om smärtan huvudsakligen beror på vävnadsskada, nervskada eller en blandning — en viktig ledtråd vid val av lämpliga läkemedel. Därefter konsulterar Treatment-Planning-agenten kunskapsbasen, som styrs av riktlinjer, genom en teknik kallad retrieval-augmented generation, vilket låter modellen hämta in specifika, aktuella avsnitt istället för att enbart förlita sig på intern kunskap. Den föreslår stegvisa planer — ofta förankrade i Världshälsoorganisationens (WHO) ”smärttrappa” — inklusive startdoser, sätt att justera dem och rescue-doser för plötsliga smärtgenombrott. Slutligen agerar Safety-Check-agenten som en försiktig farmaceut: den söker efter dosproblem, riskabla kombinationer och saknad laboratorieinformation samt markerar fall där underlaget är för tunt för en säker rekommendation.
Att pröva systemet
För att välja den bästa underliggande språkmodellen jämförde forskarna sju ledande system i flera medicinska fråge‑ och svarstester. Claude 4 visade sig vara mest korrekt, om än inte snabbast, och valdes därför som OncoPainBots ”hjärna”. De utvärderade sedan olika sätt att koppla denna hjärna till riktlinjebiblioteket och fann att en ”Hybrid”-hämtstrategi — som använder både nyckelordssökning och djupare semantisk sökning — gav de mest tillförlitliga svaren. Med denna uppsättning körde teamet OncoPainBot på 516 verkliga cancerpårsjournaler från ett stort kinesiskt sjukhus. Systemets skriftliga rapporter stämde väl överens med klinikernas egna anteckningar i både språk och innehåll, och dess förslag till smärtbehandling motsvarade läkares faktiska ordinationer i cirka 84 % av fallen. Viktigt är att de flesta avvikelser berodde på subtila, patient‑specifika nyanser — såsom odokumenterad opioidtolerans eller komplex organsvikt — snarare än uppenbart felaktiga läkemedelsval.
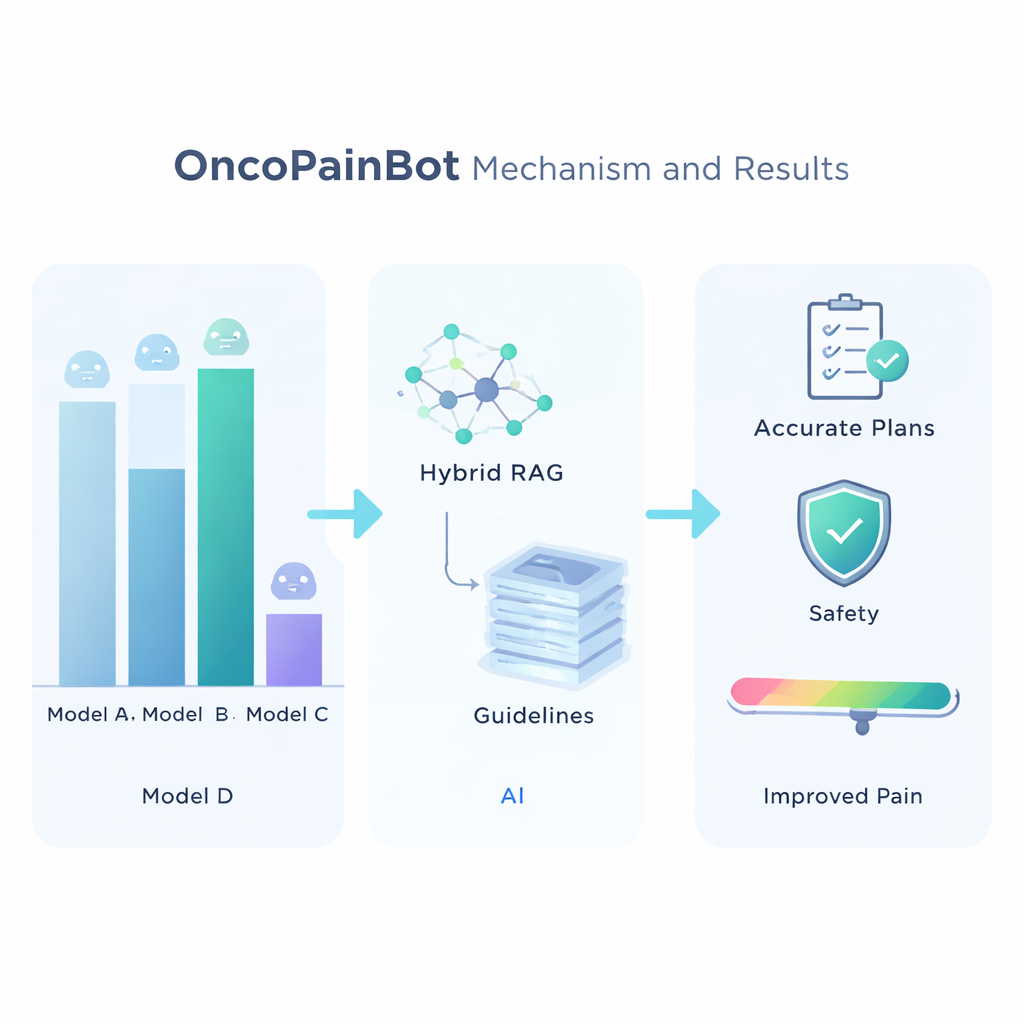
Vad detta kan betyda för patienter
För personer som lever med cancer innebär löftet med OncoPainBot inte att en maskin ska ta över deras behandling, utan att den ska ge vårdteamet en skarpare, mer konsekvent second opinion. Ramverket är utformat som ett verktyg med ”kliniker i loopen”: det lyfter fram smärtkaraktäristika som annars kan vara dolda i journaler, föreslår riktlinje‑alignerade alternativ och uppmärksammar säkerhetsrisker, samtidigt som de slutgiltiga besluten lämnas till människliga läkare. Författarna betonar att arbetet fortfarande är i ett tidigt, retrospektivt stadium och endast har testats på ett center; realtidsstudier över flera sjukhus krävs fortfarande. Ändå tyder deras resultat på att noggrant utformad AI — förankrad i robust evidens och transparent resonemang — skulle kunna hjälpa till att standardisera cancersmärtvården, minska farliga doseringsfel och, viktigast av allt, öka chansen att patienter tillbringar mindre tid lidande och mer tid med att leva sina liv.
Citering: Liu, H., Hu, Y., Li, D. et al. LLM-driven collaborative framework for knowledge-enhanced cancer pain assessment and management. npj Digit. Med. 9, 180 (2026). https://doi.org/10.1038/s41746-026-02362-6
Nyckelord: hantering av cancersmärta, kliniskt beslutsstöd, stora språkmodeller, opioidbehandling, retrieval-augmented generation