Clear Sky Science · sv
Tillämpning och framtidsutsikter för artificiell intelligens inom diagnostisk bildgivning av prostatacancer
Varför smartare undersökningar spelar roll för mäns hälsa
Prostatacancer är en av de vanligaste cancerformerna hos män, och att upptäcka den tidigt kan skilja mellan ett mindre hälsoproblem och en livshotande sjukdom. Denna översikt förklarar hur artificiell intelligens (AI) integreras i moderna medicinska avbildningar för att hitta prostatacancer tidigare, bedöma hur farlig den är och följa om behandlingarna fungerar. För läsaren ger den en inblick i hur datorer blir tysta medarbetare i avläsningsrummet, som hjälper läkare att fatta snabbare och mer konsekventa beslut samtidigt som nya frågor uppstår kring data, rättvisa och förtroende.
Från suddiga skuggor till datarika bilder
Läkare förlitar sig på flera bildgivande verktyg för att leta efter prostatacancer. Ultraljud är snabbt och billigt men har svårt att skilja cancer från ofarlig förstoring eller inflammation. Magnetresonanstomografi (MRI) ger detaljerade bilder av mjukdelar och är nu det främsta testet för kliniskt signifikant prostatacancer, men det tar tid att tolka och även experter är ofta oense. PET/CT‑undersökningar med spårämnen som binder till ett protein kallat PSMA på cancerceller är utmärkta för att hitta spridning till ben och lymfkörtlar men kan missa mycket små förändringar och är kostsamma. AI ersätter inte dessa maskiner; istället lägger den sig ovanpå de bilder de producerar. Algoritmer rengör och segmenterar först skannarna, och extraherar sedan subtila mönster i ljusstyrka, textur och form. Dessa osynliga ledtrådar, i kombination med laboratorieresultat som PSA‑värden, används för att träna modeller som kan markera misstänkta områden, uppskatta cancerrisk och föreslå var man bör ta biopsi eller hur man bedömer behandlingssvar.
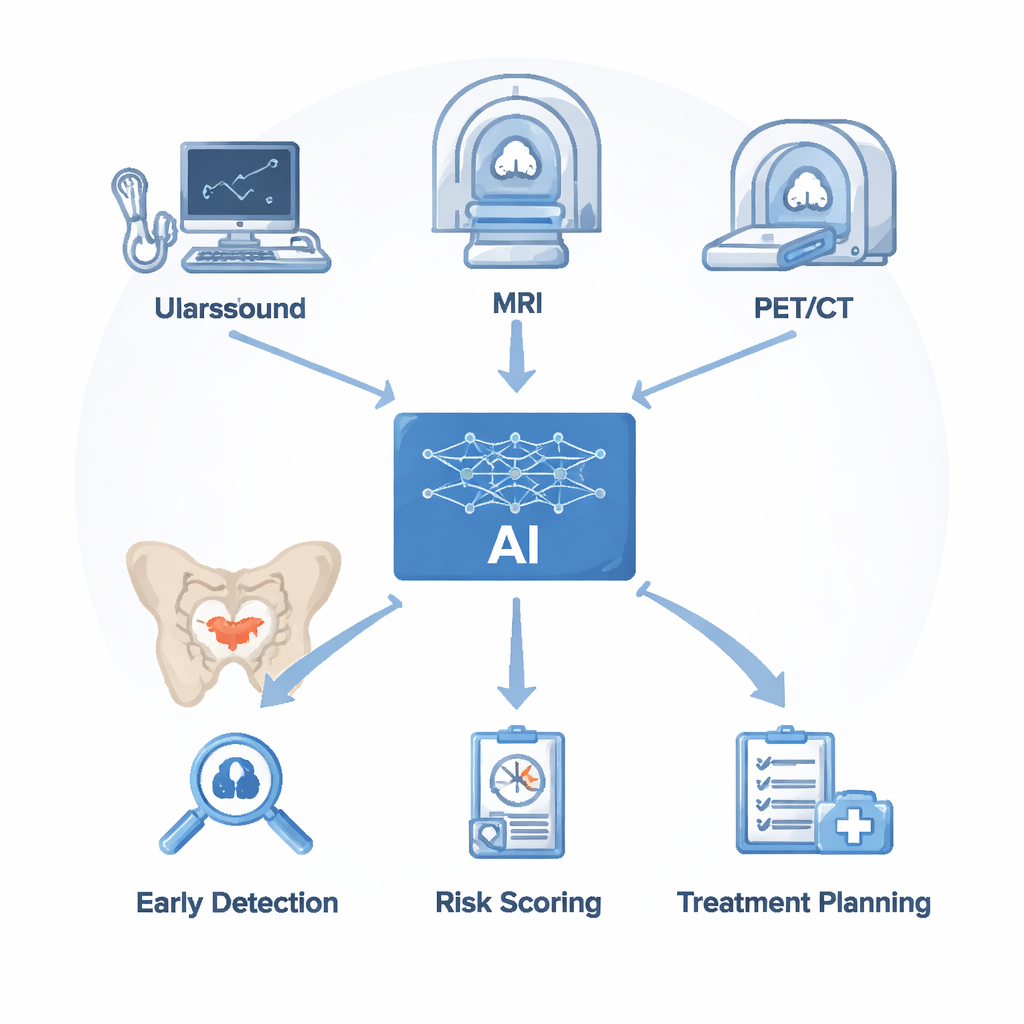
Att lära datorer se det radiologer missar
I ultraljud lär sig AI‑system från hundratals exempel att upptäcka cancerregioner som kan smälta in i bakgrunden. Djupa nätverk kan automatiskt lokalisera prostatan och markera sannolika tumörer i realtid, ibland motsvara eller överträffa erfarna sonografer samtidigt som de bibehåller hastighet och minskar missade små lesioner. Radiomikmetoder går ett steg längre och omvandlar ultraljudsbilder till stora mängder siffror som fångar vävnadsmönster för komplexa för det mänskliga ögat. Maskininlärningsmodeller byggda på dessa egenskaper har tydligt överträffat traditionellt ultraljud och PSA ensamt, särskilt för män vars PSA‑nivåer hamnar i den förvirrande ”gråzonen”, där äldre metoder ofta felklassificerar nästan hälften av fallen. Liknande principer driver AI för MRI, där avancerade nätverk automatiskt ritar upp prostatan och dess inre zoner, vilket minskar manuell konturering från omkring 20 minuter till knappt över en minut och avsevärt förbättrar överensstämmelsen mellan olika läsare.
Skarpare riskuppskattningar och smartare uppföljning av behandling
AI kommer till sin rätt när den sammanför information från flera MRI‑sekvenser som visar anatomi, vattenrörelse och blodflöde. Transformer‑baserade modeller, anpassade från språkbehandling, fusionerar dessa indata för att producera sannolikhetskartor över kliniskt viktiga tumörer. I tester på stora patientgrupper har sådana system matchat eller överträffat erfarna radiologer, särskilt för små tumörer under en centimeter som människor ofta förbiser. Vid dynamisk kontrast‑MRI kan tidsseriemodeller läsa de förändrade ljusstyrkekurvorna hos injicerat kontrastmedel för att uppskatta hur läckiga tumorns blodkärl är—en indikator kopplad till mer aggressiv sjukdom och högre risk för återfall. I PSMA PET/CT upptäcker tredimensionella nätverk tränade på helkroppsskanningar automatiskt skelett‑ och lymfkörtelmetastaser, mäter total tumörbörda och relaterar den till hur länge patienter förblir fria från progression. Andra AI‑verktyg jämför skanningar tagna före och kort efter hormon‑ eller cytostatikabehandling och förutsäger behandlingsutfall flera månader i förväg, mycket tidigare än traditionella regler baserade på enkla upptagningsförändringar.
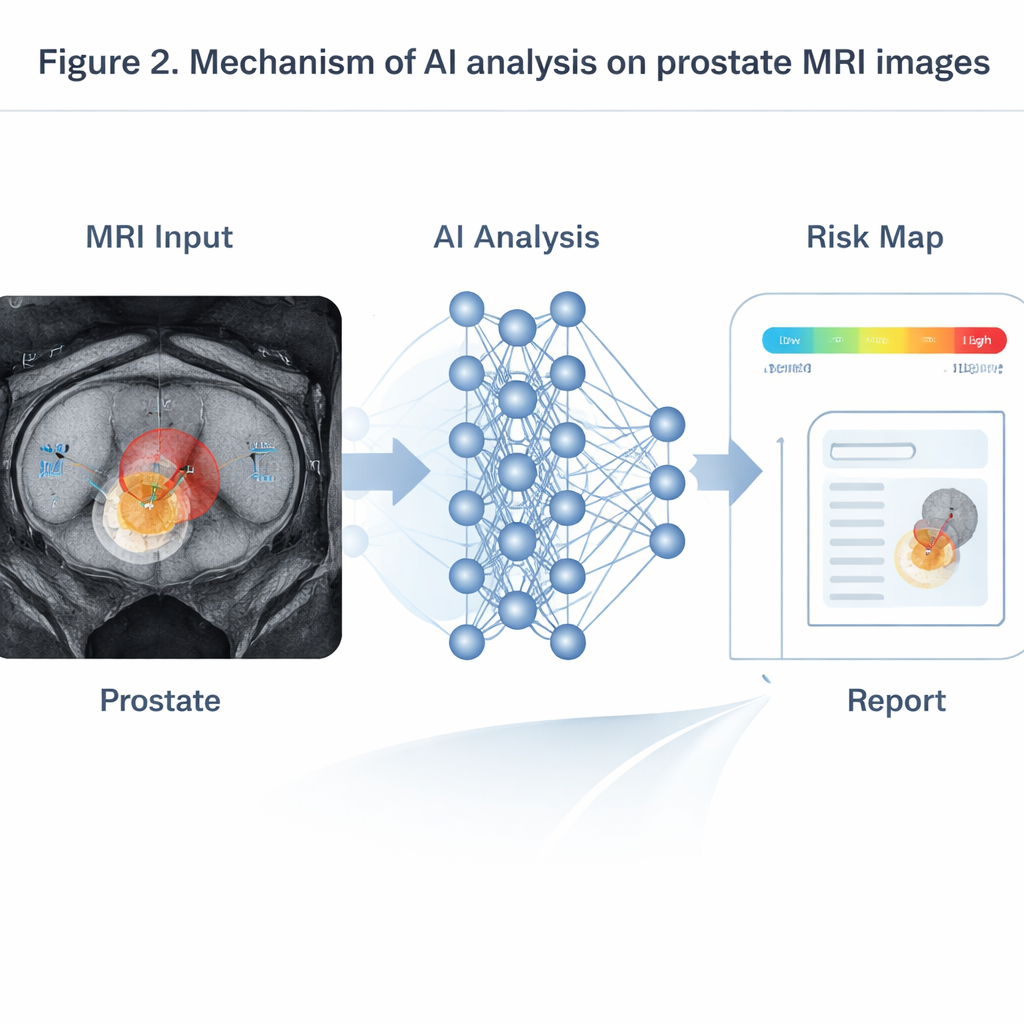
Hinder: databrister, svarta lådor och rättvis användning
Trots framstegen möter verklig implementering allvarliga hinder. Högkvalitativa, väl annoterade bilddata är fortfarande begränsade och snedvridna mot stora universitetskliniker, medan skanningar från mindre centra och olika populationer är underrepresenterade. Subtila skillnader mellan skannermärken, inställningar och bildkvalitet kan få modeller tränade på ett ställe att misslyckas på ett annat. Många kraftfulla AI‑system fungerar som ”svarta lådor” och ger en riskpoäng utan klar förklaring, vilket undergräver läkarnas förtroende—särskilt när datorn inte håller med klinisk erfarenhet. Översikten lyfter också fram oro kring integritet, begränsningar i datadelning och risken att modeller presterar sämre för vissa grupper, vilket potentiellt kan vidga hälsoklyftor om det inte övervakas och åtgärdas noggrant.
Bygga pålitliga partners i kliniken
Framåt ser författarna AI mer som en betrodd medspelare än en mystisk spåman. De skisserar ansträngningar för att bygga stora, delade datamängder över sjukhus samtidigt som integriteten bevaras genom tekniker som federerad inlärning, där endast modelluppdateringar—inte råa patientdata—utbyts. Nya ”förklarliga AI”‑verktyg syftar till att visa vilka bildregioner som drev ett beslut och koppla dem till känd patologi, vilket ger läkare konkreta skäl att hålla med eller motsätta sig. Istället för universella modeller kommer skräddarsydda system att fokusera på specifika uppgifter: screening i upptagna kliniker, vägledning vid biopsier, övervakning av behandling eller uppföljning av högriskpatienter. Att kombinera bildgivning med genetiska och kliniska data kan ytterligare förfina prognos och individualisera terapi. För patienter är slutsatsen uppmuntrande: om tekniska, etiska och regulatoriska utmaningar hanteras väl kan AI‑förstärkt bildgivning innebära tidigare upptäckt, färre onödiga biopsier, snabbare svar och mer skräddarsydda behandlingsplaner för prostatacancer.
Citering: Wang, X., Zhong, S., Fang, K. et al. Application and prospect of artificial intelligence in diagnostic imaging of prostate cancer. npj Digit. Med. 9, 168 (2026). https://doi.org/10.1038/s41746-026-02354-6
Nyckelord: prostatacancerbildgivning, artificiell intelligens, MRI och ultraljud, PSMA PET/CT, radiomik