Clear Sky Science · sv
Maskerad autoenkodning, generaliserbar förtränin g och integrerade experter för förbättrad gliomsegmentering
Varför smartare skanningar spelar roll för hjärntumörer
Hjärntumörer som kallas gliom är bland de dödligaste cancerformerna, och ändå ägnar läkare fortfarande mycket tid åt att manuellt spåra tumörgränser i MR‑bilder. Denna noggranna avgränsning styr operation och strålbehandling, men kan ta 15–20 minuter per patient och måste upprepas över tid. Studien presenterar MAGPIE, ett artificiellt intelligenssystem som lär sig från tiotusentals hjärnskanningar utan mänskliga etiketter och sedan bara behöver ett fåtal expertmärkta fall för att pålitligt kartlägga gliom. För patienter kan detta innebära snabbare och mer konsekvent behandlingsplanering, även på sjukhus som saknar stora, förädlade dataset.
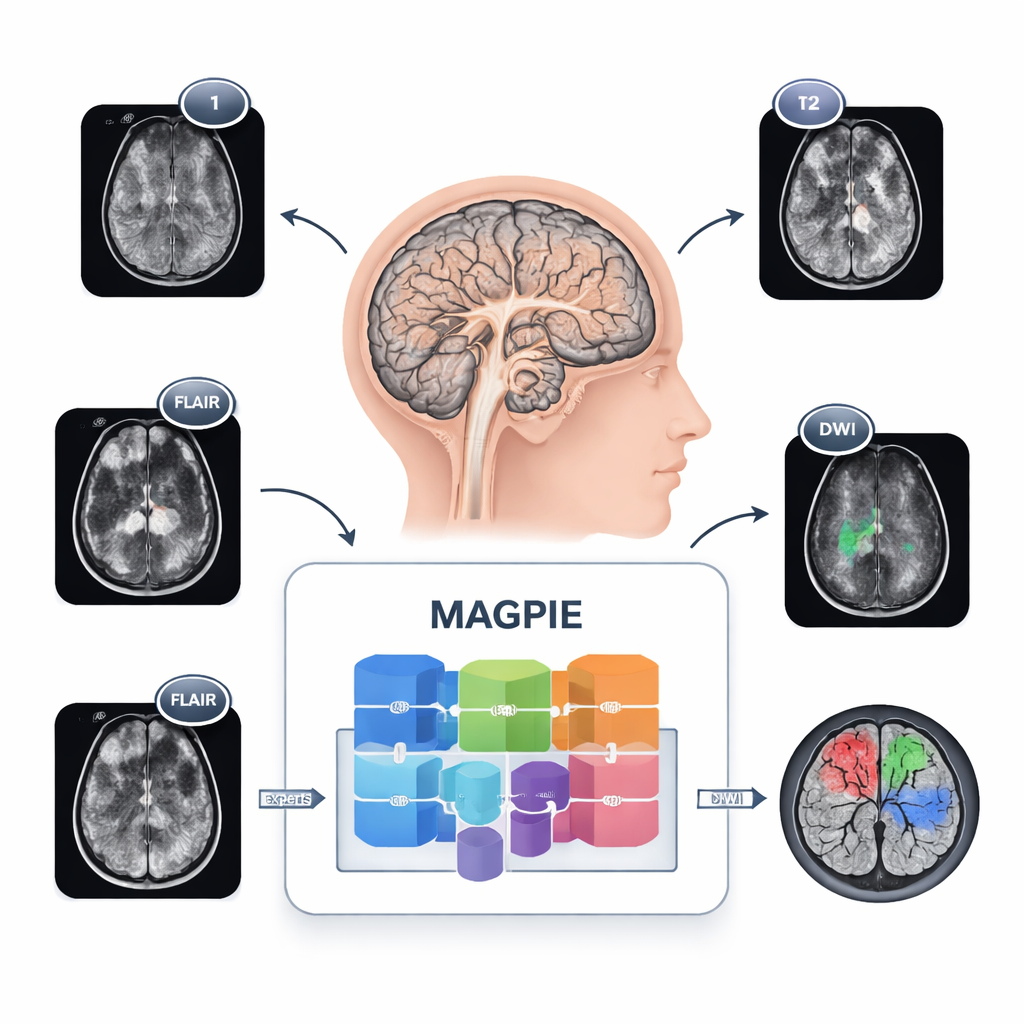
Att se tumörer på ett nytt sätt
Gliom är svåra att kartlägga eftersom de inte bildar prydliga klot. Cancerceller sprider sig längs hjärnans ledningsbanor och ger upphov till otydliga kanter och små satellitfokus som är svåra att upptäcka. Olika sjukhus använder dessutom olika MR‑protokoll och kombinationer av sekvenser, så ett verktyg tränat på ett ställe kan få problem på ett annat. MAGPIE hanterar allt detta samtidigt. Det exponerades först för 43 505 oetiketterade hjärn‑MRI‑skanningar hämtade från många studier och skannertyper. Under denna fas lärde det sig generella mönster för frisk och sjuk hjärnvävnad genom att försöka återskapa borttagna bilddelar och genom att jämföra olika förstärkta vyer av samma hjärna, vilket tvingade modellen att fokusera på stabila, meningsfulla egenskaper snarare än sköra pixeldetaljer.
Låta flera experter dela arbetet
I stället för att vara en enda monolitisk modell innehåller MAGPIE en "blandning av experter" internt. När den analyserar en ny skanning aktiverar den bara en liten delmängd av åtta specialiserade subnätverk för varje region av bilden. Under träningen delar dessa experter naturligt upp uppgiften: några blir känsliga för den ljusa, aktivt växande tumörranden; andra identifierar den döda kärnan; ytterligare andra lär sig den diffusa ring av svullnad runt tumören; och vissa fokuserar främst på normal hjärnbakgrund och gränser. Författarna visar detta genom att mäta hur starkt varje experts aktivitet överlappar de olika tumörzonerna som radiologer ritat ut. Denna arbetsdelning förbättrar noggrannheten samtidigt som beräkningen hålls hanterbar—endast omkring hälften av modellens parametrar är aktiva för en given bildruta.
Hantera röriga, verkliga skanningar
Kliniska MR‑protokoll är långt ifrån enhetliga. Vissa patienter har fyra sekvenser, andra färre; maskiner från olika tillverkare ger subtilt olika bilder. MAGPIE:s design behandlar varje MR‑sekvens som en separat "token" och lär sig hur mycket vikt varje sekvens ska tilldelas i realtid, i stället för att förvänta sig en fast uppsättning indata i en bestämd ordning. Detta kanalagnostiska angreppssätt gör att systemet kan anpassa sig om till exempel en kontrastförstärkt sekvens saknas men FLAIR är närvarande. Modellen använder också avancerade attention‑mekanismer som låter den både "se långt", fånga långdistansspridning längs vit substans‑banor, och "se precist", upptäcka mycket små lesioner på bara några millimeter.
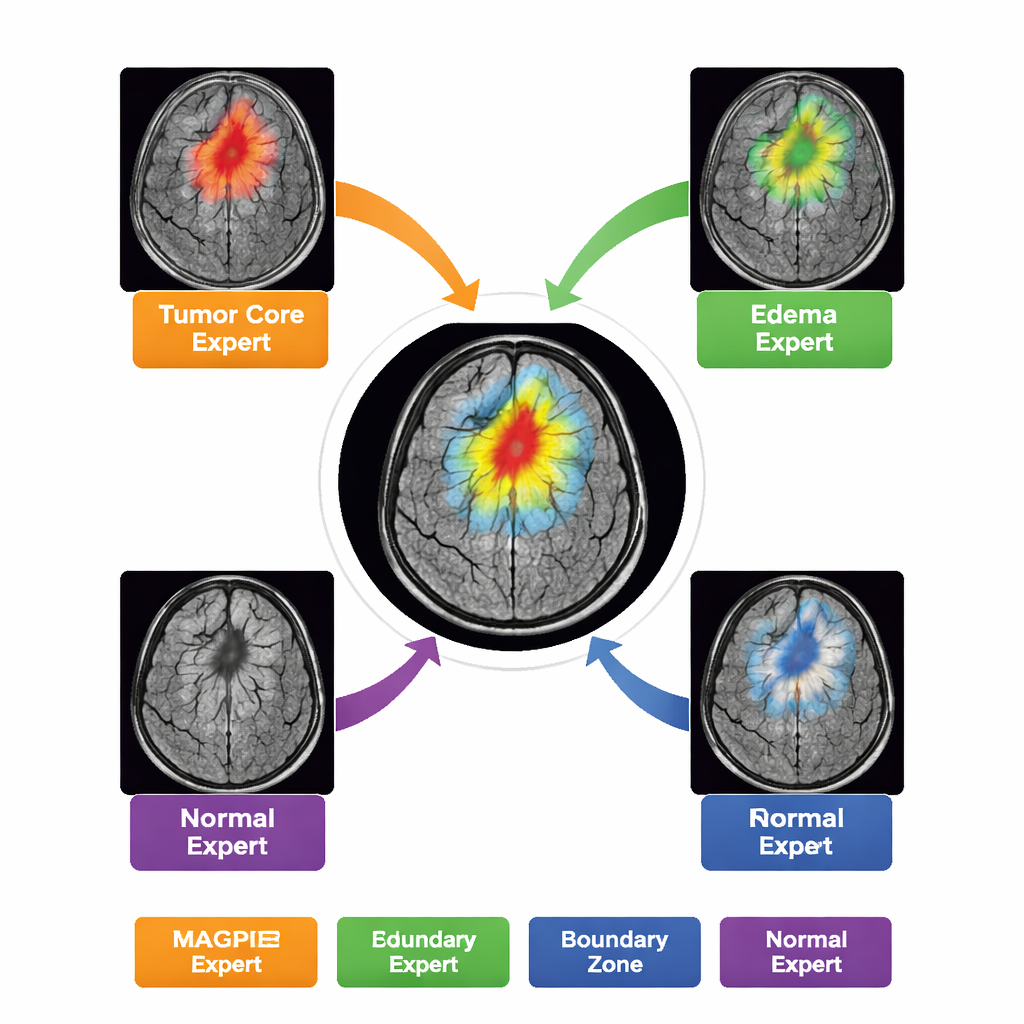
Mera med betydligt färre etiketter
Efter förtränin g finjusterade forskarna MAGPIE på endast 20 fullt etikettera de gliomfall och jämförde det med standardmodeller tränade från början under samma förhållanden. På ett stort benchmark för hjärntumörer (BraTS21) uppnådde MAGPIE ett Dice‑poäng—en vanlig överlappsmått i medicinsk bildbehandling—på omkring 61 %, vilket slog den bästa från‑scratch‑versionen med ungefär 2,6 procentenheter och överträffade en stark tidigare självövervakad metod utan att visa någon skadlig "negativ överföring". På utmanande out‑of‑distribution‑data—skanningar från olika sjukdomar, skannertyper och bildinställningar—höll den sig också bättre och nådde över 70 % Dice på ett dataset med vit substans‑lesioner utan extra justering. Viktigt är att denna prestandanivå normalt kräver i storleksordningen 400 etikettera de fall; MAGPIE når den med bara cirka 5 % av den ansträngningen.
Vad detta kan betyda för patienter och kliniker
För icke‑experter är huvudbudskapet att MAGPIE förvandlar ett berg av oetiketterade MR‑skanningar till en kraftfull assistent som kräver mycket lite expertträning för att bli kliniskt användbar. Den kan avgränsa komplexa hjärntumörer med realistiska gränser, upptäcka små satellitfokus som andra system missar och fortsätta fungera tillförlitligt när skanningar kommer från okända maskiner eller saknar vissa sekvenser. Denna kombination kan minska radiologers annoteringstid med omkring 95 %, sänka tröskeln för mindre sjukhus att ta i bruk avancerad bild‑AI och stödja mer preciserad kirurgi och strålplanering. Även om ytterligare validering på sällsynta tumörtyper och låggradiga fall fortfarande behövs, visar studien hur omsorgsfullt utformad självövervakad inlärning kan föra robust, dataeffektiv hjärntumörsegmentering närmare vardaglig klinisk verklighet.
Citering: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Nyckelord: gliomsegmentering, hjärn‑MRI, självövervakad inlärning, blandning av experter, medicinsk bild‑AI