Clear Sky Science · sv
Respons på midostaurin vid AML formas av ett progenitorliknande celltillstånd som selektivt riktas av SMAC‑mimetika
Varför vissa leukemiläkemedel slutar fungera
För många personer med en typ av blodcancer som kallas akut myeloisk leukemi (AML) har nya riktade läkemedel gett hopp — men inte alla får nytta av dem, och svaren försvinner ofta med tiden. Denna studie ställer en enkel men avgörande fråga: varför ignorerar vissa leukemiceller ett ofta använt läkemedel, midostaurin, och kan vi hitta en smart kombination som tvingar dessa envisa celler att dö?
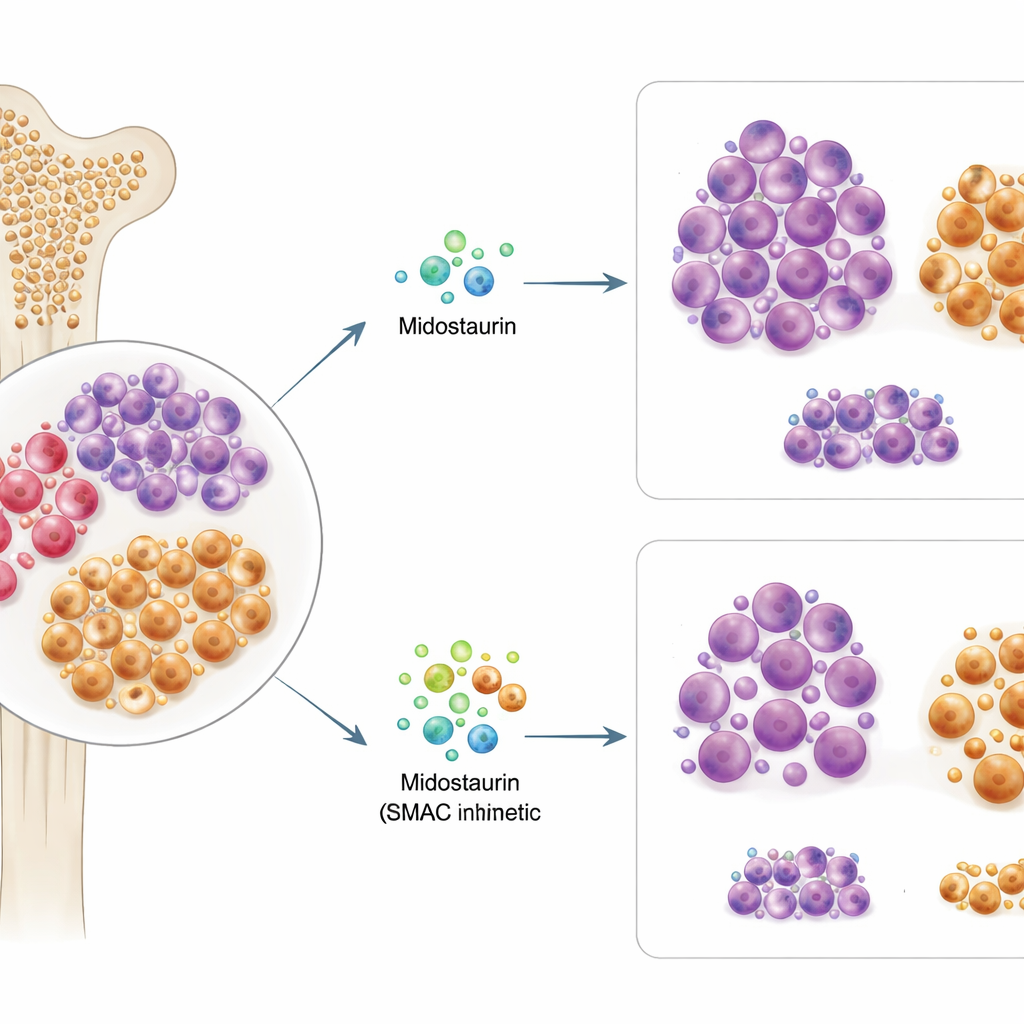
Att se bortom huvudmutationen
Cirka en av tre AML‑patienter bär på en förändring i genen FLT3, som driver leukemitillväxt och är anledningen till att midostaurin förskrivs. Forskarna testade benmärgs‑ och blodprover från 63 patienter med FLT3‑muterad AML och exponerade cellerna för midostaurin och mer än 500 andra cancerläkemedel i laboratoriet. De fann att hur känsliga patienternas celler var för midostaurin ex vivo nära överensstämde med hur den patienten senare svarade kliniskt. Överraskande nog förutsade inte den exakta typen av FLT3‑mutation eller dess kvantitet pålitligt midostaurinframgång, vilket tyder på att genetik ensam inte kan förklara vem som drar nytta av behandlingen.
En dold pool av envisa ”frö”celler
Betraktligt djupare analyser visade att teamet jämförde övergripande protein‑ och genaktivitetsmönster mellan celler som var känsliga för midostaurin och sådana som inte var det. Icke‑responsiva prover var berikade på egenskaper hos omogna, stamcellsliknande progenitorceller — celler närmare blodbildningens rot och som antas fungera som ”frön” som kan återstarta leukemin. Däremot liknade responsiva prover mer delvis mogna immunceller och myeloida celler. Med avancerade enkelcellsmetoder identifierade forskarna en specifik population av leukemiceller markerade av ytmolekylerna CD38 och CD45RA som uppträdde som dessa progenitorliknande frön. Dessa celler visade ovanlig organisation av sitt yttre membran, vilket antyder att viktiga signalmolekyler arrangerades på sätt som gynnade överlevnad.
Överlevnads‑koppling: en växling i signalvägar
Midostaurin är utformat för att blockera FLT3‑signalering, som normalt matar en kedja av signaler inklusive molekylen STAT5 och kan driva celltillväxt. När teamet undersökte signalering i cellinjer och patientprover efter midostaurinbehandling såg de två skilda mönster. I midostaurin‑känsliga celler sjönk STAT5‑aktiviteten snabbt, i linje med effektiv FLT3‑inhibering. I resistenta celler dominerade däremot en annan väg: PI3K/AKT, en klassisk överlevnadsrutt som hjälper celler att motstå celldöd. Dessa resistenta celler upprätthöll eller ökade till och med AKT‑aktiviteten efter behandling och visade högre nivåer av proteiner som blockerar apoptos (programmerad celldöd). Med andra ord verkade kopplingarna inuti dessa progenitorliknande celler vara omkopplade för att gynna överlevnad även när FLT3 hämmas.
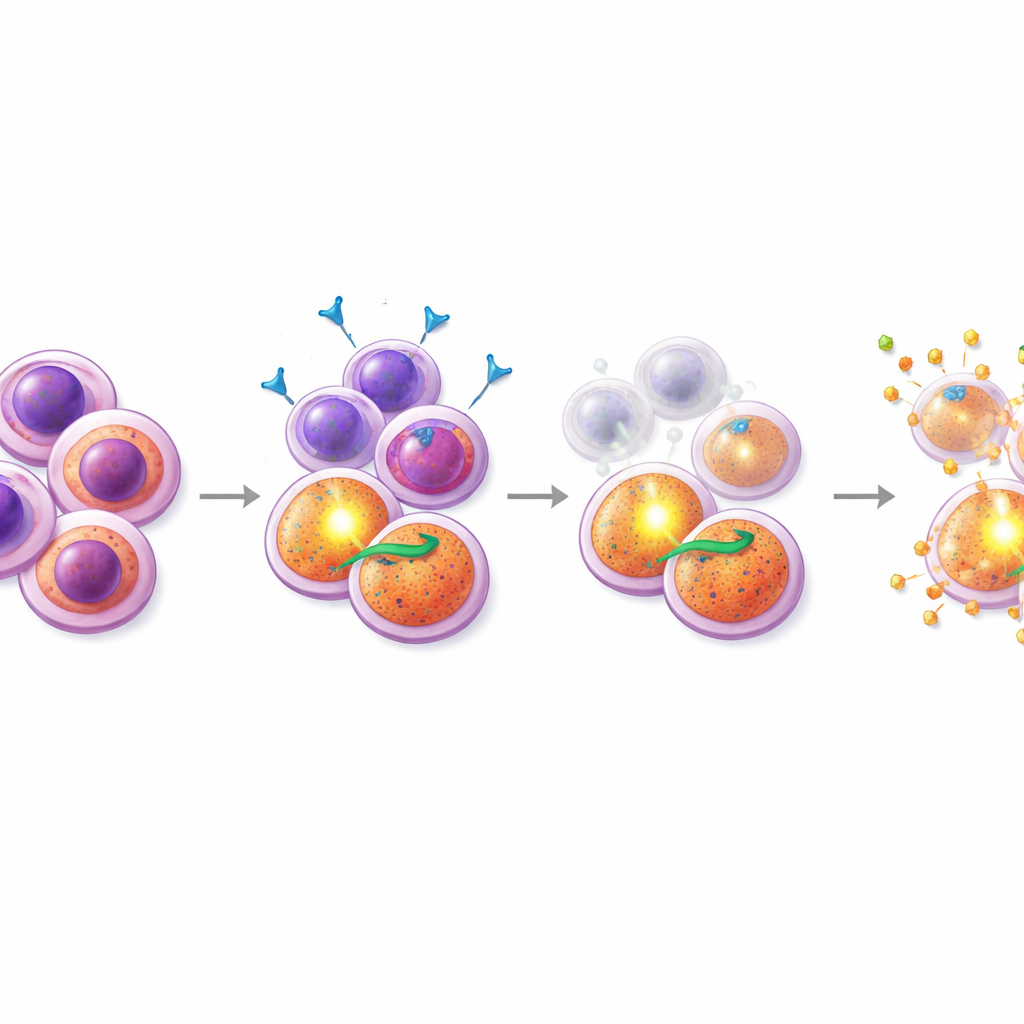
Att hitta en partnerläkemedel som träffar svaga punkten
Med denna insikt screendade forskarna kombinationer av midostaurin med hundratals andra föreningar, med fokus på läkemedel som påverkar celldöd. En framstående grupp var SMAC‑mimetika, läkemedel som inaktiverar de ”hämmarna av apoptos” proteiner som PI3K/AKT‑drivna celler är beroende av. I resistenta patientprover och en resistent FLT3‑mutant cellinje gav tillsats av SMAC‑mimetika såsom birinapant till midostaurin stark synergism: tillsammans dödade läkemedlen betydligt fler celler än någon av dem för sig. Viktigt nog visade detaljerade flödescytometriexperiment att midostaurin–SMAC‑mimetika‑kombinationen selektivt utarmade den CD38+CD45RA+ progenitorliknande populationen och reducerade dess karakteristiska ytmarkörnivåer, vilket tyder på att denna terapi specifikt riktar sig mot de svårslagna fröna. Till skillnad därom var kombinationer med den godkända BCL‑2‑hämmaren venetoclax mer effektiva mot en annan, CD34‑hög undergrupp och visade inte samma fokuserade effekt på de resistenta cellerna.
Vad detta betyder för patienter
Denne studie tyder på att resistens mot midostaurin inte bara handlar om själva FLT3‑mutationen, utan också om leukemicellernas ”tillstånd” — deras mognadsnivå, membranorganisation och föredragna överlevnadsvägar. En progenitorliknande CD38+CD45RA+ undergrupp verkar vara ett centralt reservoar för resistens, som skiftar sin signalering från den vanliga STAT5‑vägen till ett överlevnadsvänligt PI3K/AKT‑program. Genom att kombinera midostaurin med SMAC‑mimetika kunde forskarna återkänsliggöra dessa celler och driva dem mot celldöd i laboratoriet. Även om större kliniska studier fortfarande krävs pekar fynden mot en framtid där läkare kan använda funktionell testning och celltillståndsprofilering, inte bara DNA‑sekvensering, för att välja FLT3‑inriktade kombinationer som slår ut både den stora leukemin och dess mest motståndskraftiga frön.
Citering: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
Nyckelord: akut myeloisk leukemi, FLT3‑hämmare, läkemedelsresistens, leukemiska stamceller, SMAC‑mimetika