Clear Sky Science · sv
COL3A1-höga cancerassocierade fibroblaster orkestrerar metabola och immuna mikroenvironments för att ge kemoterapiresistens vid bröstcancer
Varför vissa brösttumörer nonchalerar kemoterapi
Kemoterapi kan rädda liv vid bröstcancer, men många patienter upplever att deras tumörer slutar svara eller aldrig svarade väl från början. Denna studie tittar bortom cancercellerna själva och undersöker grannskapet de lever i: vilka närliggande celler hjälper tumörer att överleva behandlingen och hur gör de det? Svaret kretsar kring en särskild grupp stödjeceller som omprogrammerar både tumörernas näringstillgång och den lokala immuniteten för att skydda cancerceller från kemoterapi.
De dolda medhjälparna runt tumören
Brösttumörer består av mer än bara cancerceller; de är blandade samhällen som innefattar blodkärl, immunceller och bindvävsceller kallade fibroblaster. När fibroblaster finns i en tumör kallas de cancerassocierade fibroblaster, eller CAFs, och de kan antingen hämma eller främja cancer. Genom att kombinera flera kraftfulla genetiska profileringsmetoder på patientprover—single-cell, spatial och bulkanalyser—tillsammans med laboratorium- och djurförsök, identifierade forskarna en CAF-subgrupp som producerar höga nivåer av en molekyl kallad COL3A1, en komponent i vävnadens stomme. Patienter vars tumörer innehöll fler av dessa COL3A1-höga CAFs löpte större risk att få dåligt svar på kemoterapi och sämre överlevnad.
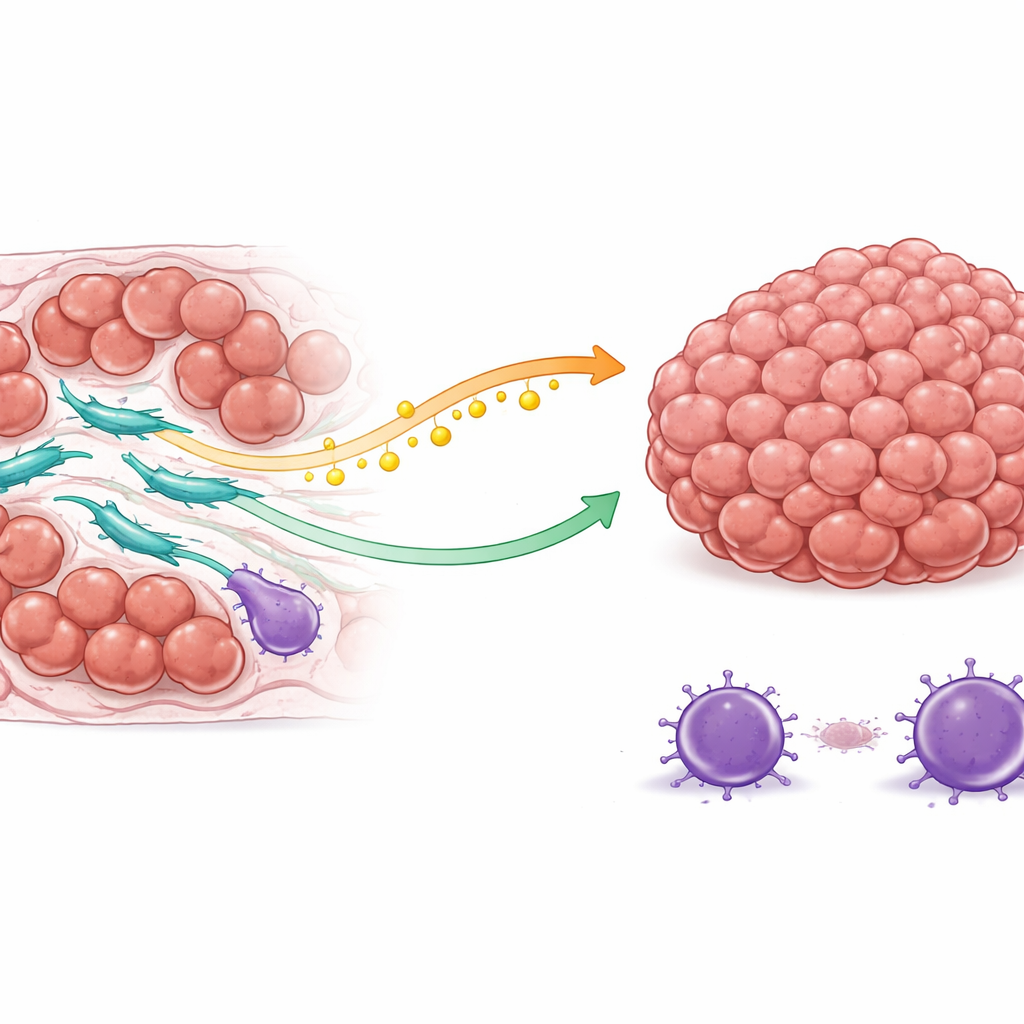
En tvådelad sköld: bränsle och skydd
Teamet upptäckte att COL3A1-höga CAFs skyddar cancerceller på två huvudsakliga sätt. För det första ändrar de hur de hanterar fetter. Dessa fibroblaster ökar aktiviteten hos ett enzym som tillverkar oljesyra, en typ av fett. Istället för att behålla detta bränsle släpper de ut det i tumörens omgivning. Cancerceller tar upp oljesyran via ett ytprotein och som svar slår de på en intern överlevnadssignalväg som är känd för att hjälpa celler att motstå dödssignaler. Som ett resultat, när kemoterapi försöker utlösa självdödsprogram i cancercellerna, är dessa celler bättre rustade att motstå och fortsätta dela sig.
Formar ett ogästvänligt immunt landskap
För det andra omformar COL3A1-höga CAFs den lokala immunmiljön till tumörens fördel. Genom komplexa signalinteraktioner lockar de regulatoriska T‑celler, en typ av immuncell som dämpar immunsvar, samtidigt som de avskräcker eller försvagar cytotoxiska T‑celler som normalt skulle attackera cancer. Rumslig kartläggning av riktiga patienttumörer visade att dessa fibroblaster tenderar att ligga nära både läkemedelsresistenta cancerceller och suppressiva immunceller, medan effektiva cytotoxiska T‑celler pressas längre bort. Denna ordning skapar en skyddad zon där cancerceller möter färre immuna hot samtidigt som de blir svårare att döda med läkemedel.
Bevis från celler, möss och patienter
För att testa orsakssamband minskade forskarna COL3A1 i CAFs odlade i laboratoriet. När bröstcancerceller odlades tillsammans med dessa förändrade fibroblaster bildade de färre invasiva strukturer, dödades lättare av cytostatikumet paklitaxel och visade mer tecken på programmerad celldöd. I möss implanterade med blandningar av bröstcancerceller och CAFs bromsade blockering av COL3A1 i fibroblasterna tumörtillväxten under kemoterapi och sänkte nivåerna av enzymet för fettsyntes samt cancercellreceptorn kopplad till oljesyra. I en grupp på 72 patienter som behandlades med kemoterapi före operation visade högre nivåer av COL3A1 och dess fettmetaboliska partners stark korrelation med sämre behandlingssvar och kortare tid tills cancer återkom.
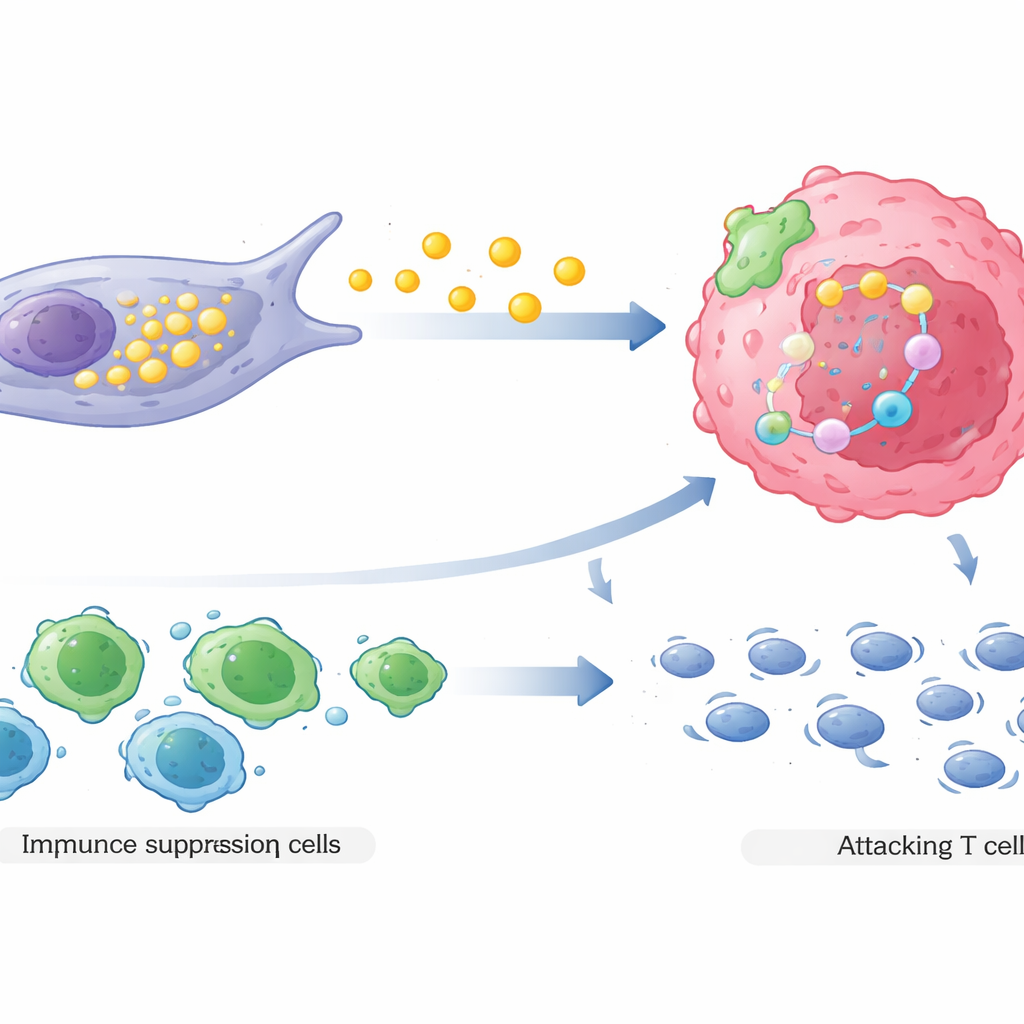
Vad detta betyder för framtida behandling
Kort sagt visar studien att en särskild uppsättning stödjeceller i brösttumörer agerar som en livvaktspatrull: de matar cancerceller med en skyddande fettbaserad diet och rekryterar immunkontakter som dämpar kroppens försvar. Tillsammans gör dessa åtgärder kemoterapi mindre effektiv. Att mäta mängden COL3A1‑höga fibroblaster förbättrar läkares förmåga att förutsäga vem som kommer att svara på behandlingen, och de vägar som används—fettproduktion, överlevnadssignalering inne i cancerceller och immunhämning—erbjuder nya måltavlor för läkemedel. I framtiden skulle terapier som oskadliggör eller omprogrammerar dessa fibroblaster kunna kombineras med standardkemoterapi för att förhindra att tumörer utvecklar resistens.
Citering: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
Nyckelord: bröstcancer, kemoterapiresistens, tumörmikromiljö, cancerassocierade fibroblaster, lipidmetabolism