Clear Sky Science · sv
Förutsäga brist på homolog rekombination och behandlingssvar med en datortomografibaserad foundation-modell: en preklinisk studie
Varför detta är viktigt för patienter och läkare
Kreftbehandlingar som skadar DNA, såsom vissa cytostatika och nya riktade läkemedel, kan vara särskilt effektiva mot tumörer vars reparationssystem redan är felaktiga. Utmaningen är att avgöra vilka tumörer som har dessa dolda svagheter utan att förlita sig på upprepade, invasiva biopsier. Denna studie undersöker om rutinmässiga medicinska skannedar hos möss, tolkade av en kraftfull artificiell intelligensmodell, kan avslöja hur sårbar en tumör är och hur väl den kommer att svara på ett nytt experimentellt läkemedel.
En dold svag punkt i cancerceller
Många tumörer bär på defekter i en central DNA‑reparationsväg som kallas homolog rekombination. När denna väg sviktar samlas skador i arvsmassan, ett tillstånd som kallas brist på homolog rekombination, eller HRD. HRD kan göra att cancer lättare bildas, men det blir också en akilleshäl: läkemedel som ytterligare skadar DNA kan få dessa redan stressade celler att gå under, och döda dem mer effektivt än friska celler. I dag identifieras HRD ofta med genetiska tester eller specialiserade laboratorieanalyser som är kostsamma, tidskrävande och ofta kräver att delar av tumören tas ut. Författarna undrade om avbildning — samma slags tredimensionella röntgenskanningar som används brett i kliniker — skulle kunna erbjuda ett snabbt, icke‑invasivt fönster mot HRD.
Använda intelligenta skanningar istället för fler biopsier
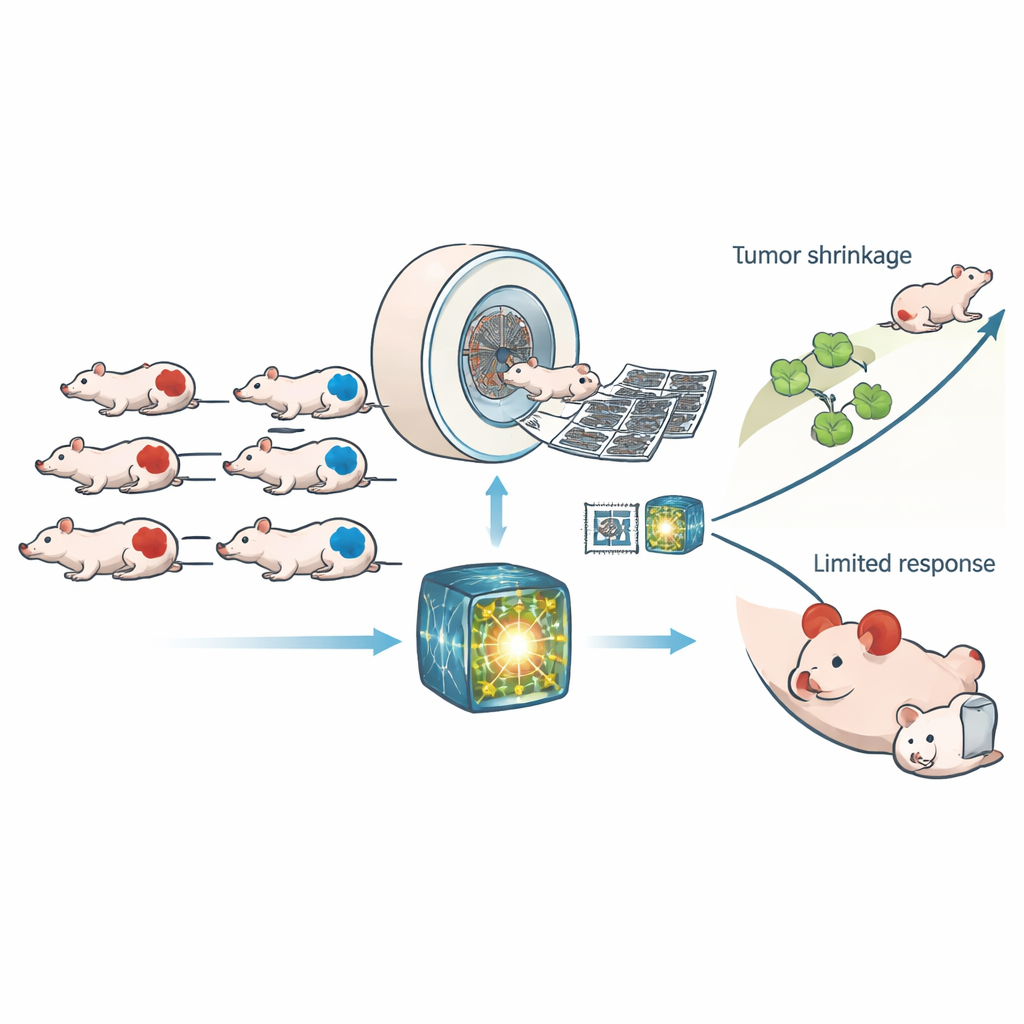
Forskarna arbetade med 307 möss som bar mänskliga tumörtransplantat som antingen var HRD eller normala vad gäller reparationsförmåga. Alla djur genomgick högupplöst datortomografi (CT) före och efter att ha fått antingen en kontrollbehandling eller CP‑506, ett experimentellt läkemedel som aktiveras i låga syreområden i tumörer och korslänkar DNA‑strängar. Istället för att förlita sig på ett fåtal handgjorda bildmått använde teamet en modern ”foundation‑modell” tränad på stora mänskliga CT‑datamängder för att extrahera tusentals subtila mönster från varje skanning. En enkel klassificerare tränades sedan på dessa mönster för att avgöra om en tumör var HRD, och samma inlärda funktioner återanvändes för att förutsäga hur mycket DNA‑skada och tillväxthämning CP‑506 skulle orsaka.
Hur bra avbildningsmodellen klarade uppgiften
Foundation‑modellen överträffade tydligt både traditionell radiomik och ett standard djupinlärningsnätverk som tränades från början. På nya testskanningar särskiljde den HRD‑ från icke‑HRD‑tumörer med en area under kurvan på cirka 0,88, en noggrannhetsnivå som höll över olika CT‑energinställningar. När båda AI‑metoderna var överens om tumörtypen ökade prestandan ännu mer. Modellens bildbaserade HRD‑poäng stämde väl överens med den verkliga genetiska statusen i flera prostatacancer‑ och kolorektala tumörlinjer, även om en linje med ovanligt reparationsbeteende fortfarande var svårare att klassificera. Viktigt är att CT‑egenskaperna kopplade till HRD inte bara var statistiska artefakter: de förutsade också hur mycket bestående DNA‑skada CP‑506 orsakade 48 timmar efter behandling och hur lång tid det tog för tumörer att växa tillbaka till fyrdubbel storlek i ett parallellt experiment.
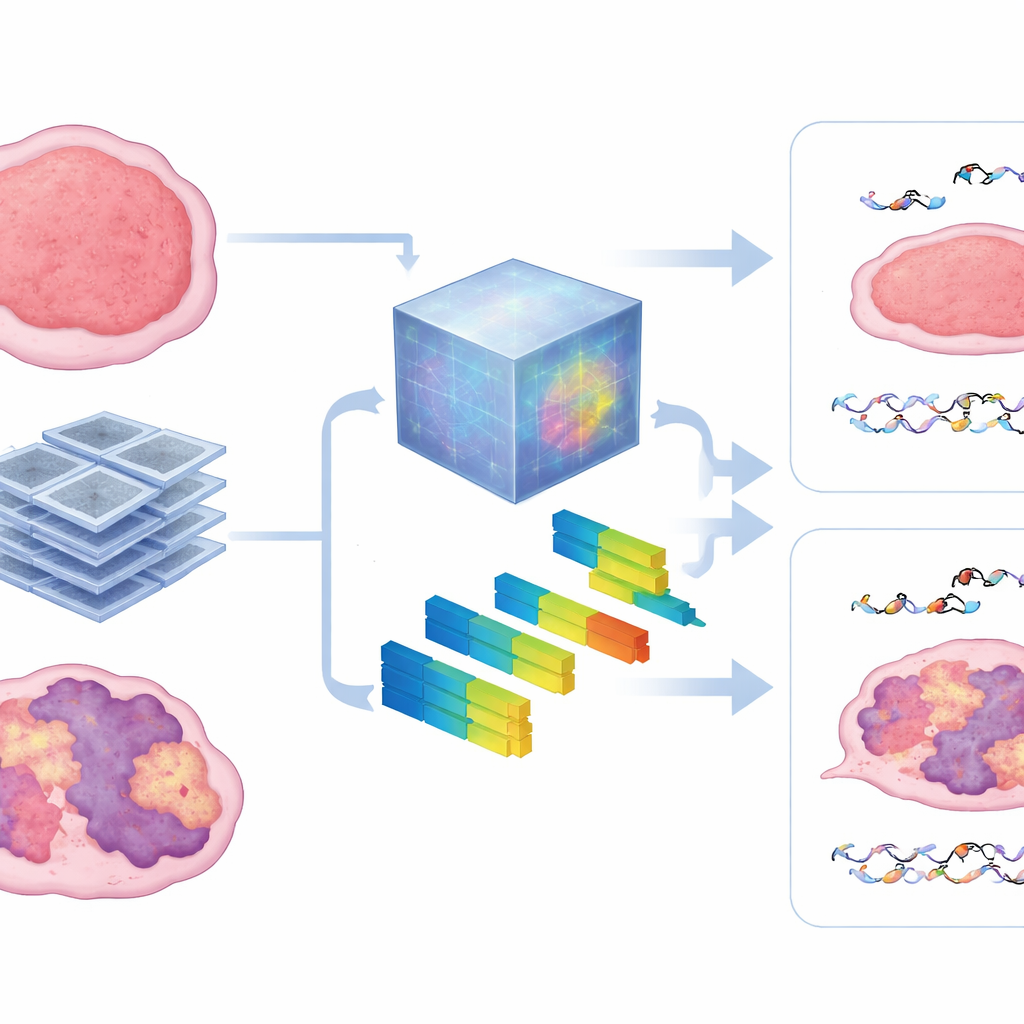
Vad skanningarna avslöjar inne i tumören
För att titta in i den svarta lådan jämförde författarna mönstren som foundation‑modellen lärde sig med standardradiomiska mått som beskriver bildtextur och intensitet. De fann att modellen i hög grad förlitade sig på mått av heterogenitet — hur fläckig, grov eller oregelbunden tumören såg ut på CT. Tumörer med starkare HRD‑signaturer visade sig tendera att uppvisa mer oorganiserade texturer, och dessa samma egenskaper hjälpte till att förutsäga både mikroskopisk DNA‑skada och makroskopisk tumörkontroll. Metoden förblev robust även när mindre träningsdata fanns tillgängliga, vilket antyder att sådana förtränade modeller kan övervinna ett stort hinder i djurstudier, där det är svårt att samla stora avbildningsdatamängder.
Från musförsök till framtida patientvård
Detta prekliniska arbete visar att en enda CT‑skanning, tolkad genom en kraftfull, förtränad AI, kan fånga signaler om defekt DNA‑reparation och förutse hur kraftigt en tumör kommer att svara på ett DNA‑skadande läkemedel. För en lekmannapublik är slutsatsen att standardliknande skanningar snart kan göra dubbel nytta — lokalisera en tumör och avslöja hur skör den är — utan extra ingrepp. Innan detta blir en del av rutinvården måste metoden testas och valideras hos mänskliga patienter. Lyckas dessa insatser kan CT‑baserade AI‑fingeravtryck för HRD hjälpa läkare att matcha patienter mer precist till behandlingar som CP‑506 och besläktade terapier, förbättra utfallen samtidigt som andra skyddas från ineffektiva, toxiska läkemedel.
Citering: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Nyckelord: brist på homolog rekombination, canceravbildning, radiomik, foundation-modeller, DNA‑skadande terapi