Clear Sky Science · sv
Utveckling och validering av en artificiell intelligens‑baserad modell för diagnostik av benigna, gränsfalliga och maligna adnexala tumörer
Varför detta är viktigt för kvinnors hälsa
Ovariala och andra adnexala tumörer är vanliga fynd vid bäcken‑ultraljud, men att avgöra vilka som är ofarliga och vilka som kan vara tidig cancer är fortfarande svårt, även för experter. Denna studie beskriver ett nytt system baserat på artificiell intelligens (AI), kallat Clinical‑OMTA, som läser ultraljudsbilder och hjälper läkare att dela upp dessa tumörer i tre viktiga grupper—benigna, gränsfalliga och maligna—så att kvinnor får rätt behandling samtidigt som onödiga operationer kan undvikas.
Tre typer av tumörer, tre mycket olika val
Inte alla adnexala tumörer är likadana. Benigna förändringar kan ofta följas upp eller tas bort med enkel kirurgi. Maligna tumörer är livshotande cancerformer som kräver specialistkirurgi och ofta cytostatika. Gränsfalliga tumörer ligger mitt emellan: de kan recidivera men drabbar ofta yngre kvinnor som vill bevara fertiliteten, så kirurger försöker begränsa ingreppet till det nödvändiga. Tyvärr kan dessa tre kategorier se mycket lika ut på ultraljud. Gränsfalliga tumörer kan särskilt likna antingen en ofarlig cysta eller en aggressiv cancer, vilket gör behandlingsbesluten stressande för både patient och kliniker.
Att omvandla komplexa skanningar till tydligare svar
Ultraljud är vanligtvis det första och mest lättillgängliga testet för adnexala tumörer, men tolkning av de korniga, mycket varierande bilderna kräver omfattande erfarenhet. Befintliga poängsystem och riskkalkyler, som den välanvända ADNEX‑modellen, kombinerar specifika ultraljudsfynd med enkla kliniska uppgifter som ålder och en blodmarkör (CA125), men de förlitar sig fortfarande på att människor korrekt beskriver bilderna. Nyare arbete inom djupinlärning—en gren av AI som lär sig mönster direkt från pixlar—ger en möjlighet att minska dessa subjektiva moment genom att träna datorer att känna igen subtila bildsignaturer för olika tumörtyper.
En AI‑assistent tränad över många sjukhus
Med utgångspunkt i tidigare arbete utformade författarna Clinical‑OMTA, en tvåvägsmodell som först skiljer benigna från icke‑benigna förändringar och sedan särskiljer gränsfalliga från maligna tumörer. Systemet bearbetar gråskalebilder från ultraljud och kan även ta ålder och CA125‑värden som valfria indata. För att lära upp och testa modellen samlade teamet en stor, mångsidig datamängd: 2381 kvinnor från 23 sjukhus i Kina, skannade med 38 olika ultraljudsapparater. De flesta fallen hade kirurgisk verifiering av diagnosen; en mindre grupp tydligt benigna cystor bekräftades genom minst sex månaders ultraljudsuppföljning. Data delades upp i träningsset, interna testset och två helt oberoende externa testkohorter, inklusive både stillbilder och korta videogenomdrag av ovarierna. 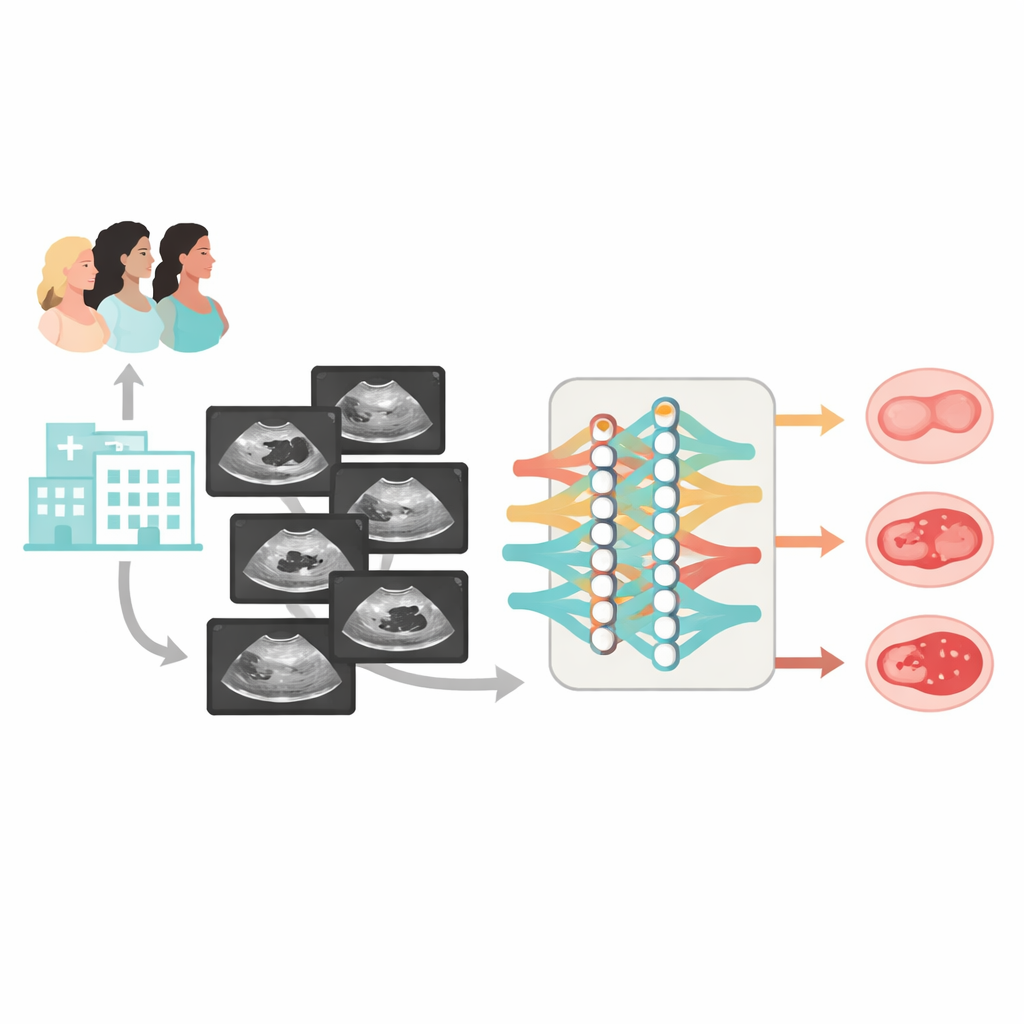
Hur väl AI:n presterade i verkliga miljöer
På externa testbilder skiljde Clinical‑OMTA korrekt mellan benigna, gränsfalliga och maligna tumörer med en noggrannhet som var jämförbar med både ADNEX‑modellen och bedömningen från en erfaren ultraljudsundersökare. Dess prestanda var stabil över olika ultraljudsmärken, skanningsmetoder (genom buken eller via vagina) och de två externa sjukhusen, vilket tyder på att modellen inte är överanpassad till en viss apparat eller center. Systemet fungerade också väl på videoklipp, inte bara på stillbilder. Intressant nog förbättrade inmatning av ålder och CA125 inte besluten jämfört med att använda endast ultraljudsbilder, vilket bekräftar tidigare studier som visar att denna blodmarkör tillför lite när högkvalitativ bilddata finns tillgänglig. 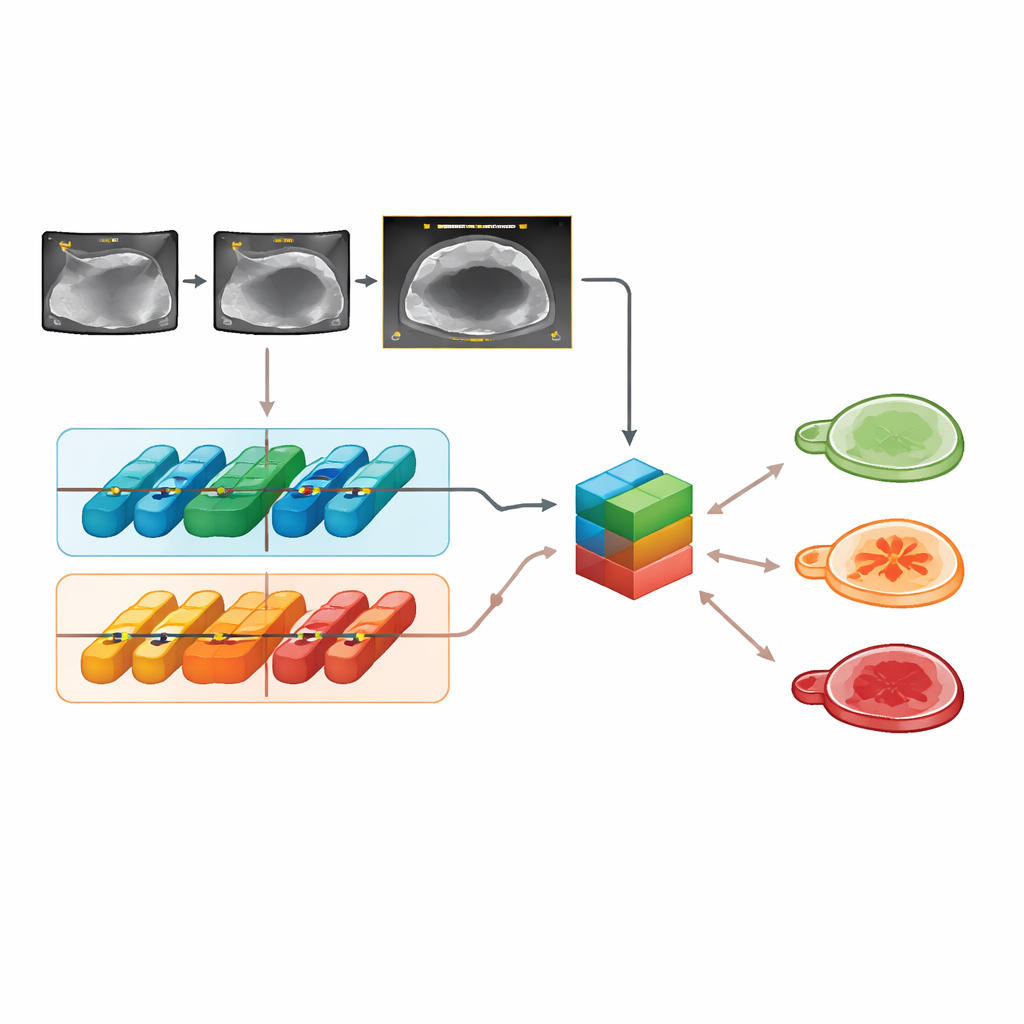
Hjälper mindre erfarna läkare — och dess begränsningar
Forskarna bad därefter 11 radiologer—juniorer, medelnivå och mycket erfarna—att klassificera samma fall, först utan hjälp och sedan med AI:ns resultat och värmekartor som markerar de bildregioner modellen anser viktiga. Med Clinical‑OMTA:s hjälp ökade juniorernas noggrannhet med cirka 18–20 procentenheter, och även de medelnivåläkare förbättrades markant och nådde nästan expertprestation. Överensstämmelsen mellan läsare, som tidigare varierat från endast måttlig till relativt god, steg till mycket höga nivåer när de använde verktyget. Samtidigt noterar studien att sådan stark konvergens kan återspegla "automationsbias", där kliniker förlitar sig för mycket på AI, särskilt i de mest tvetydiga gränsfalliga fallen. Författarna understryker därför att värmekartor är forskningsverktyg, inte fristående förklaringar, och att AI‑vägledning måste integreras omsorgsfullt i klinisk utbildning och beslutsfattande.
Vad detta betyder för patienter
Sammanfattningsvis visar Clinical‑OMTA att ett AI‑system tränat på mångsidig ultraljudsdata kan matcha expertprestation i att klassificera adnexala tumörer som benigna, gränsfalliga eller maligna, samtidigt som det avsevärt förbättrar färdigheter och konsekvens hos mindre erfarna radiologer. Eftersom det fungerar över olika apparater och center kan modellen så småningom implementeras i skannrar eller användas som fristående programvara för att stödja läkare i upptagna eller resursbegränsade kliniker. Författarna varnar att ytterligare prospektiva och internationella studier behövs innan rutinmässig användning, särskilt i miljöer med enklare utrustning eller icke‑specialistoperatörer. Ändå pekar deras arbete mot en framtid där fler kvinnor, oberoende av var de vårdas, kan få fördel av expertlik tolkning av ovarieultraljud och mer skräddarsydd, snabb vård.
Citering: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
Nyckelord: ovarialt ultraljud, artificiell intelligens, adnexala tumörer, gränsfalliga ovarietumörer, kliniskt beslutsstöd