Clear Sky Science · sv
ACACA reglerar R-loop-homeostas för att förbättra lipidmetabolism och mikro-miljöinteraktioner i ccRCC
Varför denna njurcancerberättelse är viktig
Clear cell‑njurcancer är beryktad för att både vara vanlig och svårbehandlad när den sprider sig. Ett kännetecken är att tumörceller blir ovanligt fettrika, lagrar lipider och ändrar hur de skaffar energi. Den här studien ställer en överraskande fråga: hur hänger förändringar i cellens genetiska stressignaler ihop med denna oljiga omställning och med hur tumörer kommunicerar med sin omgivning? Genom att följa ett enda enzym, ACACA, avslöjar forskarna en molekylär koppling mellan genomet i stress, förändrad fettmetabolism och den tillväxtvänliga miljö som byggs upp runt njurtumörer.
Dold tresträngad knut i tumör-DNA
I våra celler kan DNA och RNA tillfälligt bilda tresträngade knutar, så kallade R-loopar, under genläsning. I måttliga mängder hjälper dessa strukturer till att reglera genomet, men i överflöd kan de hindra DNA-kopiering och utlösa skador. Med hjälp av stora offentliga dataset med njurtumörer och frisk vävnad byggde teamet en poäng som speglar hur aktiva R-loop‑relaterade gener är hos varje patient. De fann att denna aktivitet är tydligt högre i clear cell‑njurcancer än i normal njurvävnad och ökar ytterligare i avancerade tumörer och de som spridit sig. Patienter vars tumörer visade starkare R-loop‑signaturer hade i regel sämre överlevnad, vilket tyder på att störd kontroll av dessa strukturer går hand i hand med mer aggressiv sjukdom.
Ett enskilt enzym står ut
Av mer än tusen R-loop‑associerade gener smalnade forskarna ned fältet till 44 som både var felreglerade i tumörer och kopplade till patientutfall. De använde flera linjära maskininlärningsmodeller för att se vilken kombination som bäst förutsade överlevnad. I olika metoder och oberoende patientkohorter steg en gen fram konsekvent: ACACA, ett nyckelenzym som driver det första engagerande steget i nybildning av fettsyror. Höga ACACA‑nivåer hjälpte till att identifiera patienter med högre risk för återfall eller död. När teamet kombinerade ACACA‑uttryck med standardklinisk information — tumörstorlek, spridning och mikroskopisk grad — kunde de bygga ett praktiskt poängverktyg som motsvarade faktisk patientöverlevnad över många år.
En fettrik navpunkt i maligna celler
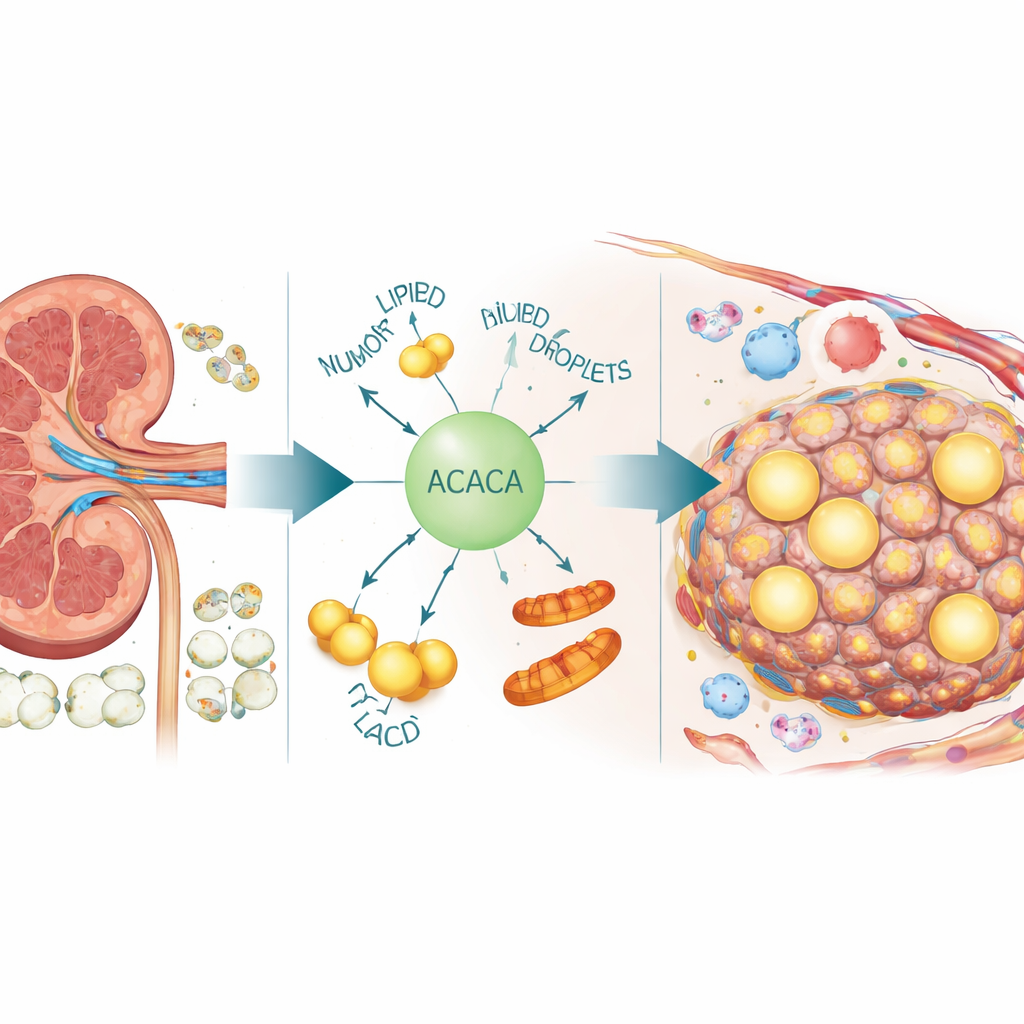
För att se var ACACA placerar sig i tumörekosystemet använde författarna single‑cell och spatial transkriptomik, tekniker som läser genaktivitet cell för cell och kartlägger den tillbaka på vävnadsskivor. Dessa analyser visade att ACACA inte uttrycks jämnt: det koncentreras i maligna celler, där det sammanfaller med aktiva celldelningsprogram och tecken på DNA‑skada och reparation. ACACA‑rika cancerceller framstod som kommunikationsnav, som skickar och tar emot många signaler från närliggande immunceller och blodkärlsceller. Många av dessa signaler går via lipidrelaterade vägar som involverar ANGPTL‑molekyler, kända för att samordna hantering av fett med inflammation och blodkärlsbildning. I vävnadsnitt överlappade ACACA‑rika regioner med täta tumörområden snarare än med omgivande normal vävnad.
Från genetisk stress till bränsleförsörjning och tumörtillväxt
Författarna testade därefter ACACA direkt i njurcancercellinjer och i musmodeller. Nedreglering av ACACA bromsade celltillväxt, minskade rörlighet och ökade celldöd, medan uppreglering gav motsatt effekt. Mikroskopi visade att låg ACACA ledde till ansamling av R‑loopar och fler tecken på DNA‑skada, medan hög ACACA minskade dessa strukturer. Samtidigt ökade ACACA antalet lipidkärnor i cellerna, höjde nivåerna av fettsyror och triglycerider och förbättrade mitokondriernas hälsa, bedömt genom starkare membranpotential, fler mitokondrier och lägre nivåer av reaktiva syrearter. Hos möss begränsade blockad av ACACA i implanterade njurcancerceller tumörtillväxten, ökade signaler för DNA‑skada, minskade lipidförråd och försvagade mitokondriell funktion — vilket knyter enzymet till både genomstabilitet och tumörens energibudget.
Vad detta betyder för framtida behandling
Sammantaget framställer studien ACACA som en molekylär strömbrytare som hjälper clear cell‑njurcancer att överleva under genetisk stress genom att omforma fettmetabolismen och stärka interaktionerna med omgivande mikromiljö. Förhöjd R‑loop‑aktivitet markerar farligare tumörer, och ACACA framträder som en central spelare som kopplar denna stress till lipid‑rika, energieffektiva cancerceller som växer och sprider sig lättare. Eftersom ACACA är ett enzym som i princip kan riktas av läkemedel, pekar dessa fynd på nya sätt att både förutsäga vilka patienter som löper störst risk och att utforma behandlingar som samtidigt stör tumörens genombeskyddande strategier och dess metaboliska livlinor.
Citering: Zhang, D., Chen, X., He, X. et al. ACACA modulates R-loop homeostasis to enhance lipid metabolism and microenvironmental interactions in ccRCC. npj Precis. Onc. 10, 102 (2026). https://doi.org/10.1038/s41698-026-01319-y
Nyckelord: clear cell renal cell carcinoma, R-loopar, ACACA, lipidmetabolism, tumörmikromiljö