Clear Sky Science · sv
Nästa lager: förstärkning av grundmodeller med strukturbevarande och uppmärksamhetsstyrd inlärning för medvetenhet om lokala fält till global kontext i beräkningspatologi
Lära datorer att läsa cancerpreparat
När en patolog undersöker ett cancerbiopsi under mikroskopet tittar hen inte bara på enskilda celler—hen ser mönster, grannskap och hur tumör-, immunceller och normalt vävnad är arrangerade tillsammans. Dagens artificiella intelligenssystem för digital patologi är mycket bra på att upptäcka detaljer i små bildfönster, men de missar ofta den större helheten. Denna studie introducerar EAGLE-Net, en ny AI-metod som hjälper datorer att se cancerpreparat mer som mänskliga experter genom att uppmärksamma både lokala detaljer och vävnadens övergripande uppläggning på preparatet.

Varför tumörvävnadens uppläggning är viktig
En tumör är mer än en samling cancerceller. Den lever i ett komplext grannskap fyllt av blodkärl, immunceller, bindväv och områden med ärrbildning eller celldöd. Hur dessa element är ordnade—deras avstånd, gränser och blandningar—kan ge signaler om hur aggressiv cancern är och hur en patient kan svara på behandling. Konventionella AI-system i patologi delar vanligen en helbild i tusentals små rutor och analyserar dem nästan isolerat. De försöker sedan skatta patientens diagnos eller utfall genom att poola information från alla rutor. Denna strategi ignorerar ofta hur rutorna förhåller sig till varandra i rummet, vilket kan försvaga prediktioner och göra AI-värmekartor spridda eller svåra att tolka.
Ett nytt sätt att fånga den större bilden
EAGLE-Net är utformat för att överbrygga klyftan mellan lokal detalj och global struktur. Det utgår från kraftfulla ”grundmodeller” som redan kan extrahera rika visuella drag från små preparatfönster. Ovanpå detta lägger det till en modul som kodar var varje fönster kommer ifrån på preparatet, och bevarar den verkliga geometrin i vävnaden i stället för att pressa in den i ett förvrängt rutnät. Med hjälp av flerskaliga filter lär sig EAGLE-Net mönster som spänner från små cellulära förändringar till bredare vävnadsstrukturer såsom tumörgränser och omgivande stroma. Därefter använder det en uppmärksamhetsmekanism—i praktiken ett sätt att tilldela betydelsescore—för att fokusera på fönster och grannskap som är mest relevanta för att förutsäga diagnos eller överlevnad.
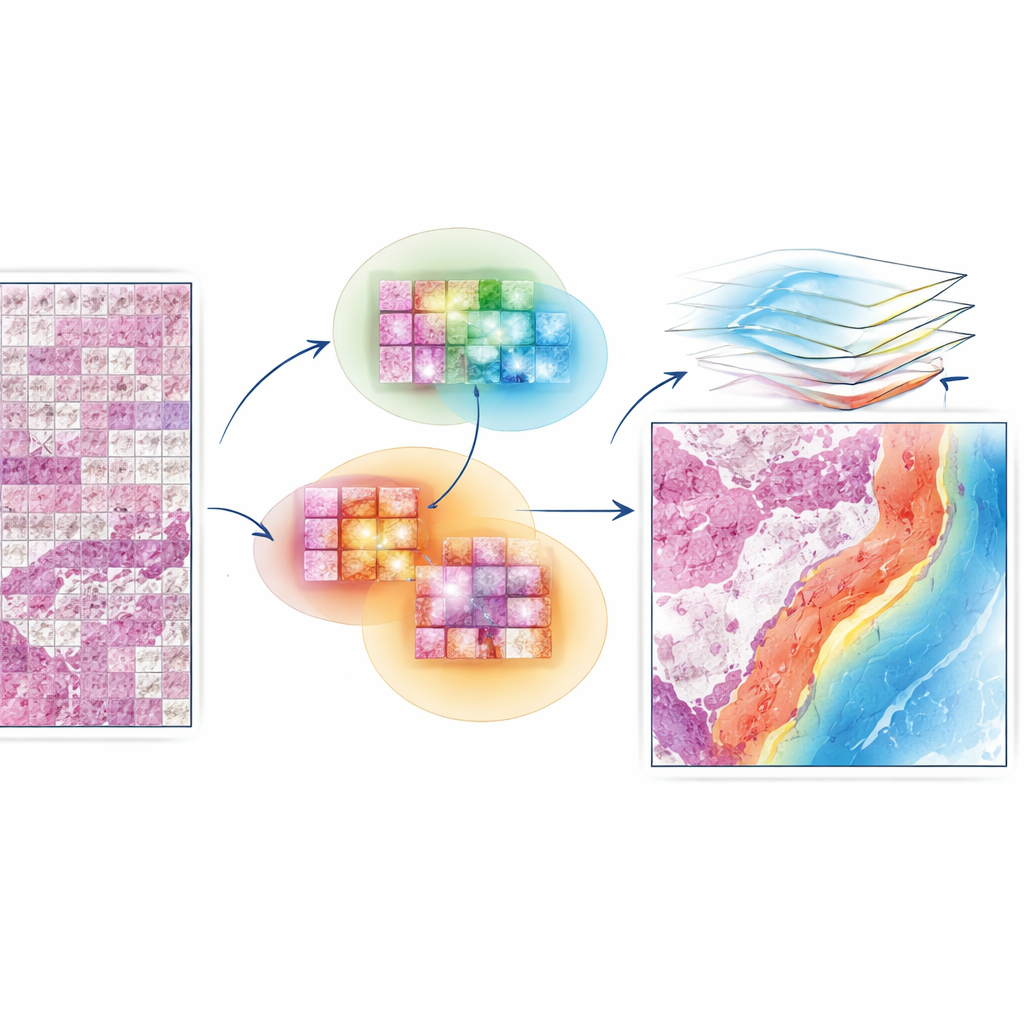
Låta modellen lära från grannskap, inte bara punkter
En central innovation i EAGLE-Net är hur den lär nätverket att värdera inte bara de viktigaste rutorna utan också deras närliggande grannar. Under träning identifierar metoden upprepade gånger de rutor som modellen finner mest informativa och uppmuntrar den sedan att betrakta omgivande rutor inom en liten radie som en del av samma meningsfulla region. Denna ”grannskapsmedvetna” inlärning puttar modellen mot att forma släta, sammanhängande uppmärksamhetsregioner som stämmer överens med hur patologer ser tumörkanter, immunkluster och andra mikromiljöer. Samtidigt innehåller träningsprocessen en extra term som aktivt driver modellen att ignorera bakgrund eller tomma områden, vilket minskar risken för falska markeringar på artefakter eller vita ytor.
Bevisa sitt värde över många cancertyper
Forskarna testade EAGLE-Net på nästan 15 000 helbildspreparat som täckte 10 olika cancerformer, inklusive lung-, njure-, magsäck-, livmoder-, sköldkörtel-, kolorektal- och prostata-tumörer. De utvärderade två huvudsakliga uppgifter: att förutsäga hur länge patienter skulle överleva och att klassificera tumörtyper eller grader. I de flesta cancerkohorter matchade eller överträffade EAGLE-Net flera ledande uppmärksamhetsbaserade metoder och förbättrade ofta överlevnadsprognospoäng och klassificeringsnoggrannhet med några procentenheter, vilket är betydelsefullt i populationsstudier. Det presterade också starkt när det kombinerades med tre mycket olika underliggande grundmodeller, vilket visar att dess design är flexibel och inte knuten till en enda dra-konstruktör.
Se in i modellens resonemang
Bortom ren noggrannhet granskade teamet noggrant var EAGLE-Net ”tittade” på preparaten. Jämfört med andra metoder bildade dess uppmärksamhetskartor slätare, mer sammanhängande regioner som följde tumörgränser och fångade invasiva kanter, nekrotiska fickor och immuncellskluster. Kvantitativa jämförelser med expertritade tumörmasker visade att EAGLE-Nets markerade regioner överlappade bättre med den verkliga tumören, gjorde färre falska träffar på normal vävnad och återgav mer troget komplexa tumörformer. Modellen ägnade också en större andel av sin uppmärksamhet åt tumör-, nekros- och immunkompartiment, och mindre åt normal lungvävnad eller blodkärl, vilket speglar vad en patolog skulle prioritera vid bedömning av prognos.
Vad detta innebär för framtida cancervård
I praktiska termer visar EAGLE-Net att tillägg av rumslig medvetenhet och grannskapsresonemang ovanpå befintlig patologi-AI kan förbättra både prestanda och tolkbarhet. I stället för att behandla ett preparat som en påse med oberoende rutor lär sig metoden att känna igen biologiskt meningsfulla nischer—tumörkanter, immurrika regioner och invasionsmönster—som har betydelse för patientutfall. Eftersom den fungerar med många olika grundmodeller och inte kräver arbetskrävande pixelnivåannoteringar kan EAGLE-Net tillämpas brett på stora arkiv av digitala preparat. Med ytterligare validering och integrering i kliniska arbetsflöden kan sådana system hjälpa patologer att stratifiera patienter mer precist, upptäcka nya vävnadsbaserade biomarkörer och i slutändan vägleda mer skräddarsydda cancerbehandlingar.
Citering: Waqas, M., Bandyopadhyay, R., Showkatian, E. et al. The next layer: augmenting foundation models with structure-preserving and attention-guided learning for local patches to global context awareness in computational pathology. npj Precis. Onc. 10, 109 (2026). https://doi.org/10.1038/s41698-026-01312-5
Nyckelord: beräkningspatologi, cancerprognos, digital patologi AI, tumörmikromiljö, EAGLE-Net