Clear Sky Science · sv
Storskalig encellsanalys och in silico-perturbation avslöjar HCC:s dynamiska utveckling: från initiering till terapeutisk inriktning
Varför levercancerens inre liv spelar roll
Hepatocellulärt karcinom, den vanligaste formen av levercancer, är notoriskt svår att behandla. Många patienter svarar dåligt på dagens läkemedel, och tumörer återkommer eller sprider sig ofta. En viktig orsak är att varje tumör är en kaotisk blandning av olika celler som utvecklas över tid och ständigt kommunicerar med sin omgivning. Denna studie använder kraftfulla encells- och rumsliga genavläsningstekniker för att följa den utvecklingen, cell för cell, från tidig tumörtillväxt till avancerad, behandlingsresistent sjukdom, och för att identifiera svaga punkter som nya terapier kan utnyttja.
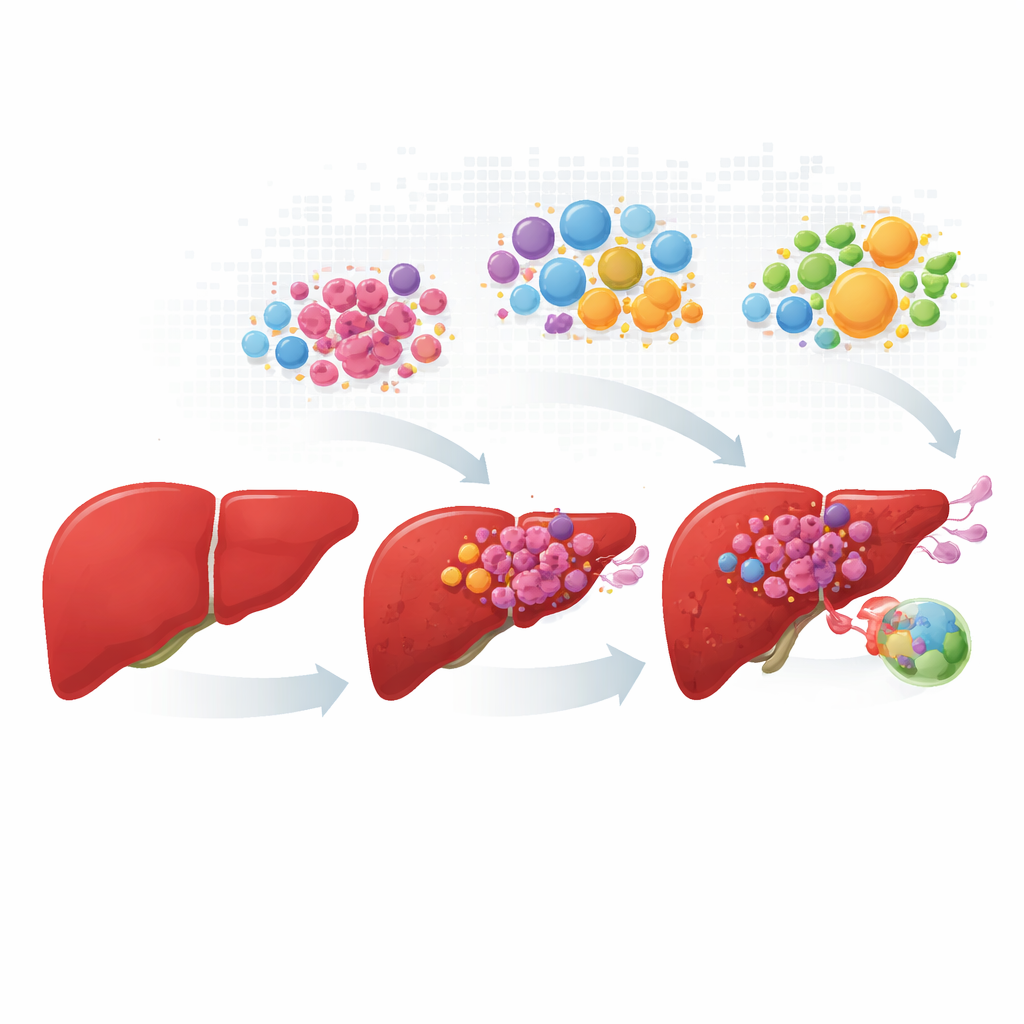
Följa cancerceller från tidig förändring till spridning
Forskarna samlade och harmoniserade data från mer än hundra patienter, och täckte normal levervävnad, primära tumörer, tillväxt i blodkärl och lymfkörtelmetastaser. Istället för att betrakta varje tumör som en homogen massa profilerade de hundratusentals enskilda celler och kartlade sedan var dessa celler sitter i faktiska vävnadsskivor. Cancerösa leverceller delade in sig i fyra återkommande ”personligheter”. En grupp behöll många normala leverfunktioner och metabola uppgifter; de övriga tre visade stressdriven tillväxt, hög aktivitet i MYC-växtvägen eller invasivt, inflammation-bundet beteende. Dessa fyra tillstånd förekom i olika proportioner när sjukdomen fortskred, där snabbväxande och invasiva celler dominerade i kärl- och lymfkörtellesioner.
Fyra tumörpersonligheter med olika prognos
De fyra cancercellstillstånden var inte bara teoretiska kategorier; de korrelerade med patienternas utfall. Tumörer rika på det leverliknande, metabolt aktiva tillståndet kopplades till bättre överlevnad, medan tumörer dominerade av de tre aggressiva tillstånden tenderade att ge sämre resultat. Även det ”goda” tillståndet hade dock en baksida: det var starkt överrepresenterat hos patienter som inte drog nytta av levercancermedicinen sorafenib, troligen eftersom dessa celler bevarar avgiftningsmaskineri som kan inaktivera läkemedel. Genom att återskapa hur celler rör sig längs utvecklingsbanor visade teamet att invasiva, inflammatoriska celler kan grenra sig mot mer differentierade eller mer högt proliferativa tillstånd, vilket tyder på att tumörceller kan byta identitet och potentiellt undkomma terapier riktade mot ett enda tillstånd.
Medhjälparna: immunceller och stromala kompanjoner
Cancerceller agerar inte ensamma. Studien avslöjade specialiserade immunceller och stödjeceller som antingen bekämpar tumörer eller tyst hjälper dem. Bland makrofagerna, vävnadens sop- och vaktsoldater, producerade vissa typer inflammatoriska signaler som kan stödja anti-tumörimmunitet, medan andra var metabolt omprogrammerade, undertryckte hjälpsamma signaler och främjade blodkärlsbildning och invasion. Dessa ”skurkmakrofager” expanderade i avancerade prov. Likaså bildade vissa endotelceller som bekläder blodkärl och fibroblaster som bygger bindväv distinkta undergrupper kopplade till dålig prognos. I avancerad sjukdom skapade en särskild endotelial undergrupp och två fibroblasttyper tätt sammankopplade nav som omformade den extracellulära matrisen, drev ny kärlbildning och korrelerade med de mest aggressiva cancercellstillstånden.
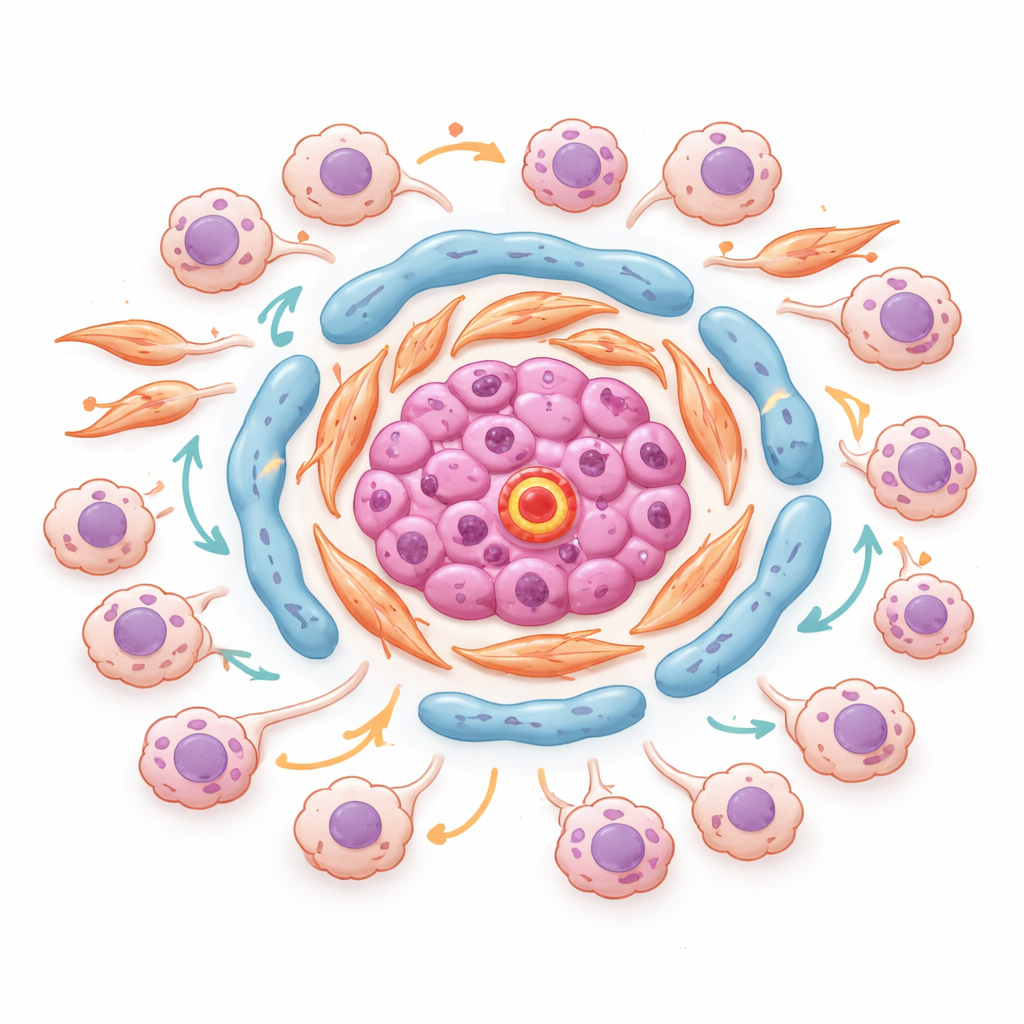
Se farliga grannskap inne i tumörer
Med rumslig transkriptomik, som mäter genaktivitet utan att förlora kartan över var varje punkt sitter i vävnaden, identifierade författarna organiserade ”grannskap” inne i tumörer. I en representativ tumör klustrade endotelceller rika på ett molekylärt markörprotein kallat ESM1 med lipid- och matrisproducerande fibroblaster i kärnan av stromala öar. Runt dessa kärnor samlades stressdrivna och invasiva cancerceller i regioner med stark TGF-beta- och lågt syresignalering. Nyckeltranskriptionsfaktorer som styr hur celler svarar på stress och inflammation delades mellan dessa cancer-tillstånd och var som mest aktiva precis där tumörcellerna mötte dessa stromala nav. Detta tyder på att specifika mikronischer vid tumör–stroma-gränser aktivt uppmuntrar cancerceller att ändra tillstånd, bli mer aggressiva och motstå terapi.
Hitta en gemensam svag punkt för nya behandlingar
För att gå från beskrivning till intervention använde teamet en maskininlärningsmodell tränad på miljontals celler för att simulera ”virtuella knockouts” av gener och förutsäga vilka förändringar som kunde skifta skadliga celler mot friskare tillstånd. Genom att jämföra makrofager, endotelceller och cancerceller fann de en liten uppsättning gener vars borttagande hjälpte till att normalisera alla tre. Bland dessa stack HSP90B1 ut: cancercellinjer är starkt beroende av den, den överproduceras i levertumörer, särskilt i dem som är resistenta mot riktade läkemedel och immunterapi, och höga nivåer förutsäger sämre överlevnad. HSP90B1 kodar för en stresshanterande chaperon i cellens proteinvikningsmaskineri som stödjer många ytreceptorer och signalvägar. Eftersom selektiva läkemedel mot denna chaperon redan finns och dessutom kan omforma den immuna miljön, föreslår studien HSP90B1 som ett lovande mål för att övervinna resistens, särskilt i kombination med befintliga levercancerbehandlingar.
Vad detta betyder för patienter och behandlingar
Tillsammans visar arbetet att levercancer inte är en enda sjukdom utan ett dynamiskt ekosystem av celltillstånd och nischer som skiftar när tumören växer och sprider sig. Genom att knyta specifika cancercellspersonligheter, stödjeceller och rumsliga grannskap till patientutfall och läkemedelssvar erbjuder studien en färdplan för mer precisa behandlingar: matcha terapier till dominerande celltillstånd, störa stromala nav som odlar aggressivt beteende, och rikta gemensamma beroenden som HSP90B1 som många tumör- och mikromiljőceller är beroende av. Även om ytterligare laboratorie- och klinisk testning krävs, ger atlasen som teamet byggt en detaljerad blueprint för att vända tumörens interna komplexitet från ett hinder till en möjlighet för smartare, mer hållbara levercancerterapier.
Citering: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Nyckelord: hepatocellulärt karcinom, encellsanalys, tumörmikromiljö, rumslig transkriptomik, HSP90B1