Clear Sky Science · sv
Översättning av rumsliga transkriptomiska signaturer i adenoskvamöst karcinom till prognostiska bulkmarkörer i lungadenocarcinom: en bottom-up-strategi
Dolda varningssignaler inuti lungtumörer
Lungcancer är fortfarande en av de mest dödliga cancerformerna, delvis eftersom tumörer är blandningar av många olika celltyper. Vissa av dessa celler kan tyst driva sjukdomen mot ett mer aggressivt förlopp eller motstå behandling, men de är för få eller för insmälta för att upptäckas med standardtester. Denna studie visar hur ultradetljerade "kartor" över genaktivitet i tumörer kan avslöja dessa dolda bovar och omvandla dem till enkla laboratoriemarkörer som hjälper till att förutsäga hur patienter med lungcancer kommer att klara sig.
Närmare granskning av en sällsynt, blandad tumör
Forskarna fokuserade på en sällsynt lungcancer som kallas adenoskvamöst karcinom, vilken kombinerar två huvudtyper av icke–småcellig lungcancer i samma massa: körtelliknande adenocarcinom och platt, hudliknande skivepitelkarcinom. Eftersom båda komponenterna växer sida vid sida i samma tumör är denna cancer en ideal modell för att studera hur tumörceller kan skifta från en identitet till en annan när de blir mer maligna. Med en avbildningsmetod kallad rumslig transkriptomik mätte teamet vilka gener som var aktiva i tusentals enskilda celler samtidigt som deras exakta positioner i tunna tumörsnitt bevarades. Samtidigt använde de standardfärgningar för två vanliga diagnostiska markörer, TTF‑1 (för adenocarcinom) och p40 (för skivepitelceller), för att förankra sina högteknologiska kartor i rutindiagnostik. 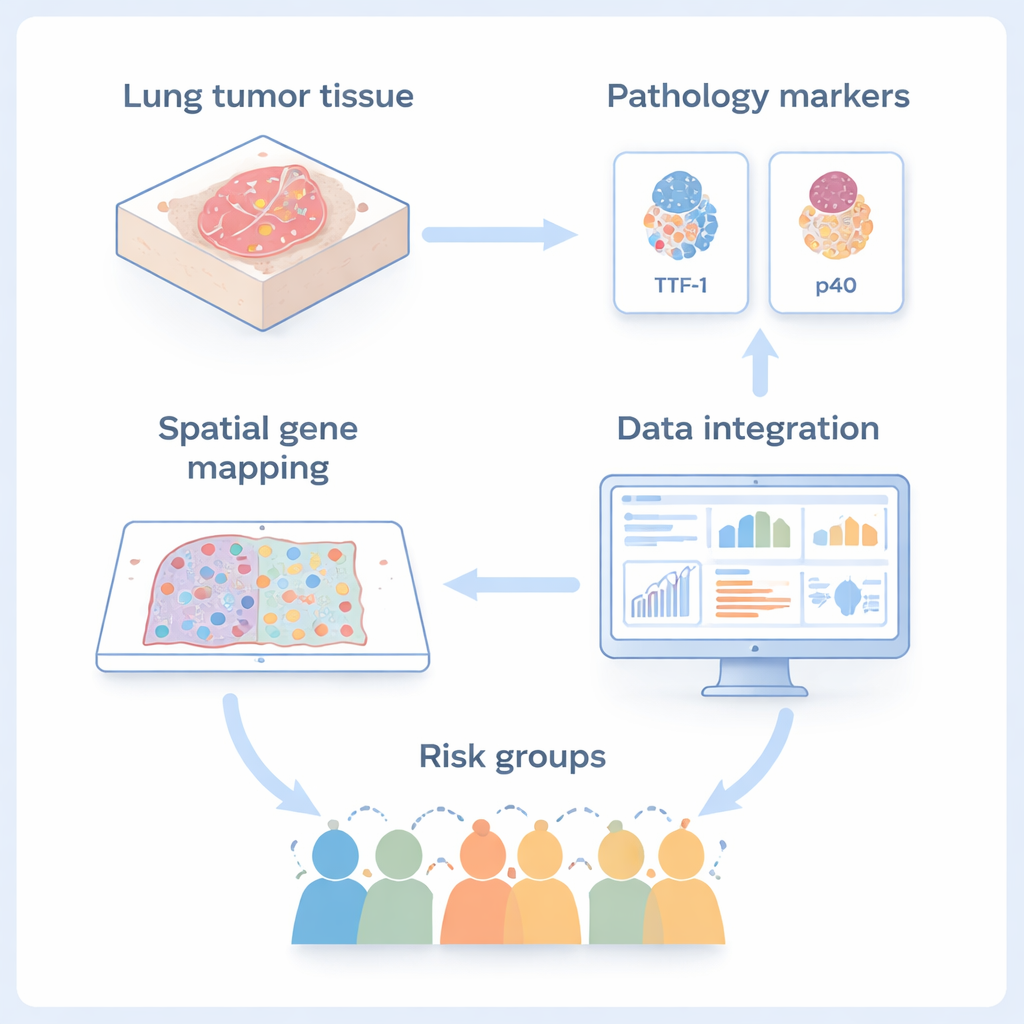
Färgkoda tumörceller för att hitta de avvikande
Bara att gruppera celler efter deras genmönster räckte inte, eftersom normala lungceller och tumörceller ibland kan se likadana ut i genutläsningar. För att skärpa bilden använde teamet en visualiseringstrick de kallar RGB‑UMAP. I denna metod komprimeras varje cells övergripande genaktivitetsmönster till tre tal som översätts till en röd‑grön‑blå färg. Celler som beter sig likadant framträder i liknande färger när de projiceras tillbaka på vävnadsbilden. Detta gjorde det möjligt för forskarna att upptäcka fickor av normala celler som gömde sig bland tumörceller och ta bort dem från analysen, så att de säkerställde att de studerade verkliga cancerceller snarare än friska medvandrare.
Hittade ett hybridtillstånd och en viktig sockelucka
Efter att ha filtrerat bort normala celler sökte forskarna efter gener som var starkt och konsekvent aktiva endast i tumörceller. Bland dessa upptäckte de en grupp tumörceller som var negativa för både TTF‑1 och p40 men ändå visade ett blandat genmönster, med egenskaper från både adenocarcinom och skivepitelkarcinom. En gen stod ut i denna hybridgrupp: SLC2A1, som kodar för proteinet känt som GLUT1. GLUT1 fungerar som en port som släpper in glukos, cellens bränsle, från blodomloppet. I flera tumörer var SLC2A1 rikligt förekommande i skivepitelområden och i de TTF‑1/p40‑negativa zonerna, men nästan frånvarande i normal lungvävnad. Teamet bekräftade detta mönster i flera patientprover, vilket tyder på att hög SLC2A1 markerar en skivepitel‑lik, metabolt aktiv subpopulation av cancerceller.
Från mikroskopiska kartor till patientutfall
För att undersöka om denna mikroskopiska iakttagelse har betydelse för verkliga patienter vände forskarna sig till stora befintliga datamängder där bulkgenaktivitet (genomsnitt över hela tumörprov), DNA‑förändringar och kliniska utfall fanns tillgängliga för hundratals personer med lungadenocarcinom. När de grupperade dessa patienter efter SLC2A1‑nivåer i deras tumörer, hade de med högre SLC2A1 fler genförändringar som typiskt ses i skivepitelcancer, en starkare signatur för sockerhungrig metabolism och signifikant sämre överlevnad. Denna koppling höll i sig även efter hänsynstagande till faktorer som ålder, stadium, rökvanor och kön, och bekräftades i en oberoende offentlig datamängd. I kontrast till detta skilde sig inte patienter med rena skivepitelstumörer tydligt efter SLC2A1‑nivåer, vilket understryker att markören är särskilt informativ inom adenocarcinom.
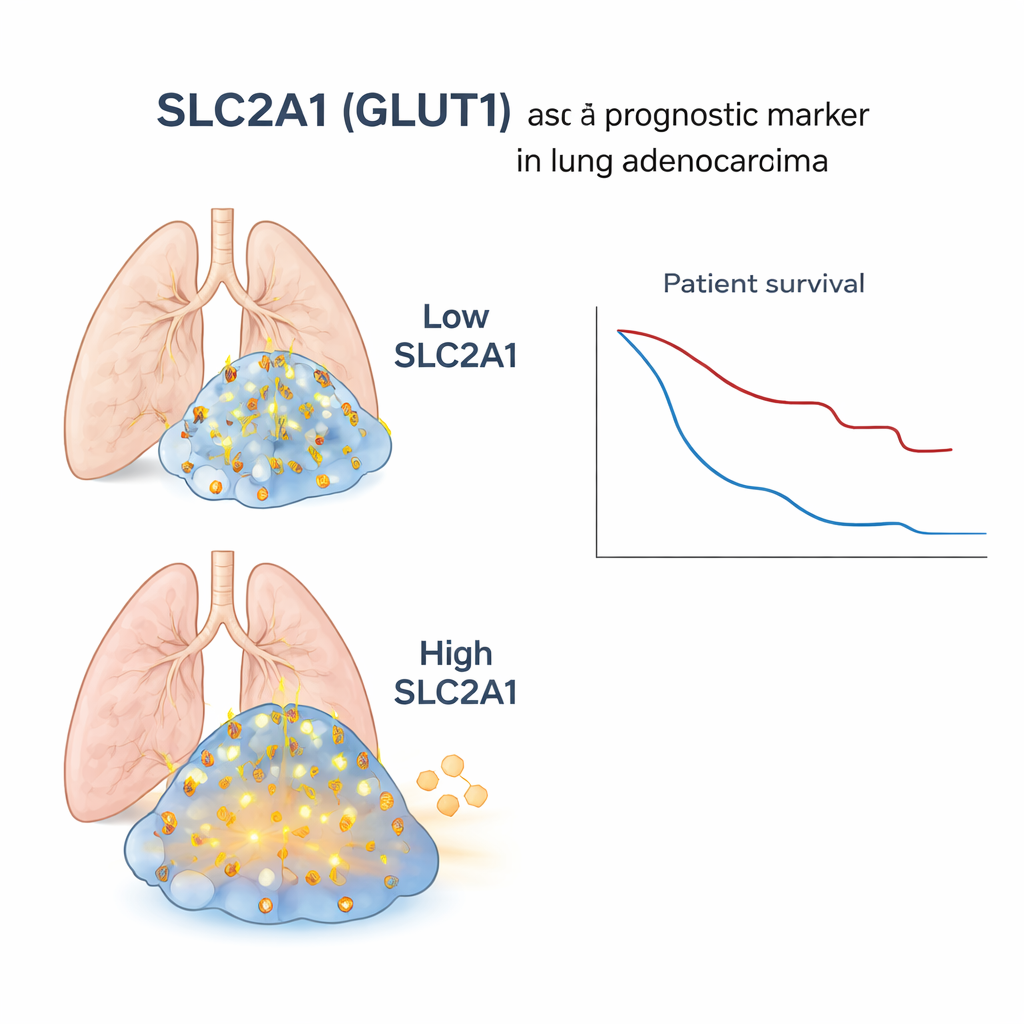
Vad detta betyder för patienter med lungadenocarcinom
För icke‑specialister är huvudbudskapet att inom det som vid mikroskopisk granskning ser ut som en enda typ av lungcancer kan det finnas dolda fickor av celler som beter sig mer som en annan, mer aggressiv typ. Genom att använda högupplöst genkartläggning identifierade forskarna SLC2A1 som en enkel, mätbar signal för dessa skivepitel‑lika, bränslehungriga celler som lurar inne i adenocarcinom. Höga nivåer av denna gen i rutinprovsnitt flaggar patienter vars tumörer med större sannolikhet uppträder aggressivt och som kan behöva tätare uppföljning eller annorlunda behandlingsstrategier. Mer generellt visar studien en "bottom‑up"‑väg — från enskilda celler i ett vävnadssnitt till tester på hela tumören — som kan tillämpas på andra cancerformer för att avslöja farliga celltillstånd som rutinmetoder i dag missar.
Citering: Hatakeyama, K., Kawata, T., Muramatsu, K. et al. Translating spatial transcriptomic signatures in adenosquamous carcinoma into bulk prognostic biomarkers in lung adenocarcinoma: a bottom-up approach. npj Precis. Onc. 10, 77 (2026). https://doi.org/10.1038/s41698-026-01297-1
Nyckelord: lungadenocarcinom, rumslig transkriptomik, adenoskvamöst karcinom, SLC2A1 GLUT1, cancermarkörer