Clear Sky Science · sv
Förlust av mikroRNA-29b främjar DNMT3b-medierad nedreglering av STING och dämpar strålbehandlingsinducerad antitumörimmunitet i KRAS-mutant kolorektal cancer
Varför denna forskning är viktig
För många personer med ändtarms- och tjocktarmscancer är strålbehandling en central del av behandlingen före operation. Ändå krymper vissa tumörer knappt, och cancer återkommer eller sprider sig ofta. Denna studie granskar en vanlig genetisk förändring i kolorektal cancer — en KRAS-mutation — för att förklara varför dessa tumörer ofta står emot strålning och nya immunoterapier, och föreslår en strategi för att återaktivera kroppens eget immunsystem mot dem.
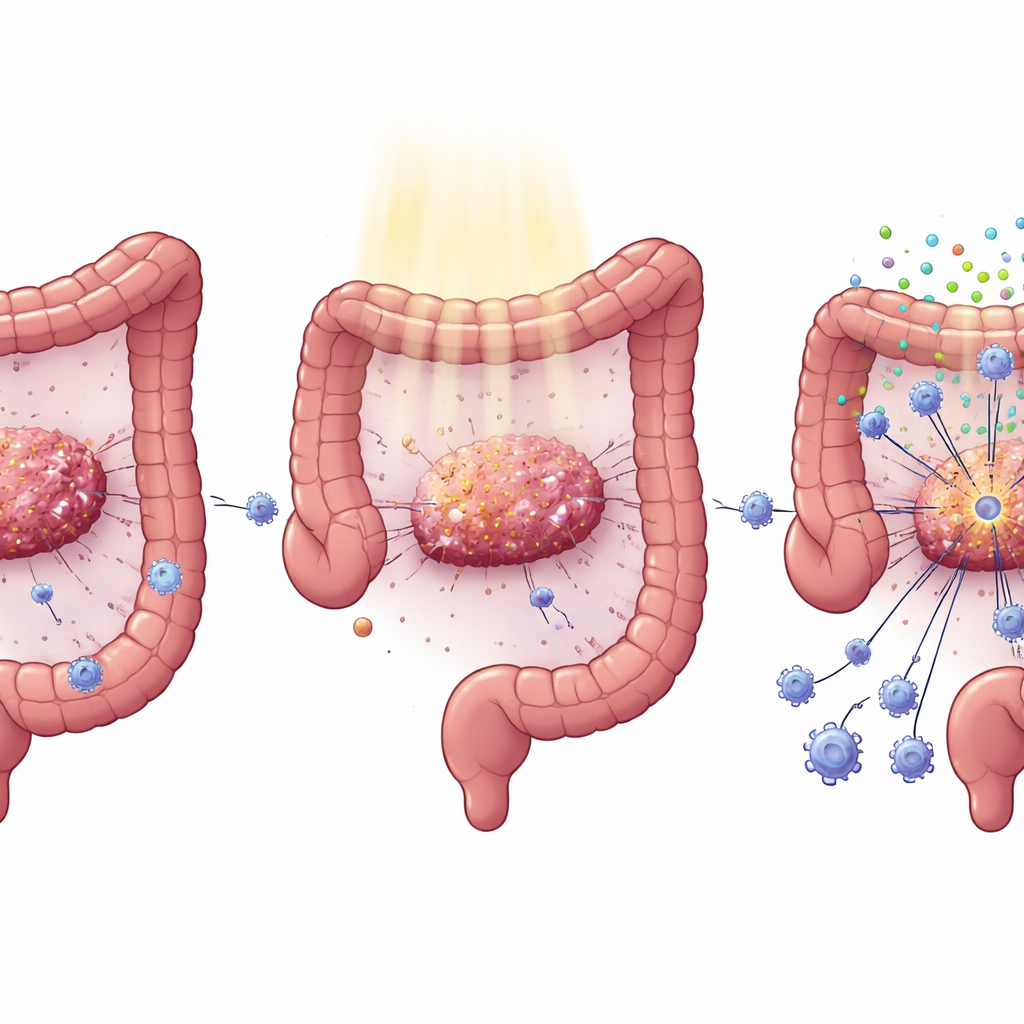
En vanlig mutation som döljer tumörer från immunangrepp
Kolorektal cancer bär ofta mutationer i KRAS-genen, en huvuddrivare för tumörtillväxt och spridning. Kliniker hade redan noterat att KRAS-mutanta tumörer ofta svarar dåligt på både riktade läkemedel och strålbehandling. Genom att gräva i stora cancerregister och undersöka patientprover fann författarna att tumörer med mutant KRAS uppvisar färre CD8‑T‑celler som dödar cancer och svagare aktivitet i interferon‑drivna immunstärkande signaler. Hos patienter som fått standard kemoradioterapi före operation för rektalcancer ökade antalet CD8‑T‑celler inne i tumörerna betydligt mer hos dem med vildtyp KRAS än hos dem med KRAS‑mutation, vilket hjälper till att förklara deras bättre utfall.
Det saknade larmsystemet inne i cancercellerna
Strålbehandling skadar inte bara tumörens DNA; den kan också fungera som en signal som får cancerceller att släppa ut DNA‑fragment som aktiverar en intern larmsignalväg kallad cGAS–STING. När STING är aktiv producerar cellerna typ I‑interferoner och andra signaler som lockar till sig och aktiverar immunceller, inklusive T‑celler och dendritiska celler. Forskarna visade att i kolorektala cancerceller som konstruerats att bära mutant KRAS är detta larmsystem dämpat: efter strålning producerade dessa celler mycket mindre interferon och relaterade molekyler. I möss återställde tystande av KRAS i tumörer STING‑nivåerna, förstärkte interferon‑signaler och ledde till fler CD4‑ och CD8‑T‑celler, färre regulatoriska T‑celler och bättre tumörkontroll — inte bara i bestrålade tumörer utan också i avlägsna, icke‑bestrålade ”abscopala” tumörer.
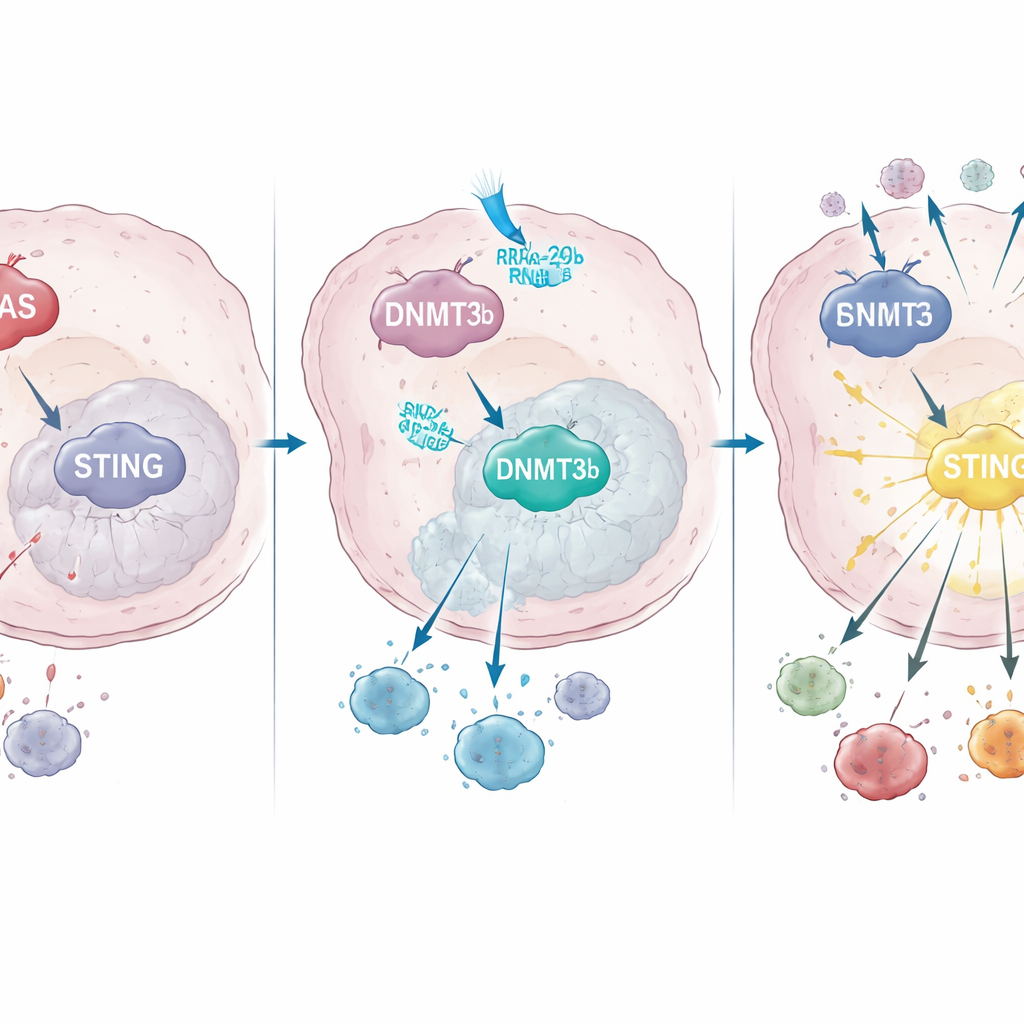
Hur KRAS omkopplar genreglering för att stänga ner STING
Vid djupare studier upptäckte teamet att mutant KRAS ökar aktiviteten hos ett DNA‑modifierande enzym kallat DNMT3b, som adderar metylgrupper till vissa DNA‑regioner och stänger av närliggande gener. I både cellinjer och patientprover gick hög DNMT3b hand i hand med låg STING. En nyckelregion i STING‑promotorn — DNA:s ”på‑knapp” — var starkt metylerad i KRAS‑mutanta tumörer men inte i tumörer med normal KRAS. Patienter vars tumörer fortfarande kunde uppreglera STING efter kemoradioterapi hade mer infiltration av CD8‑T‑celler och bättre överlevnad, vilket understryker hur viktig denna väg är för framgångsrik behandling.
En liten RNA som kan återväcka larmet
Författarna tog sedan reda på vad som gör DNMT3b så rikligt i KRAS‑mutant cancer. Genom microRNA‑sekvensering identifierade de en liten reglerande RNA, microRNA‑29b‑3p, som normalt håller DNMT3b i schack men som kraftigt undertrycks av mutant KRAS. Att återställa detta microRNA i laboratorieväxande KRAS‑mutanta celler sänkte DNMT3b, återupplivade STING och ökade interferonproduktionen efter strålning; att blockera det hade motsatt effekt. I tumörprover tenderade KRAS‑mutanta patienter att ha låg microRNA‑29b‑3p, hög DNMT3b och låg STING, och de med högre microRNA‑29b‑3p levde längre, vilket knyter denna molekylära kedja direkt till kliniska utfall.
En målinriktad genleveransmetod som stärker strålbehandling och immunterapi
För att översätta dessa fynd till en potentiell behandling konstruerade teamet ett ofarligt virus (AAV) som levererar microRNA‑29b‑3p under kontroll av en promotor som är aktiv främst i kolorektala cancerceller. I musmodeller med KRAS‑mutanta kolorektala tumörer gav denna AAV i kombination med lokaliserad strålning dramatiskt krympande av både bestrålade tumörer och avlägsna tumörer som inte fick strålning. Tumörerna visade lägre DNMT3b, mer STING, ökade interferonsignaler och kraftig infiltration av T‑celler och andra immunceller. När samma microRNA‑29b‑3p‑behandling kombinerades med en immunkontrollpunktshämmare riktad mot PD‑1 förbättrades överlevnaden ytterligare, och denna fördel var beroende av CD8‑T‑celler, vilket bekräftar att immunsystemet gjorde det tyngsta jobbet.
Vad detta kan betyda för patienter
Enkelt uttryckt visar denna studie hur KRAS‑mutant kolorektal cancer ”klipper sladden” till ett internt larmsystem som strålning normalt aktiverar, vilket tillåter tumörerna att undgå immunangrepp. Genom att återställa en enda liten RNA, microRNA‑29b‑3p, kunde forskarna sänka DNMT3b, återväcka STING och göra immunologiskt ”kalla” tumörer till ”heta” tumörer som svarar bättre på både strålbehandling och checkpoint‑blockad. Även om arbetet fortfarande är prekliniskt pekar det mot framtida behandlingar som parar ihop strålning med tumör‑specifik genterapi för att övervinna resistens i KRAS‑mutant kolorektal cancer, och potentiellt göra befintliga behandlingar effektiva för många fler patienter.
Citering: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Nyckelord: KRAS-mutant kolorektal cancer, strålbehandlingsresistens, STING-vägen, microRNA-29b, tumörimmunologi