Clear Sky Science · sv
Jämförande analys av ctDNA-övervakningsstrategier vid avancerad NSCLC med MET exon 14-skipning som behandlats med ensartinib
Varför ett blodprov spelar roll vid lungcancer
För personer med avancerad lungcancer är en av de största frågorna om en ny läkemedelsbehandling faktiskt fungerar — och hur snabbt läkare kan avgöra det. Den här studien undersöker en blodbaserad metod som använder små fragment av tumör-DNA i blodomloppet för att snabbt bedöma hur väl ett riktat läkemedel, ensartinib, hjälper patienter vars tumörer delar en specifik genetisk avvikelse. Resultaten tyder på att ett enkelt tidigt blodprov kan indikera vilka patienter som sannolikt får längre nytta av behandlingen och vilka som kan behöva ändra strategi.
Att föra en tumörs fingeravtryck ner i ett rör
Cancerceller släpper ifrån sig delar av sitt genetiska material i blodet, så kallat cirkulerande tumör-DNA. I den här prövningen fokuserade forskarna på personer med icke-småcellig lungcancer orsakad av en förändring i genen MET, närmare bestämt en defekt som kallas exon 14-skipning. Alla patienter fick ensartinib efter att tidigare behandlingar misslyckats. Blodprover togs precis före behandlingsstart och igen efter fyra veckor. Med hjälp av ett avancerat sekvenseringstest som skannar 229 cancerrelaterade gener kategoriserade teamet de påvisade förändringarna i tre grupper: förändringar i MET själv, en uppsättning väletablerade cancerdrivande förändringar, och en bred fångstgrupp av alla påvisbara mutationer.
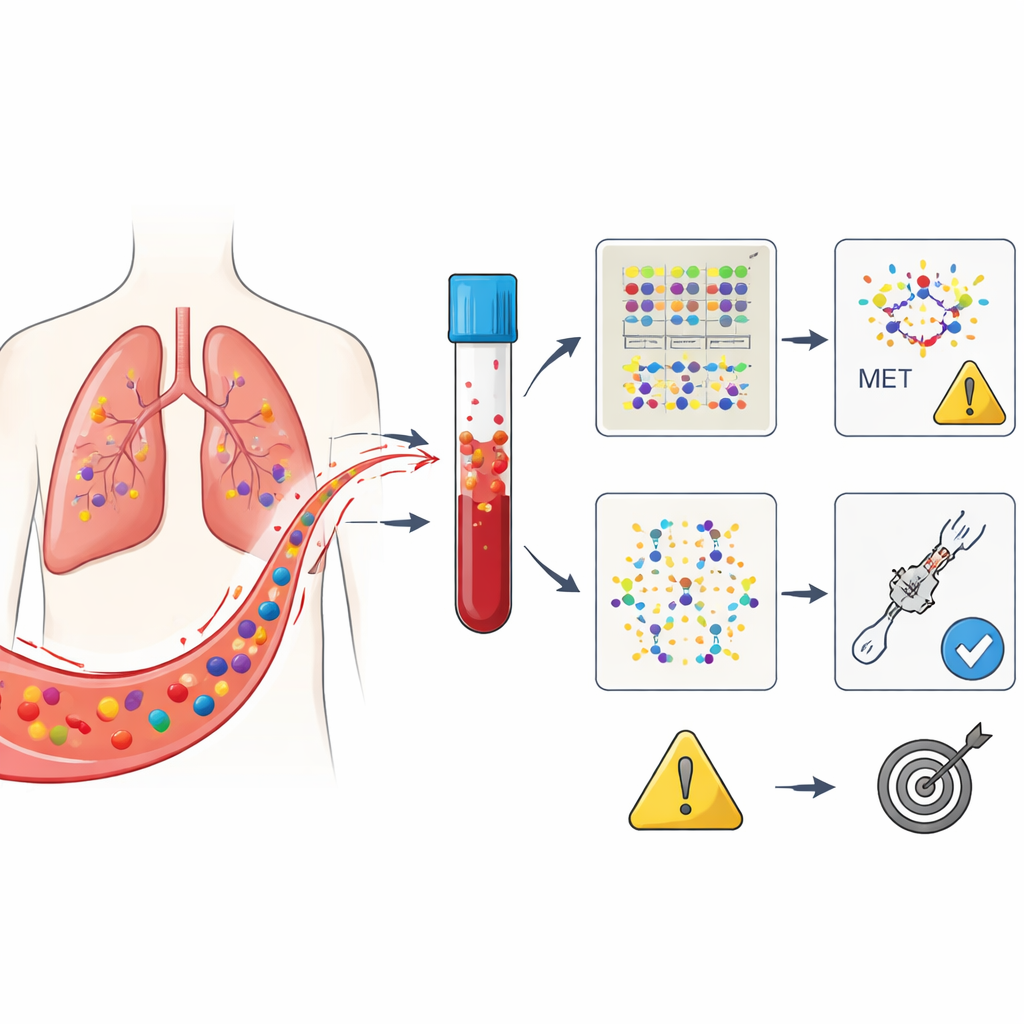
Tre sätt att läsa samma blodsignal
Den centrala frågan var vilken av dessa tre blod"vyer" som bäst förutsäger vem som svarar på ensartinib och hur länge det svaret varar. Vid start hade inte alla patienter påvisbart tumör-DNA i blodet, trots att deras tumörer bar MET-defekten; detta speglar hur ojämnt tumörer frigör DNA. I ett tidigt skede förutsade enbart positivt eller negativt tumör-DNA vid baslinjen inte starkt utfall. Men vid fyraveckorsmärkningen framträdde ett tydligt mönster: patienter vars blod inte längre visade MET-relaterade DNA-förändringar tenderade att förbli fria från sjukdomsförsämring betydligt längre än de där dessa signaler bestod. Detta gällde även om tumöravbildningar vid den tidpunkten fortfarande kunde vara tveksamma.
När MET-signaler försvinner förbättras utfallen
När teamet granskade hur blodresultaten förändrades över tid upptäckte de tre banor. Vissa patienter hade aldrig påvisbart MET-DNA i blodet, vissa började positiva och blev negativa, och andra förblev positiva eller utvecklade nya MET-förändringar. De som rensade MET-signaler vid vecka fyra hade längst period innan deras cancer progredierade, omkring nio månader i genomsnitt, och hade den högsta andelen mätbar tumörminskning. Patienter som förblev positiva för MET-DNA klarade sig mycket sämre, med sjukdomsprogression på knappt över två månader i genomsnitt. Övervakning av de bredare mutationstexterna gav också användbar information, men var mindre precis eftersom många lågnivå- eller orelaterade förändringar kunde göra bilden mer diffus.
Att väga enkelhet mot djupare insikt
Att använda enbart MET-relaterat DNA som vägledning gav den skarpaste och enklaste bilden av huruvida ensartinib var effektivt. Denna fokuserade strategi hade hög specificitet, vilket innebär att när MET-signaler försvann fanns det en god sannolikhet att patienten skulle må bra. Det gör metoden attraktiv som ett praktiskt verktyg: enkelgenstester är billigare, snabbare och lättare att tolka än stora genpaneler. Samtidigt hade bredare genpaneler fortfarande värde eftersom de kunde upptäcka nya mutationer som förklarar varför en tumör senare slutade svara och peka på framtida behandlingsalternativ. Studien antyder att en kombination av en snäv, MET-centrerad vy för tidiga behandlingsbeslut och en bredare vy för att följa upp resistens kan ge det bästa av två världar.
Vad detta betyder för patienter
För en lekman är huvudbudskapet att ett blodprov taget redan en månad efter påbörjad behandling med ensartinib kan ge en indikation på läkemedlets långsiktiga nytta. Om MET-relaterat tumör-DNA försvinner ur blodomloppet är sannolikheten för en meningsfull och varaktig nytta hög; om det kvarstår kan läkare behöva följa patienten noggrannare eller överväga andra alternativ. Även om detta var en relativt liten, enarmsstudie som behöver bekräftas i större grupper stärker den idén att "flytande biopsier" kan fungera som ett tidigt betyg på riktade behandlingar. I framtiden skulle sådan övervakning kunna hjälpa till att individualisera vården, skona patienter från att fortsätta på ineffektiva läkemedel och snabbare leda dem till behandlingar som fungerar.
Citering: Zhou, M., Zhu, Y., Sun, X. et al. Comparative analysis of ctDNA monitoring strategies in advanced NSCLC with MET exon 14 skipping mutations treated with ensartinib. npj Precis. Onc. 10, 110 (2026). https://doi.org/10.1038/s41698-026-01284-6
Nyckelord: circulerande tumör-DNA, MET exon 14-skipning, ensartinib, icke-småcellig lungcancer, övervakning med flytande biopsi