Clear Sky Science · sv
Överuttryck av mitokondriella komplex I-subenheten NDUFS4 driver gliomprogression genom att reglera mitokondriefunktion och COX5B
Varför energikrävande hjärntumörer är viktiga
Gliom är bland de mest aggressiva hjärncancerformerna och återkommer ofta trots kirurgi, strålning och cytostatika. Denna studie undersöker gliomcellerna på djupet för att ställa en enkel fråga med stora konsekvenser: är dessa tumörer beroende av en särskild del av sina inre ”kraftverk” för att växa och sprida sig? Genom att följa ett litet mitokondriellt protein kallat NDUFS4 avslöjar forskarna en metabolisk svag punkt som verkar driva tumörprogression samtidigt som friska hjärnceller påverkas betydligt mindre.
En dold strömbrytare i hjärntumörernas kraftverk
Inne i varje cell fungerar mitokondrier som små generatorer som omvandlar näring till användbar energi. I gliomceller pressas dessa generatorer i övervarv. Forskargruppen analyserade stora offentliga cancerregister och enkelcellssekvenseringsdata och fann att proteinet NDUFS4, en komponent i ett av mitokondriens huvudkomplex för energiproduktion, konsekvent var uppreglerat i gliomvävnad jämfört med normal hjärna. Högre nivåer av NDUFS4 korrelerade med högre tumörgrad och med patienter som avled snabbare av sin sjukdom. På enkelcellsnivå visade analysen att detta extra NDUFS4 var koncentrerat specifikt till tumörceller snarare än till omgivande icke‑cancerösa celler i hjärnan.
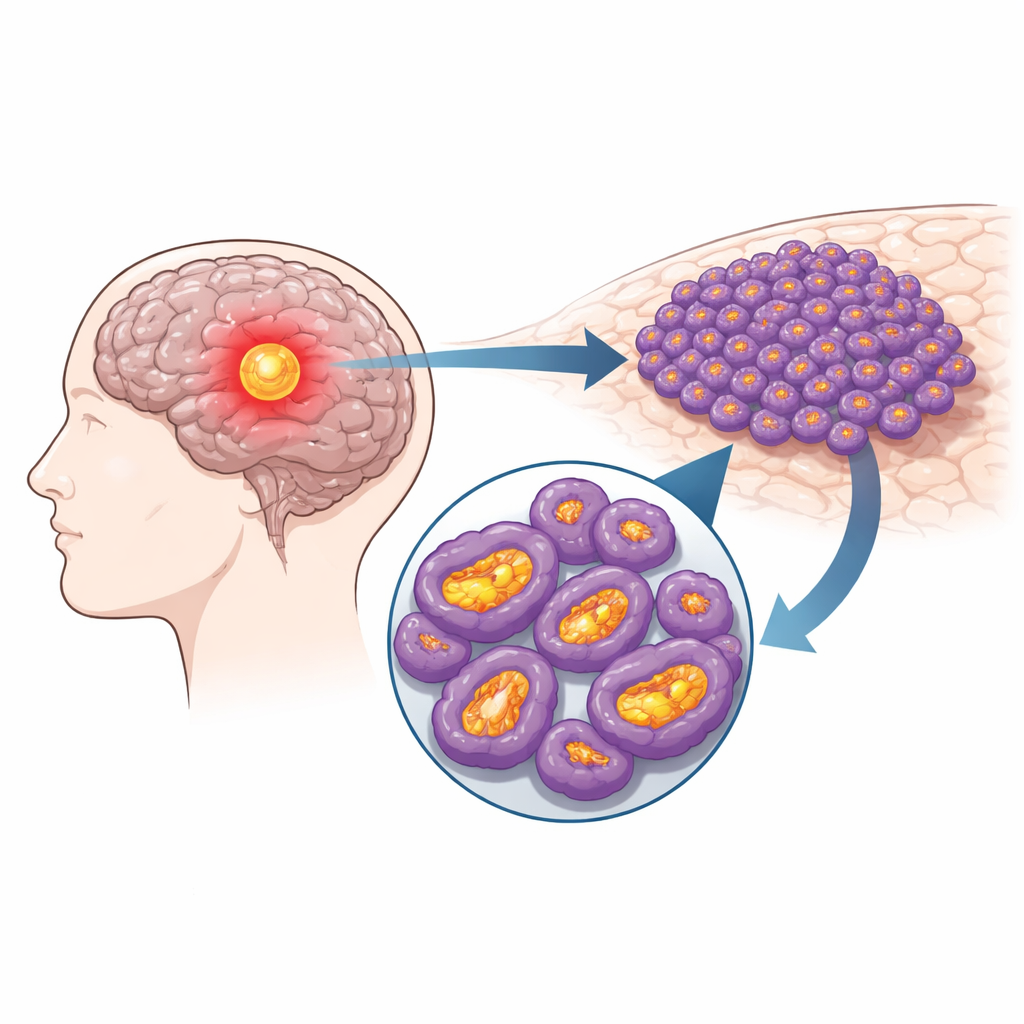
Sänk energin för att bromsa cancern
För att testa om NDUFS4 bara är en markör eller en verklig drivkraft minskade eller eliminerade forskarna proteinet i patient‑hereledda gliomceller odlade i labb. När NDUFS4 tystades eller knockoutades försämrades cellernas mitokondrier: syreförbrukningen sjönk, ett centralt steg i energiproduktionen försvagades och mängden cellulärt bränsle (ATP) minskade. Samtidigt ökade skadliga biprodukter, så kallade reaktiva syreradikaler, och cellernas inre membran visade tecken på stress och oxidation. Funktionellt delade dessa energibristande tumörceller sig mindre, bildade färre kolonier, rörde sig och invaderade mindre effektivt och uppvisade fler tecken på programmerad celldöd. Slående nog gav samma genetiska påverkan i icke‑cancerösa astrocyter — stödjeceller från normal hjärnvävnad — liten eller ingen skada, vilket tyder på att tumörceller är ovanligt beroende av denna mitokondriella brytpunkt.
Ökad effekt gör tumörer mer aggressiva
Den omvända delen av experimentet gav en lika tydlig bild. När forskarna fick gliomceller att producera extra NDUFS4 blev deras mitokondrier mer aktiva: energiuttaget ökade och det centrala respiratoriska komplexet arbetade hårdare. Dessa upptrimmade celler växte snabbare, migrerade lättare och invaderade barriärer mer aggressivt, både i primära patientceller och i etablerade labbcellinjer. Hos möss bildade gliomceller som konstruerats för att bibehålla höga NDUFS4‑nivåer större intrakraniella tumörer, medan celler med nedsatt NDUFS4 växte mycket långsammare i hjärnan, visade svagare mitokondriefunktion, mer oxidativ skada, färre delande celler och fler döende celler. Tillsammans visar dessa experiment att NDUFS4 inte bara är en passagerare utan en drivkraft i gliomprogression.
En partnerprotein kopplar energikontroll till tumörbeteende
För att förstå hur NDUFS4 ger så omfattande effekter korsrefererade teamet genuttrycksdata från bulk‑tumörer, enkelceller och kartläggningar av cancerproteiner och identifierade ett annat mitokondriellt protein, COX5B, som en nyckelpartner. COX5B hjälper till i det sista steget av cellens huvudsakliga energikedja. Det var starkt korrelerat med NDUFS4‑nivåer i gliom och är redan känt för att vara uppreglerat i andra cancerformer. När forskarna minskade COX5B i gliomceller såg de samma mönster som vid NDUFS4‑förlust: försämrad mitokondriefunktion, ökad oxidativ stress, långsammare tillväxt och rörelse samt ökad celldöd. Avgörande var att återställande av COX5B i NDUFS4‑utsatta celler återvände stora delar av mitokondrieskadorna och den antitumöreffekten. De fann också att NDUFS4 påverkar hur starkt en transkriptionsfaktor (Sp1) binder till COX5B‑genens kontrollregion, vilket hjälper till att reglera hur mycket COX5B cellen producerar.
Vad detta betyder för framtida behandlingar av hjärncancer
För en icke‑specialist är huvudbudskapet att många gliom tycks vara beroende av ett överdrivet energisystem centrerat kring NDUFS4 och dess nedströmspartner COX5B. Att dämpa detta system berövar tumörcellerna den energi och balans de behöver för att växa och invadera, samtidigt som normala stödjeceller i hjärnan i jämförelse klarar sig relativt väl. Eftersom denna sårbarhet återfinns konsekvent i patientprover, isolerade celler och mössens hjärntumörer framträder NDUFS4 — och dess kontroll över COX5B — som ett lovande mål för nya läkemedel. Terapier som selektivt stör denna mitokondriella ”kraftkrets” skulle kunna komplettera befintliga behandlingar, potentiellt bromsa tumörtillväxt och förlänga överlevnad utan att allvarligt skada frisk hjärnvävnad.
Citering: Wu, J., Li, J., Xu, L. et al. Mitochondrial complex I subunit NDUFS4 overexpression drives glioma progression by regulating mitochondrial function and COX5B. npj Precis. Onc. 10, 99 (2026). https://doi.org/10.1038/s41698-026-01281-9
Nyckelord: gliom, mitokondrier, NDUFS4, COX5B, hjärntumörmetabolism