Clear Sky Science · sv
En tolkbar djupinlärningsmodell för att förutsäga molekylära subtyper av endometriecancer från H&E‑färgade preparat
Varför detta är viktigt för kvinnors hälsa
Endometriecancer, som uppstår i livmoderns slemhinna, är en av de vanligaste cancerformerna hos kvinnor och dödligheten ökar globalt. Läkare vet idag att denna cancer faktiskt förekommer i flera molekylära ”smaker” som svarar olika på kirurgi, strålning, cytostatika och nyare immunterapier. I dag kräver identifiering av dessa molekylära subtyper vanligtvis kostsamma och tidskrävande gentester som många sjukhus inte enkelt kan erbjuda. Denna studie undersöker om ett noggrant utformat artificiellt intelligens (AI)-system kan läsa rutinmässiga patologiplan—de rosa‑och‑lila vävnadsbilder som redan tas för varje patient—och noggrant härleda dessa molekylära subtyper, vilket potentiellt kan göra precisionsvård mer allmänt tillgänglig.
Närmare om tumördiversitet
Alla endometriecancer beter sig inte likadant. Vissa växer långsamt och förblir begränsade till livmodern; andra sprider sig tidigt och är svårare att behandla. Moderna riktlinjer delar in dessa tumörer i fyra molekylära subtyper baserat på DNA‑förändringar och hur cellerna reparerar genetiska skador. Dessa kategorier hjälper till att förutsäga utfall och vägleda beslut, till exempel hur omfattande kirurgin bör vara och om en patient kan ha nytta av immunterapi. De nödvändiga gentesterna och speciella färgningarna är emellertid dyra, kräver expertbedömning och finns ofta inte på mindre eller resurssvaga sjukhus. Patologer har länge misstänkt att många av dessa molekylära skillnader lämnar visuella ledtrådar i hur celler och stödjevävnad ser ut under mikroskopet—men dessa ledtrådar kan vara för subtila och komplexa för att det mänskliga ögat ska bedöma konsekvent.
Att lära datorer läsa patologiplan
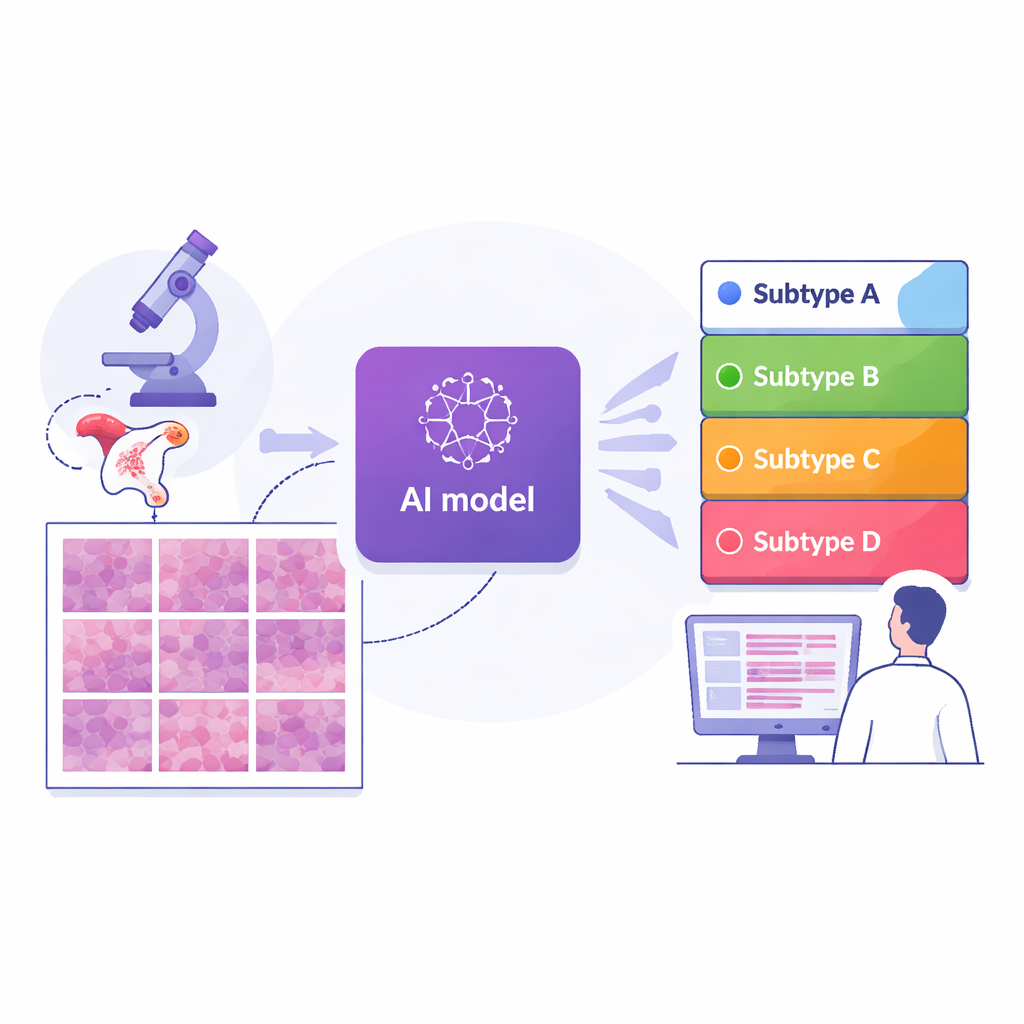
Forskarna samlade digitala bilder av 364 preparat från 324 kvinnor som behandlats vid ett stort cancercentrum i Shanghai, tillsammans med två oberoende jämförelsegrupper: 296 preparat från en internationell offentlig datamängd och 36 från ett annat sjukhus i Suzhou. Varje fall hade redan klassificerats i en av de fyra molekylära subtyperna med hjälp av avancerade gentester. Teamet delade sedan varje helbild i tusentals små brickor och tränade en djupinlärningsmodell—en typ av AI som används för bildigenkänning—att granska varje bricka och uppskatta sannolikheten att den tillhörde varje subtyp. Genom att medelvärdesbilda brick‑prediktionerna över hela sliden producerade systemet en enda subtyp‑prediktion per patient, vilket speglar hur läkare tänker på tumören som helhet.
Hur väl systemet presterade
I den huvudgrupp från Shanghai uppnådde AI en hög noggrannhet: dess övergripande poäng för att särskilja de fyra subtyperna (mätt med en standardstatistik som går från 0,5 vid gissning till 1,0 vid perfekt separation) var cirka 0,87. Prestandan förblev stark—runt 0,84—när modellen testades på de två externa grupperna från olika sjukhus och skanningssystem, vilket tyder på att tillvägagångssättet är relativt robust. Jämfört med flera ledande AI‑strategier som använder mer komplexa attention‑ eller pooling‑scheman presterade denna end‑to‑end‑modell, byggd på en modern bildanalysbas, generellt bättre. Viktigt är att författarna utformade systemet för att vara tolkbart: de använde visualiseringsverktyg för att framhäva exakt vilka regioner i varje bricka AI‑n förlitade sig på i sina beslut.
Vad AI:n “såg” i tumörens mikromiljö
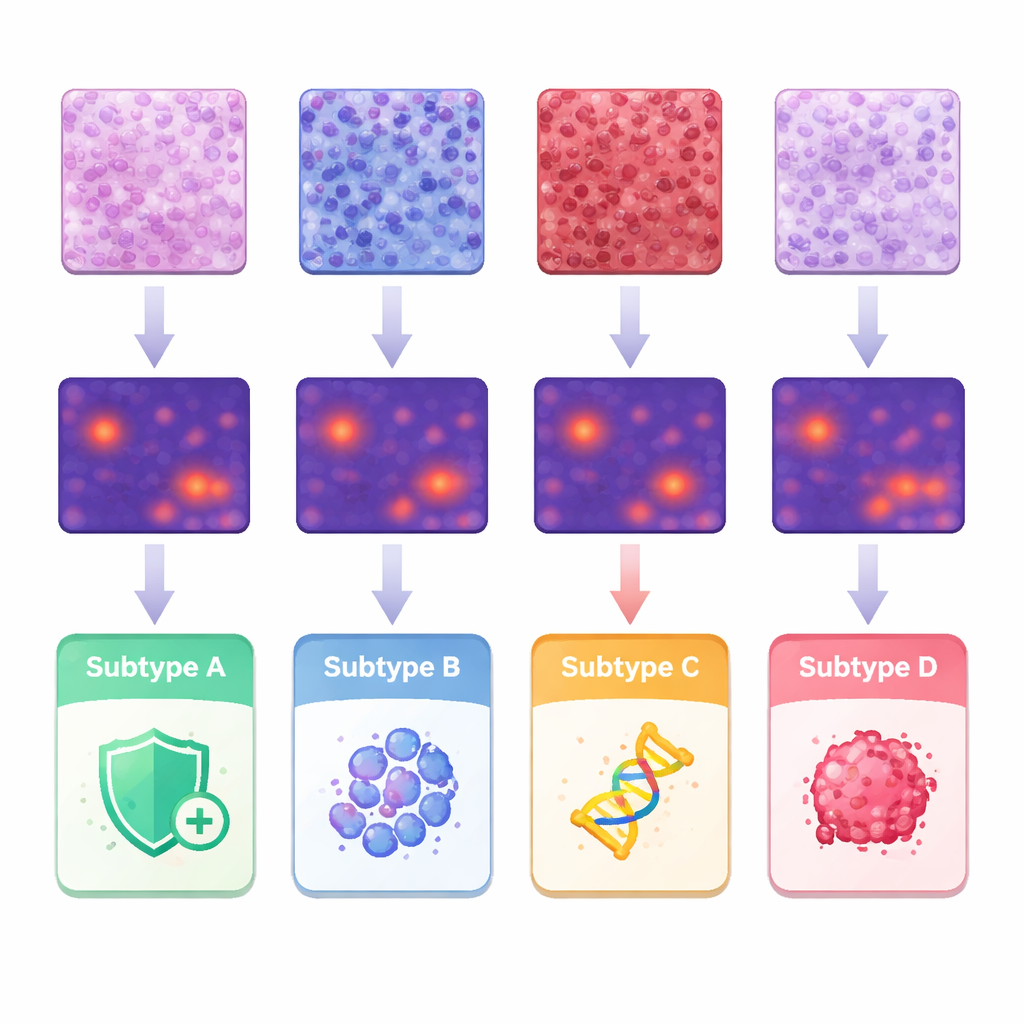
För att förstå vilka egenskaper som drev prediktionerna kopplade teamet AI:ns värmekartor till klassiska patologiska observationer och till detaljerade mätningar av enskilda cellers form och arrangemang. Tumörer i en subtyp visade tät infiltration av immunceller i stödjevävnaden, medan en annan subtyp tenderade att ha tätt packade strukturella celler. En tredje grupp visade mer solida ark av starkt avvikande tumörceller, och den subtyp som förknippas med aggressivt beteende uppvisade papillära, fingerliknande strukturer och mycket oregelbundna kärnor. Genom att segmentera och analysera omkring 245 miljoner celler kvantifierade forskarna skillnader i cellstorlek, variation och avstånd, och visade hur vissa kombinationer stämde överens med specifika subtyper. Dessa fynd stöder idén att molekylära skillnader lämnar ett igenkännbart avtryck på vävnadsarkitekturen som maskiner systematiskt kan upptäcka.
Från proof of concept till klinisk nytta
Detta arbete syftar inte till att ersätta gentester; istället föreslår det ett ”H&E‑först” triageverktyg som använder den standardfärgning som redan är förberedd för varje biopsi. I praktiken skulle en AI‑genererad sannolikhetskarta för subtyper kunna hjälpa patologer att avgöra vilka bekräftande tester som bör beställas först, prioritera begränsat vävnadsprov för de mest informativa analyserna och snabba upp behandlingsbeslut, särskilt på sjukhus där full molekylär profilering är svår att få. Studien lyfter också fram nuvarande begränsningar, såsom svagare prestanda för den mest sällsynta subtypen och behovet av större, mer mångsidiga datamängder innan införande. Ändå erbjuder den en övertygande demonstration att rutinmässiga mikroskopibilder bär tillräckligt med dold information för att AI ska kunna approximera komplexa molekylära etiketter, och öppnar en väg mot mer rättvis, datadriven vård för kvinnor med endometriecancer.
Citering: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
Nyckelord: endometriecancer, digital patologi, djupinlärning, molekylära subtyper, precision oncology