Clear Sky Science · sv
En integrerad single-cell-atlas för lungcancer avslöjar distinkta fibroblastfenotyper mellan adenocarcinom och skivepitelkarsinom
Varför omgivningen runt en tumör spelar roll
Lungcancer består inte enbart av cancerceller. Den liknar snarare en tätbefolkad stad där cancerceller samexisterar med blodkärl, immunceller och stödjeceller. Denna studie ställer en överraskande enkel fråga med stora konsekvenser: bygger de två huvudsakliga formerna av icke–småcellig lungcancer—adenocarcinom och skivepitelkarsinom—olika ”kvarter” i lungan, och kan dessa skillnader hjälpa till att förklara varför patienter får olika utfall? Med kraftfulla single-cell-verktyg kartlägger forskarna hundratusentals individuella celler för att visa hur en nyckelgrupp av stödjeceller, kallade fibroblaster, beter sig mycket olika i dessa två cancerformer.
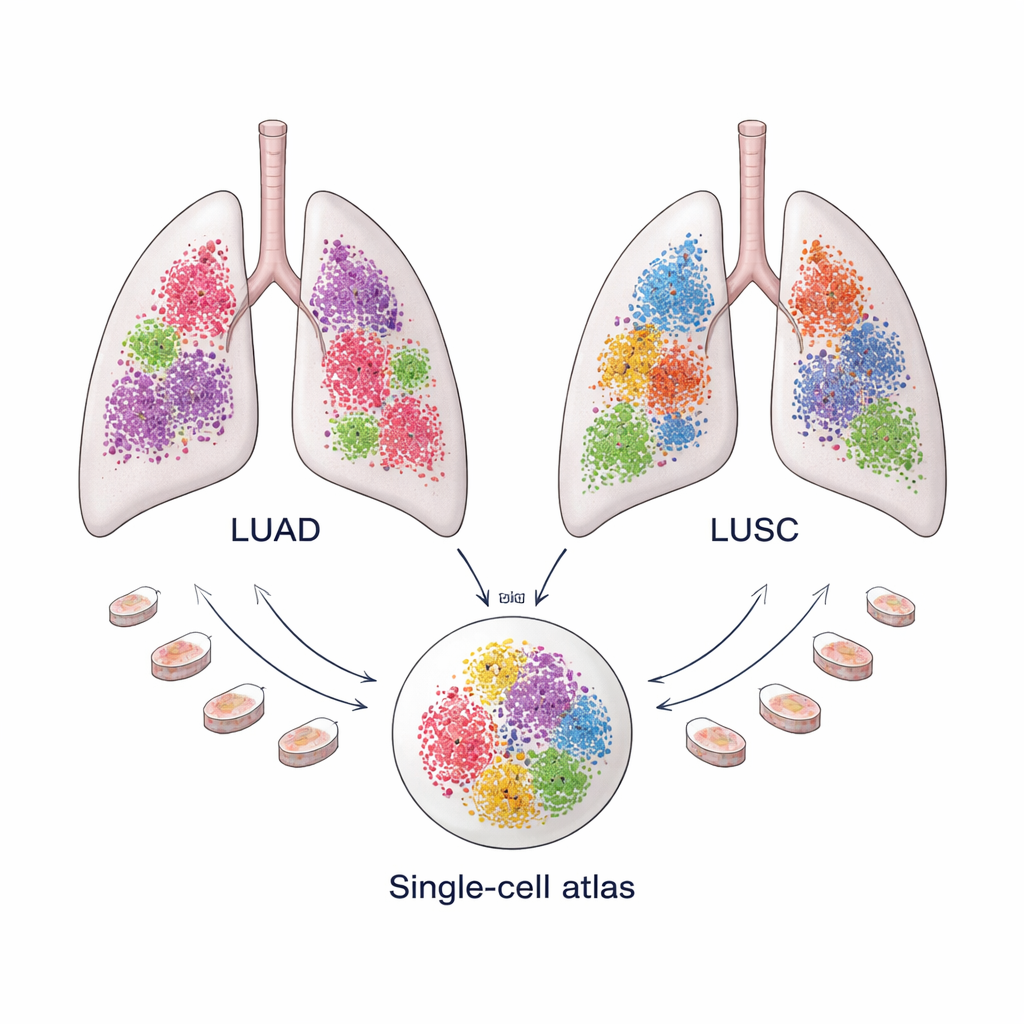
Två vanliga lungcancerformer, två distinkta ekosystem
Icke–småcellig lungcancer utgör cirka 85 procent av lungcancerfallen och domineras av två typer: lungadenocarcinom (LUAD), som ofta uppstår i de yttre delarna av lungan, och lungskivepitelkarsinom (LUSC), som tenderar att förekomma mer centralt. Även om båda idag behandlas under samma breda etikett svarar de olika på behandling och har skilda långtidserfarenheter. Vaxande bevis tyder på att dessa skillnader inte bara beror på cancercellerna själva, utan också på ”tumörmikromiljön”—blandningen av immunceller, blodkärl och strukturella celler som omger och interagerar med tumören.
Att bygga en single-cell-atlas för lungcancer
För att förstå dessa mikromiljöer i detalj samlade teamet en stor ”atlas” av single-cell RNA-sekvenseringsdata: 366 652 celler från 175 LUAD-prover och 125 238 celler från 74 LUSC-prover, hämtade från tio publika dataset. Varje cells genaktivitetsmönster fungerade som ett fingeravtryck som gjorde det möjligt för forskarna att sortera celler i stora grupper såsom immunceller, blodkärlsceller, cancerceller och strukturella eller ”stromala” celler. Sofistikerade beräkningsmetoder tog bort tekniskt brus och anpassade prover så att celler från olika patienter kunde jämföras direkt. Denna skala är avgörande, eftersom vissa celltyper—särskilt fibroblaster—är sällsynta och svåra att isolera i tillräckligt antal i enskilda studier.
Fibroblaster: formarna av tumörlandskapet
Fibroblaster är stödjeceller som bygger och omformar bindväv. I tumörer blir de cancerassocierade fibroblaster (CAF), som beroende på sitt tillstånd antingen kan hämma eller främja tumörtillväxt. Genom att fokusera på över 8 700 fibroblaster identifierade författarna fem huvudsakliga CAF-subtyper: myofibroblastiska CAFs (mCAFs), inflammatoriska CAFs (iCAFs), kärlassocierade CAFs (vCAFs), cyklande CAFs (cCAFs) och antigenpresenterande CAFs (apCAFs). Balansen mellan dessa subtyper skiljde sig markant mellan LUAD och LUSC. LUAD-tumörer tenderade att hysa fler iCAFs, som utsöndrar höga nivåer av inflammatoriska molekyler, medan LUSC-tumörer var rikare på mCAFs, som producerar styv, fibrös vävnad och hjälper till att forma tumörens fysiska stomme.
Cancerceller lär fibroblaster deras roller
För att testa om cancerceller själva instruerar fibroblaster att anta dessa identiteter odlade forskarna normala lungfibroblaster i skålar tillsammans med antingen LUAD- eller LUSC-cellinjer. När de exponerades för LUAD-celler slog fibroblasterna på gener som är typiska för iCAFs, inklusive välkända inflammatoriska signaler såsom IL-6 och vissa kemokiner. När de parades med LUSC-celler aktiverade samma fibroblaster istället mCAF-gener involverade i muskel-liknande kontraktion och kollagenproduktion. Analyser av cell-till-cell-kommunikation antydde att LUAD-celler använder cytokiner såsom IL-1, LIF och OSM för att driva den inflammatoriska iCAF-statusen, medan LUSC-celler i större utsträckning förlitar sig på mekaniska signaler och icke-kanonisk WNT-signalering för att skjuta fibroblaster mot den matrixbyggande mCAF-statusen.
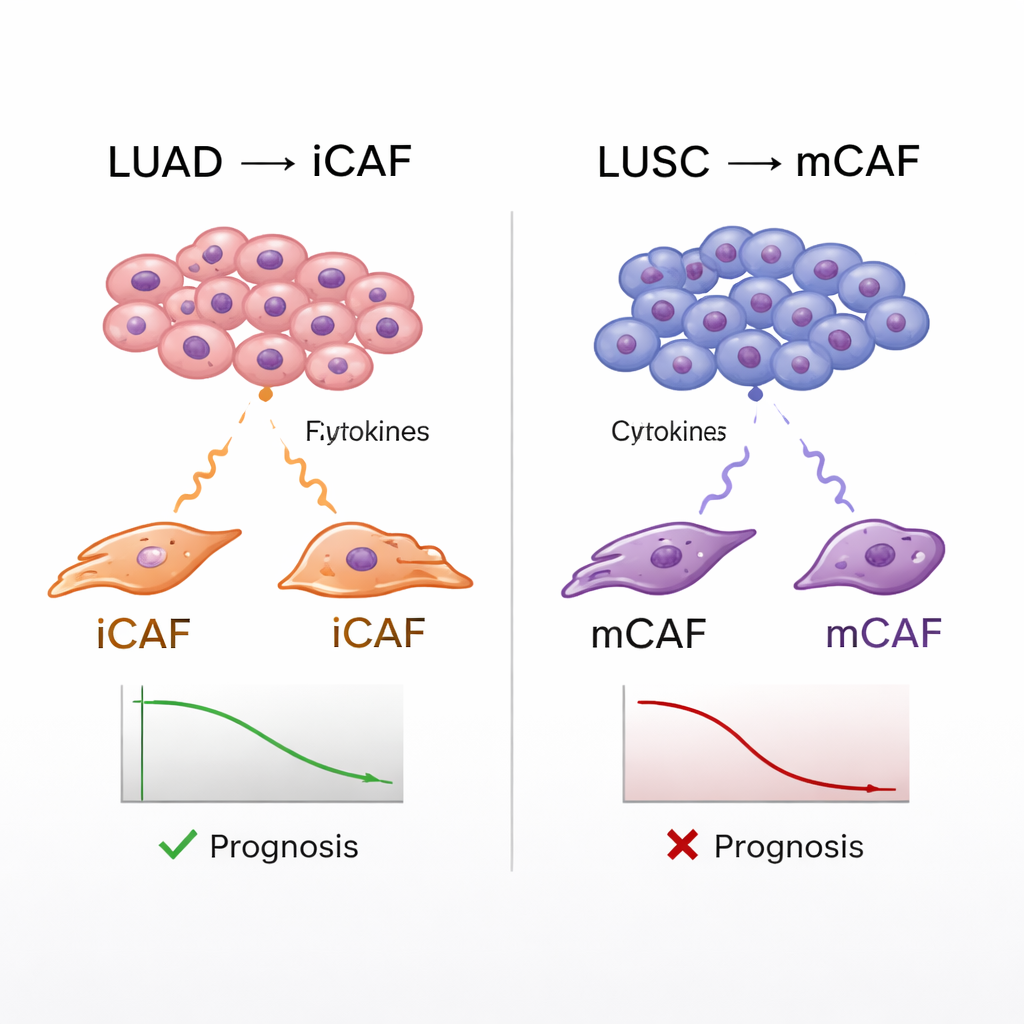
Koppla fibroblasttyper till patientutfall
Atlaset gjorde det också möjligt för teamet att koppla CAF-subtyper till verkliga patientdata. Genom att använda stora cancerregister uppskattade de hur starkt varje patients tumör uttryckte gensignaturer för de olika fibroblasttyperna, och jämförde sedan dessa poäng med överlevnad. I både LUAD och LUSC var tumörer som var berikade på mCAFs kopplade till sämre utfall, i linje med idén att ett tätt, fibröst kapsel runt tumörer kan underlätta cancerprogression och blockera immunsvar. iCAFs visade dock en delad funktion: i LUSC förutsagdes också sämre överlevnad vid höga iCAF-signaturer, medan de i LUAD associerades med bättre utfall. Ytterligare analyser föreslog att i LUSC bidrar iCAFs till att dra till sig neutrofiler—immunceller som i detta sammanhang verkar hämma hjälpsamma T-celler—vilket skapar en särskilt fientlig miljö för effektiva immunresponser.
Vad detta innebär för framtida lungcancervård
För icke-specialisten är huvudbudskapet att inte alla stödjeceller i lungtumörer är likadana, och samma fibroblastsubtyp kan ha motsatta betydelser beroende på cancerkontexten. LUAD och LUSC skiljer sig inte bara i cancercellernas DNA; de bygger olika mikroskopiska ekosystem som formar hur tumörer växer och hur patienter klarar sig. Genom att kartlägga dessa ekosystem cell för cell identifierar studien specifika fibroblastpopulationer som kan fungera som prognostiska markörer eller som mål för framtida behandlingar—i idealfallet så att behandlingar kan anpassas inte bara till cancerns typ utan även till vilka celler som omger och uppehåller den.
Citering: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Nyckelord: lungcancer, tumörmikromiljö, fibroblaster, single-cell RNA-sekvensering, cancerprognos