Clear Sky Science · sv
TheraMind: ett multi-LLM-ensemble för att påskynda läkemedelsomfördelning vid lungcancer genom granskning av fallrapporter
Varför det här är viktigt för patienter och läkare
För personer med avancerad lungcancer är tiden knapp och behandlingsalternativen tar ofta snabbt slut. Att utveckla helt nya läkemedel kan ta mer än ett decennium, men spridda ledtrådar om användbara terapier kan redan finnas gömda i publicerade patientberättelser, så kallade fallrapporter. Denna artikel presenterar TheraMind, ett artificiellt intelligenssystem som genomsöker tusentals sådana rapporter för att hitta befintliga läkemedel som eventuellt kan återanvändas säkert för att hjälpa personer med svårt behandlad lungcancer.
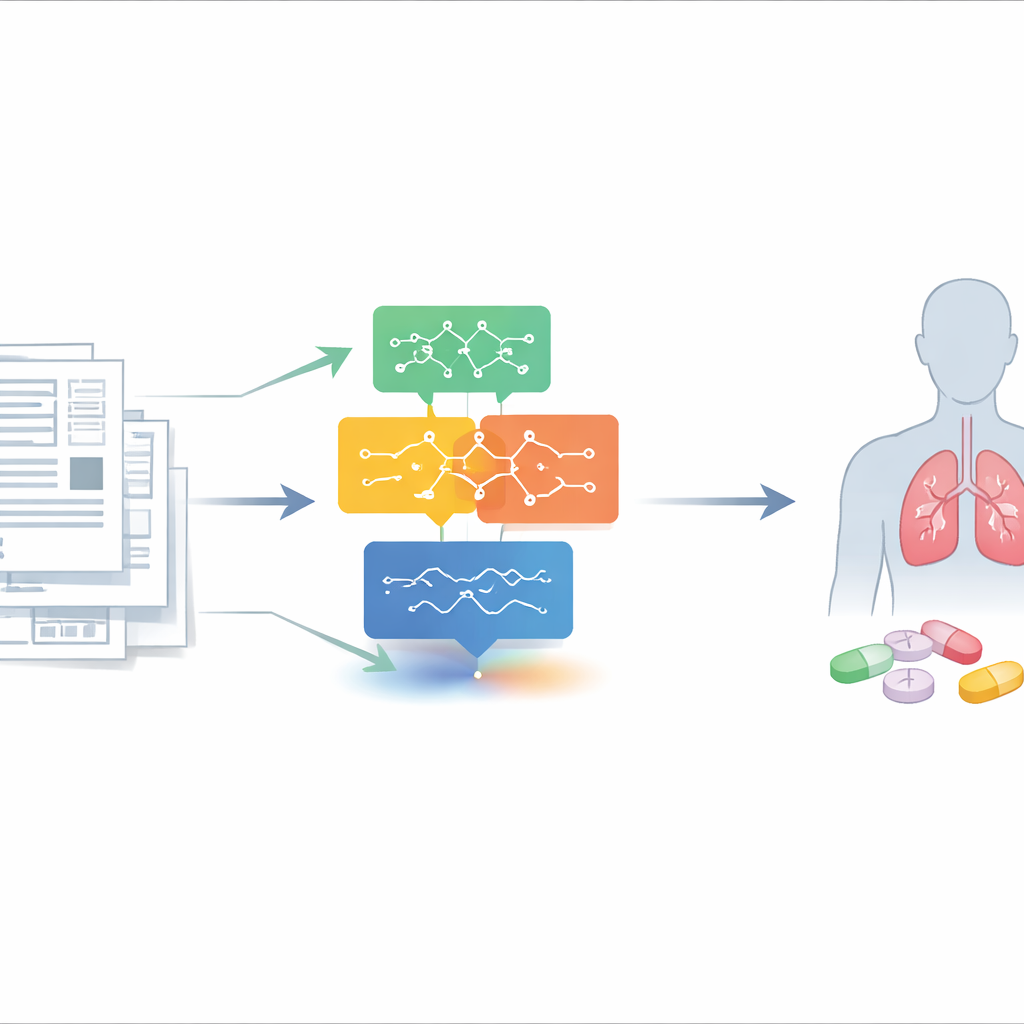
Utmaningen i att hitta nya användningsområden för gamla läkemedel
Icke-småcellig lungcancer är världens dödligaste cancer, med överlevnadssiffror som förblir mycket låga när sjukdomen har spridit sig. Att upptäcka och pröva nya läkemedel från grunden är långsamt, kostsamt och riskfyllt. I kontrast är ”omfördelade” läkemedel redan godkända för andra tillstånd, så deras säkerhet är bättre känd. Onkologer är intresserade av sådana läkemedel, särskilt för patienter som uttömt standardbehandlingarna, men de behöver verklighetsnära bevis för att ett läkemedel faktiskt hjälpt någon med lungcancer — inte bara lovande laboratoriedata. Dessa kliniska ledtrådar dyker ofta upp i enskilda fallrapporter djupt begravda i medicinsk litteratur, vilket är svårt och tidskrävande att hitta manuellt.
En digital läsare för tusentals patientberättelser
Forskarna byggde TheraMind för att fungera som en outtröttlig, noggrann läsare av fallrapporter. Utgångspunkten var 18 läkemedelskandidater föreslagna av tidigare genomiska och laboratoriestudier; systemet hämtade automatiskt 10 023 fallrapporter från PubMed, den största databasen för medicinska artiklar. Därefter matades texten i varje rapport till tre separata språkmodeller — olika AI-”läsare” tränade för att förstå medicinsk text. För varje rapport besvarade dessa modeller samma fyra enkla frågor: Beskrivs patienten som ha icke-småcellig lungcancer? Gav man studie-läkemedlet specifikt för att behandla detta? Avbröts behandlingen i förtid? Och upplevde patienten ett gott kliniskt utfall?
Hur AI-teamet når ett gemensamt beslut
När TheraMind har omvandlat varje rapport till ett set ja-eller-nej-svar träder flera beslutslager in. En metod använder ett handgjort besluts-träd som kräver att alla fyra villkor är uppfyllda innan ett fall kallas relevant för läkemedelsomfördelning. En annan låter en enda modell väga bevisen mer flexibelt och beaktar både ja-eller-nej-svaren och de korta förklaringar den producerat. Den mest kraftfulla metoden kombinerar tre separata klassificerare, var och en baserad på en annan modell, och accepterar en rapport endast när minst två av tre håller med om att den är relevant. Detta ”majoritetsomröstnings”-angreppssätt hjälper till att utjämna individuella misstag, ungefär som att be flera oberoende läkare granska samma journal.
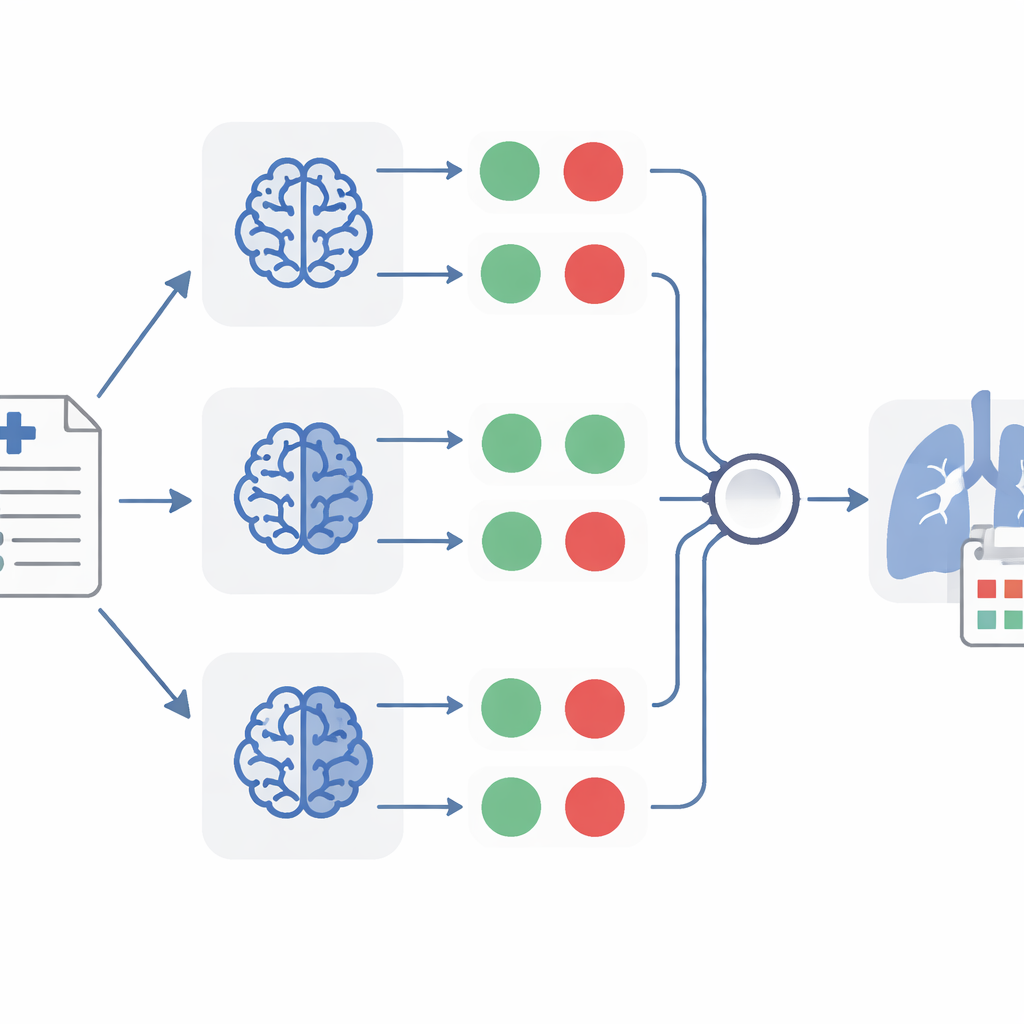
Vad TheraMind upptäckte i fallrapporter om lungcancer
Tillämpat på den stora samlingen fallrapporter flaggade TheraMind 26 rapporter som starkt stödjer användningen av tio olika läkemedel vid icke-småcellig lungcancer. Ensemblemetoden uppnådde en återkallelse på cirka 92 procent, vilket betyder att den fångade nästan alla verkligt relevanta rapporter, samtidigt som den bibehöll en mycket hög specificitet på 99,7 procent, så att mycket få irrelevanta rapporter slank igenom. För varje utvald rapport extraherade systemet också viktiga patientuppgifter — såsom ålder, kön, medicinsk bakgrund, tillstånd och det misstänkta läkemedlet — i ett konsekvent dataformat och genererade en kort, lättförståelig sammanfattning av fallet. Mänskliga granskare med bakgrund inom biologi och datavetenskap kontrollerade dessa resultat och bekräftade att en av modellerna i synnerhet producerade mycket noggranna och fullständiga extraktioner.
Bortom lungcancer och in i kliniken
För att testa systemets flexibilitet riktade teamet också TheraMind mot bröstcancer och flera kandidatläkemedel som tidigare identifierats i deras egen forskning. I det scenariot rapporterade systemet inga matchande fallrapporter, vilket korrekt speglade den vetenskapliga litteraturen i nuläget snarare än att hitta på bevis. Författarna menar att denna typ av strukturerade, transparenta pipeline — som kombinerar regelbaserad logik med flera AI-läsare — kan hjälpa till att stänga klyftan mellan laboratoriefynd och behandlingar redo för kliniska prövningar. De framhäver både löftet i att tillämpa liknande metoder på andra cancerformer och behovet av att hantera patientsekretess noggrant om framtida versioner kopplas direkt till elektroniska journaler.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt förvandlar TheraMind spridda, ostrukturerade patientberättelser till organiserad evidens som läkare och forskare kan handla utifrån. Genom att snabbt lyfta fram rapporter där befintliga läkemedel verkar hjälpa personer med lungcancer kan det vägleda vilka omfördelade läkemedel som förtjänar närmare studier i kliniska prövningar. Medan det inte ersätter medicinskt omdöme erbjuder denna multi-modell AI-läsare ett sätt att sila igenom stora mängder medicinsk text och leverera en kort, tillförlitlig lista över lovande alternativ för patienter som akut behöver nya valmöjligheter.
Citering: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
Nyckelord: läkemedelsomfördelning, lungcancer, fallrapporter, stora språkmodeller, utvinning av klinisk evidens