Clear Sky Science · sv
Neoadjuvant sintilimab, albuminbundet paklitaxel och karboplatin för lokalt avancerad, resekabel skivepitelcarcinom i esofagus: klinisk studie och mekanistisk undersökning
Vända trenden mot en dödlig halscancer
Matstrupscancer är en av de dödligaste cancerformerna globalt och upptäcks ofta först sedan den hunnit växa djupt in i bröstkorgen. Många patienter kan fortfarande opereras, men även med dagens bästa kemoterapi och strålning är risken stor att sjukdomen återkommer. Denna studie prövar ett nytt sätt att stärka kroppens egna försvar före operation och granskar på mikroskopisk nivå hur tumörer och omkringliggande celler förändras som svar. Resultaten tyder på effektivare behandlingar och en väg mot verkligt individualiserad vård.
En ny tremedicinskt schema före operation
Forskarna inkluderade 24 personer i Kina med en vanlig och aggressiv form av matstrupscancer kallad skivepitelcarcinom. Alla hade tumörer som var avancerade men fortfarande möjliga att avlägsna kirurgiskt. Innan de gick till operationssalen fick varje patient tre cykler av en kombinationsbehandling: sintilimab, en immuneaktiverande antikropp som hjälper T‑celler att känna igen cancer; samt två standardkemoterapier, albuminbundet paklitaxel och karboplatin. Efter denna ”neoadjuvanta” fas genomgick patienterna operation för att avlägsna tumören i matstrupen, och de flesta fortsatte därefter med sintilimab.
Starkare tumörkrympning och lovande överlevnad
När kirurger och patologer undersökte de borttagna tumörerna fann de att denna pre‑operativa regim gav djup krympning hos många patienter. Ungefär 42 % uppvisade vad läkare kallar en stor patologisk respons, vilket betyder att endast en liten andel levande cancerceller återstod. En av tre patienter hade inga påtagliga cancerceller alls i huvudtumörområdet. På bilder och vid klinisk uppföljning var resultaten också lovande: tre år efter behandlingen var ungefär tre av fyra patienter i livet utan tecken på återkomst, och nästan fyra av fem var fortsatt i livet. Viktigt är att biverkningarna av detta intensifierade schema var hanterbara, utan behandlingsrelaterade dödsfall och att kirurgisk borttagning förblev säker och genomförbar.
Hur tumörens närområde formar responsen
Inte alla patienter gynnades i lika hög grad, så teamet ställde frågan varför. De fokuserade på tumörmikromiljön—det komplexa närområdet av cancerceller, immunceller och signalmolekyler. Genom riktade proteinmätningar på noggrant dissekerade tumörprover jämförde de de som svarade bra med de som inte gjorde det. Före behandling fann de 14 proteiner som skilde mellan de två grupperna. Ett ytprotein, CD44, utmärkte sig: tumörer med högre CD44‑nivåer tenderade att svara bättre på sintilimab‑baserad terapi. Efter behandling minskade många proteiner som är inblandade i immunaktivitet och DNA‑reparation hos responderande patienter, vilket tyder på att kombinationsbehandlingen framgångsrikt störde tumörens stödsystem och omformade den lokala immunsituationen.
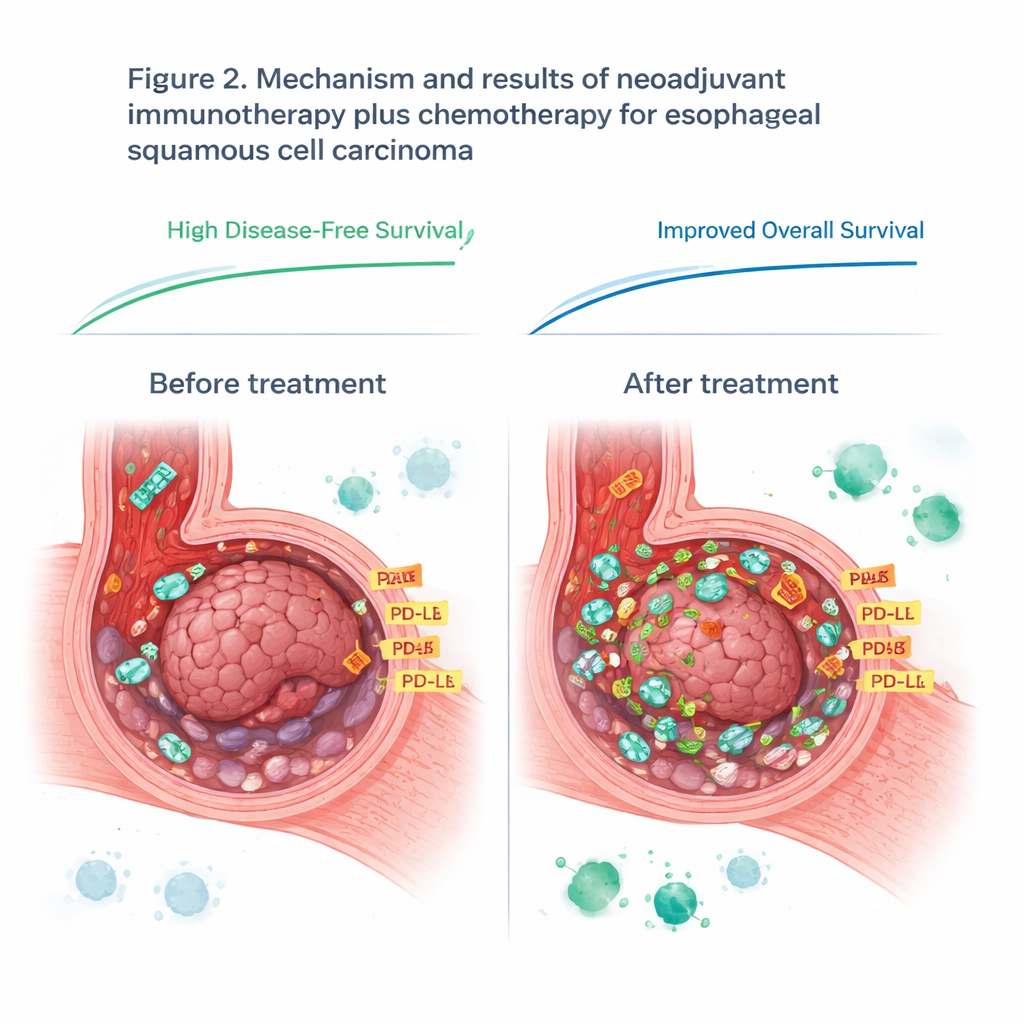
Att ompröva en populär immunmarkör
Studien undersökte också PD‑L1, ett protein som ofta används som kompass för att avgöra vem som kan dra nytta av immunkontrollspunkts‑läkemedel. Före behandling förutsade inte PD‑L1‑nivåer på tumörprover vem som skulle klara sig bra, vilket utmanar nuvarande praxis för denna cancertyp. Däremot steg PD‑L1‑nivåerna hos varje patient under behandlingen, sannolikt eftersom det aktiverade immunsystemet fyllde tumören med inflammatoriska signaler. Efter terapi var högre PD‑L1‑nivåer i den kvarvarande tumörvävnaden mer nära kopplade till hur väl immunterapin fungerade. Detta tyder på att tidpunkten spelar roll: en ensam mätning av PD‑L1 före behandling kan missa avgörande förändringar som utvecklas när immunsystemet engageras.
Vad detta betyder för patienter och framtiden
För personer som står inför operation för avancerad matstrupscancer ger denna studie två hoppfulla budskap. För det första verkar kombinationen av sintilimab och kemoterapi före operation kunna krympa tumörer djupare och förbättra chanserna till långsiktig överlevnad utan att tillföra farliga biverkningar. För det andra visar arbetet att tumören och dess mikromiljö inte är fasta; de omformas av behandlingen på sätt som kan spåras genom proteiner som PD‑L1 och CD44. I framtiden skulle sådana molekylära fingeravtryck kunna hjälpa läkare att välja och justera behandlingar i realtid, och omvandla fler ”kalla” tumörer som ignorerar immunsystemet till ”heta” tumörer som inbjuder till ett kraftfullt, bestående immunsvar.
Citering: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Nyckelord: matstrupscancer, immunterapi, neoadjuvant behandling, PD-1-hämmare, tumörmikromiljö