Clear Sky Science · sv
Algoritmstödd individualiserad terapidesign förbättrar överlevnad i en musmodell för trippelnegativ bröstcancer
Varför smartare kemoterapi spelar roll
Kemoterapi räddar liv, men ges fortfarande till stora delar enligt en ”en storlek passar alla”-princip: personer med liknande cancer får ofta samma läkemedelsdos på samma schema. Det kan innebära svåra biverkningar för vissa och otillräcklig nytta för andra. Studien som beskrivs här ställer en enkel men kraftfull fråga: vad om vi kunde använda datoralgoritmer för att anpassa kemoterapin till varje individ i realtid, på samma sätt som en termostat reglerar värmen i ett hus? Med en avancerad musmodell av en aggressiv bröstcancer visar forskarna att sådan skräddarsydd dosering kan förlänga överlevnaden och begränsa utvecklingen av läkemedelsresistens.
Problemet med rutinmässiga cancerläkemedelsscheman
I dag får många patienter den högsta dos kemoterapi de tål, given vid fasta intervall. Detta så kallade maximalt tolererade dosprotokoll tar inte hänsyn till hur snabbt en viss tumör växer, hur patientens kropp omsätter läkemedlet eller hur tumören svarar över tid. Som ett resultat kan tumörer först krympa men sedan komma tillbaka som mer läkemedelsresistenta versioner, samtidigt som patienterna drabbas av kraftiga biverkningar. Tidigare försök att förbättra detta, som ”metronomisk” kemoterapi med mindre, tätare doser, har gett blandade resultat i kliniska prövningar och har inte tydligt definierat hur doser och tidpunkt bäst ska väljas. Det finns ett klart behov av ett mer rationellt, individualiserat sätt att schemalägga kemoterapi.
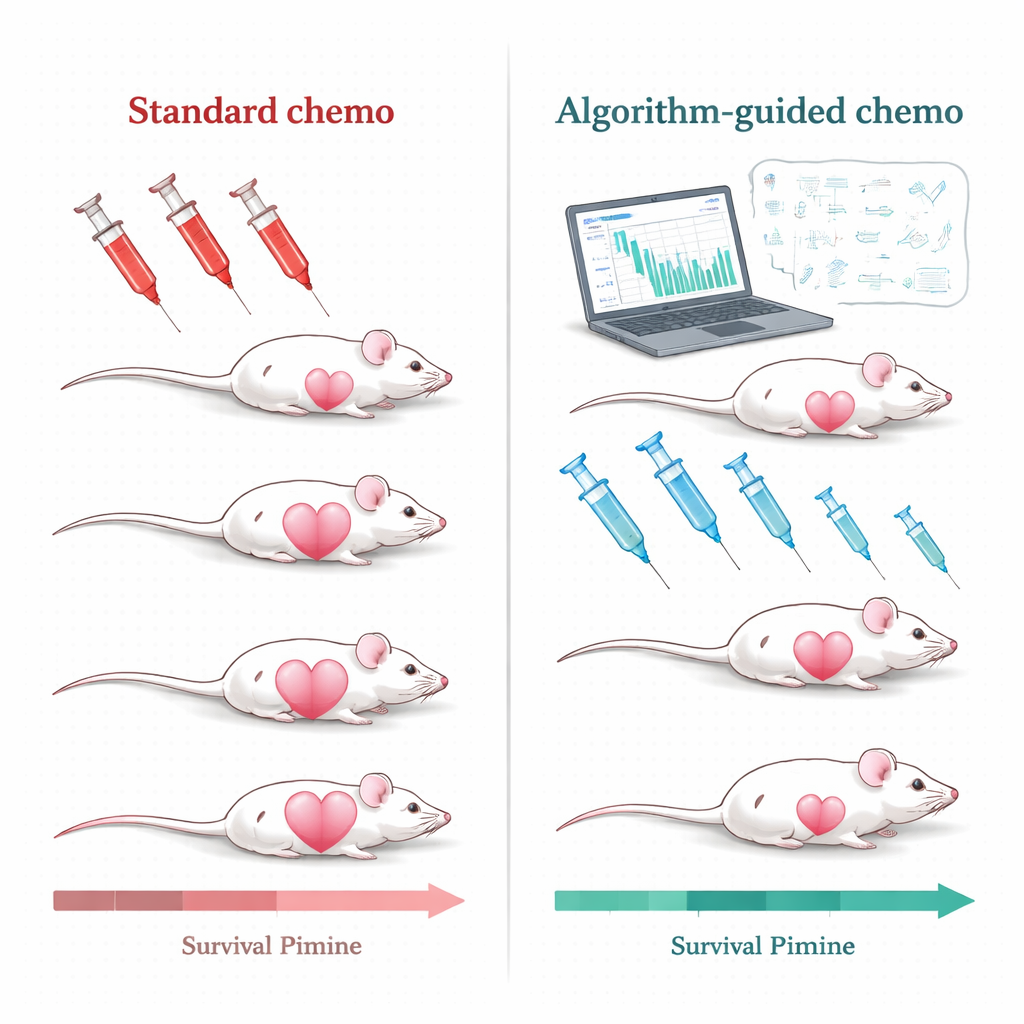
Använda algoritmer för att skräddarsy behandling
Forskargruppen tacklade denna utmaning i möss med trippelnegativa brösttumörer, en form av bröstcancer som hos människor är särskilt svår att behandla och som fortfarande nästan uteslutande förlitar sig på kemoterapi. Mössen behandlades med en vanligt använd läkemedelsformulering, pegylated liposomal doxorubicin. Istället för att upprepa högdosbehandling endast när tumörer växte tillbaka till en viss storlek byggde forskarna matematiska modeller som beskriver hur tumören växer, krymper under behandling och hur läkemedlet rör sig i blodbanan. De matade sedan modellerna med enkla, kliniskt realistiska mätningar: upprepade tumörstorleksavläsningar och läkemedelsnivåer i blodet. Utifrån dessa indata genererade en datoralgoritm personliga behandlingsplaner för varje mus.
Två sätt att låta datorn hjälpa till
Studien testade två varianter av algoritmstödd terapiutformning. I den ena metoden, kallad PDPK, använde datorn tidiga data för att utforma ett 30-dagarsschema med relativt små, upprepade doser avsedda att hålla läkemedelsnivån i blodet jämn men låg—tillräckligt hög för att kontrollera tumören, men tillräckligt låg för att begränsa toxicitet. I den andra metoden, kallad model predictive control, uppdaterade algoritmen planen varje dag baserat på den senaste tumörmätningen och justerade dosstorlekarna för att successivt trycka tumören nedåt. Båda metoderna byggde på samma grundidé: använd en realistisk ”digital tvilling” av den tumörbärande musen för att simulera många möjliga doseringsmönster i förväg och välja de som mest sannolikt fungerar bäst inom säkerhetsbegränsningar.
Längre överlevnad och mindre läkemedelsresistens
När teamet jämförde dessa algoritmstyrda regimer med det standardmässiga högdos-, tumörutlösta protokollet var skillnaderna slående. Under konventionell terapi krympte tumörerna ofta dramatiskt initialt men kom så småningom tillbaka, och upprepade stora doser gynnade framväxten av läkemedelsresistent sjukdom. I kontrast höll de flesta algoritmdesignade behandlingar tumörerna under mycket strängare kontroll, förlängde tiden till återfall och förhindrade i många fall tydliga tecken på resistens under studiens löptid. Över flera dussin möss levde både PDPK- och model predictive control-grupperna avsevärt längre än djur på standardregimen, med flera algoritmbaserade strategier som visade starka, statistiskt signifikanta överlevnadsvinster.
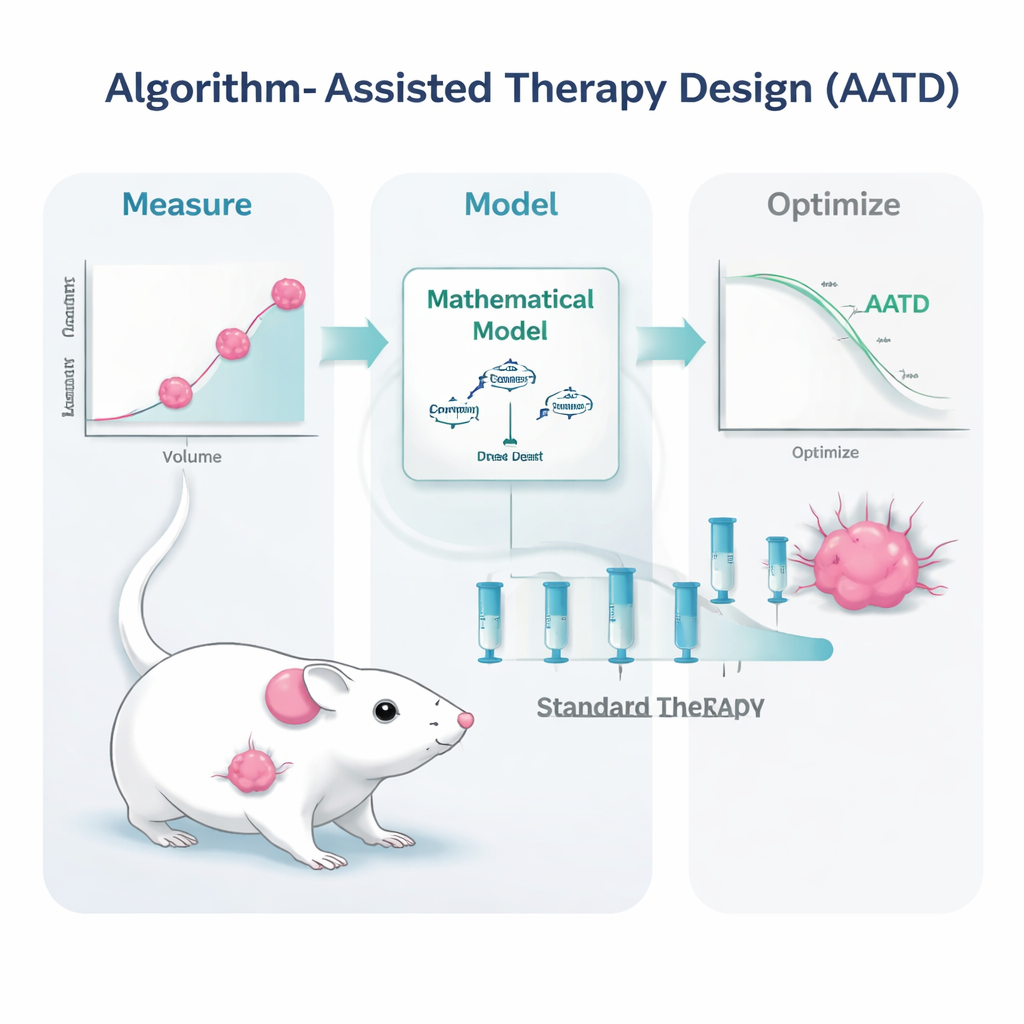
Vad detta kan betyda för framtida patienter
Även om detta arbete utfördes i möss är dess nyckelkomponenter—att mäta tumörstorlek, övervaka läkemedelsnivåer i blodet och köra datorbaserade modeller—redan möjliga hos mänskliga patienter med moderna bild- och laboratorieverktyg. Studien antyder att i stället för att fråga ”Vilken är standarddosen?” kan läkare en dag fråga ”Givet denna patients tumörbeteende och läkemedelshantering, vilken dos och tidpunkt fungerar bäst just nu?” Praktiska hinder kvarstår, såsom behovet av tätare mätningar och logistiken kring flexibel dosering, men budskapet är klart: kemoterapi behöver inte vara trubbig och enhetlig. Med hjälp av algoritmer kan den bli ett mer precist, anpassningsbart verktyg som ger patienter bättre chanser till långvarig kontroll av aggressiva cancerformer.
Citering: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
Nyckelord: individualiserad kemoterapi, trippelnegativ bröstcancer, algoritmstödd terapi, matematisk tumörmodellering, doxorubicin-dosering