Clear Sky Science · sv
Rumslig transkriptomik avslöjar molekylär heterogenitet och subtyp‑specifika terapeutiska målpunkter vid småcellig lungcancer
Varför denna lungcancerstudie är viktig
Småcellig lungcancer är en av de dödligaste formerna av cancer, drabbar främst personer med rökhistorik och återkommer ofta snabbt efter cytostatikabehandling. Läkare vet att inte alla småcellig lungcancer beter sig likadant, men de har saknat verktyg för att se hur olika cancercellstyper och immunceller är arrangerade i varje tumör. I den här studien användes en ny teknik som läser genaktivitet i tusentals små punkter över ett tumörsnitt och skapar en ”molekylär karta” för varje prov. Genom att kombinera detta med skräddarsydd datoranalys avslöjade forskarna dolda mönster som kan peka mot mer precisa, subtyp‑specifika behandlingar.
Kartläggning av tumörer på plats
Teamet analyserade tumörprover från 21 patienter med begränsad småcellig lungcancer som opererats innan de fått någon läkemedelsbehandling. Istället för att mala sönder vävnaden och förlora all rumslig information använde de rumslig transkriptomik: en teknik som mäter vilka gener som är aktiva vid många definierade punkter över ett vävnadssnitt. Varje punkt bevarar sin ursprungliga position, vilket gör det möjligt för forskarna att koppla genaktivitet till var cancerceller, normala celler och immunceller faktiskt befinner sig. De lade till två viktiga verktyg ovanpå detta: en ny ”Edgeindex”‑poäng för att kvantifiera hur djupt tumörceller tränger in i angränsande vävnad, och ett artificiellt neuralt nätverk — en form av maskininlärning — för att automatiskt markera vilka punkter som är tumör och vilka som inte är det.
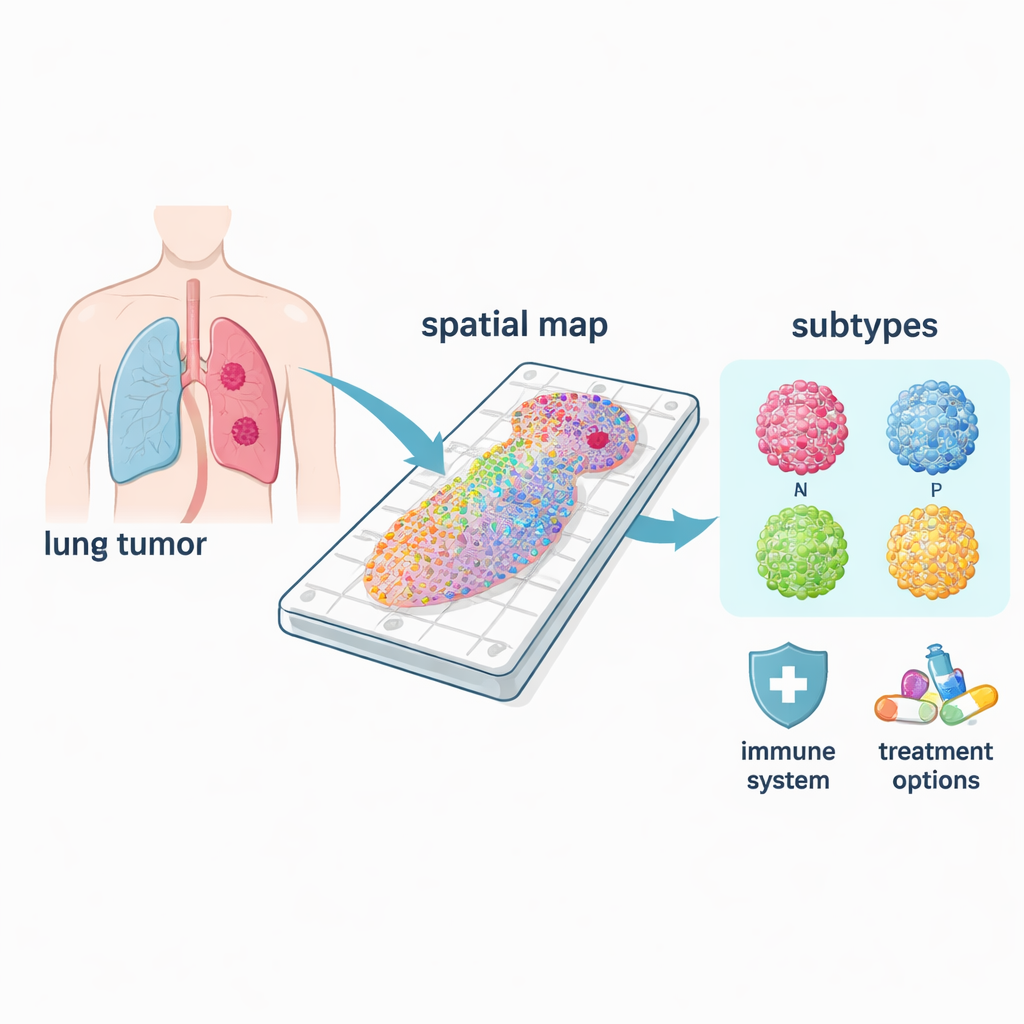
Olika cancertyper i en och samma sjukdom
Småcellig lungcancer är inte en enda sjukdom utan innefattar minst fyra stora molekylära subtyper, ofta kallade ASCL1, NEUROD1, POU2F3 och YAP1, efter nyckelgener som definierar dem. Med sina rumsliga kartor kunde forskarna se var varje subtyp dominerade inom tumörerna och hur deras biologiska egenskaper skilde sig åt. De vanliga ASCL1‑ och NEUROD1‑formerna kopplades starkt till program för celldelning, vilket stämmer med deras rykte som mycket proliferativa. POU2F3‑områden var i stället förknippade med immunrelaterade vägar, medan YAP1‑områden visade signaler relaterade till metabolism och vävnadsombyggnad — egenskaper som kan kopplas till spridning och behandlingsresistens. Eftersom dessa mönster är rumsligt upplösta kan metoden identifiera den verkliga ”drivande” subtypen i en blandad tumör, något som ofta missas av analys av homogeniserat material.
Den invaderande kanten och immunskiftet
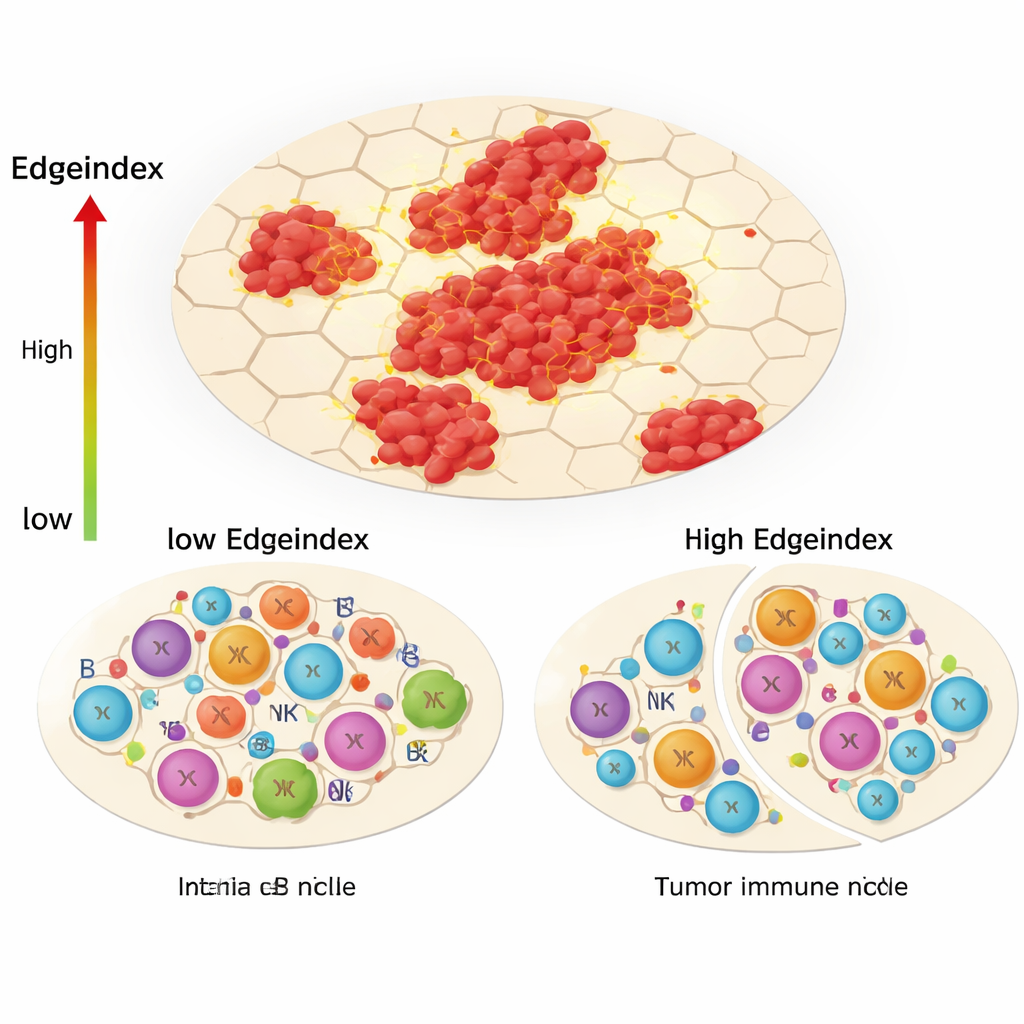
En av studiens centrala innovationer, Edgeindex, fångar hur mycket tumörceller blandar sig med omgivande icke‑tumörceller. Låga poäng återspeglar kompakta, välavgränsade tumörer, medan höga poäng indikerar utspridda öar och ojämna, invasiva gränser. Tumörer med hög Edgeindex var berikade för genprogram relaterade till extracellulär matrix, metastasering och celldöd. De visade också ett påtagligt förändrat immunlandskap: färre hjälpar‑T‑celler och andra adaptiva immunceller, men fler medfödda celler såsom vissa naturliga mördarceller och monocyter. Författarna tolkar detta som en ”immunologisk nischombyggnad”, där tumören tränger undan precisa, målinriktade immunsvar och lämnar kvar ett mindre effektivt, i huvudsak medfött försvar som inte kan kontrollera cancern fullt ut.
Gömd mångfald i och runt tumörer
Bortom subtyper och invasionsmönster visade de rumsliga data att både cancercellspopulationerna och deras omgivande mikromiljöer var interna mångfacetterade. Genom att klustra punkter inom varje tumör räknade teamet hur många distinkta genuttrycks‑”grannskap” som fanns i cancerregionerna och i den näraliggande icke‑tumörvävnaden. Högre mångfald inne i tumören kopplades till immunrelaterade vägar, medan vissa mönster i den omgivande vävnaden förknippades med cellcykelaktivitet och genetisk reglering. Forskarna undersökte också hur starkt olika regioner ”kommunicerade” med hjälp av kända signalmolekyler. Tumörer med intensivare kommunikation mellan regioner tenderade att uppvisa starkare immunsignaler, vilket förstärker bilden av att immunaktivitet och tumörtillväxt är tätt sammanflätade i rum.
Att följa tumörutveckling över tid
För att approximera hur tumörceller förändras när sjukdomen framskrider utförde teamet en så kallad ”pseudotids”‑analys som ordnar celler längs en utvecklingsbana baserat på deras genaktivitet. I flera prover identifierade de upprepade gånger en gen, UCHL1, som central i dessa trajektorier. Höga nivåer av UCHL1 sammanföll med stark cellcykelaktivitet i tumörpunkter, medan lägre nivåer stämde överens med immunsvar och celldöds‑vägar. Eftersom UCHL1 är ett nervtypat protein tidigare kopplat till aggressiva lungcancerformer stärker dessa fynd uppfattningen att det kan vara ett användbart läkemedelsmål, särskilt för de neuroendokrina‑lika celler som driver småcellig lungcancer.
Vad detta innebär för patienter
I klarspråk förvandlar den här studien platta mikroskoppreparat av småcellig lungcancer till rika, flerskiktade kartor som visar var olika cancercsubtyper sitter, hur aggressivt de invaderar, hur de kommunicerar med sin omgivning och hur immunsystemet svarar eller sviktar. Den nya Edgeindex‑poängen och kartläggningsmetoden framhäver vilka tumörer som är särskilt infiltrativa och vilka immunceller som finns eller saknas vid gränsen. Genom att koppla dessa rumsliga mönster till subtyp‑specifika svagheter — såsom läkemedel som riktar sig mot DLL3, BCL‑2, AURKA, IGF‑1R/PARP eller immunkontrollpunkter — tar arbetet fältet närmare att matcha varje patient med en skräddarsydd behandlingsstrategi. Även om dessa verktyg fortfarande behöver testas i större studier erbjuder de en ritning för mer precisa och potentiellt effektivare terapier i en cancerform som akut behöver bättre alternativ.
Citering: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Nyckelord: småcellig lungcancer, rumslig transkriptomik, tumörheterogenitet, tumörens immuna mikromiljö, precisionsterapi