Clear Sky Science · sv
Avkoda hjärnmetastaser vid epitelialt ovarialcancer: multimodal analys och potentiella biomarkörer
Varför denna forskning är viktig
Äggstockscancer är redan en allvarlig sjukdom, men hos ett litet antal kvinnor dyker den senare upp på en ännu skörare plats: i hjärnan. Dessa hjärnmetastaser är sällsynta men ofta dödliga, och läkare har fortfarande få sätt att förutsäga vem som löper risk eller hur de bäst ska behandlas. Denna studie följer den resan från bäcken till hjärna på molekylär nivå, med moderna DNA- och RNA-verktyg för att förstå hur ovarietumörer anpassar sig till hjärnan och för att peka ut tidiga varningssignaler som en dag kan vägleda mer skräddarsydd vård.
Från en vanlig cancer till ett sällsynt hjärnhot
Epitelial ovarialcancer är den dödligaste gynekologiska cancern i utvecklade länder. De flesta patienter svarar initialt på operation och kemoterapi, men omkring 80 procent får så småningom återfall och blir resistenta mot mediciner. Recidiv stannar oftast kvar i buken; endast en liten andel kvinnor utvecklar långt spridd sjukdom, exempelvis till hjärnan. När behandlingarna förbättras och kvinnorna lever längre finns dock mer tid för enstaka cancerceller att slå rot i hjärnan, och kliniker ser dessa metastaser oftare. När hjärnmetastaser väl uppträder sjunker den typiska överlevnaden till under ett år, vilket understryker behovet av att förstå hur och varför detta sker.
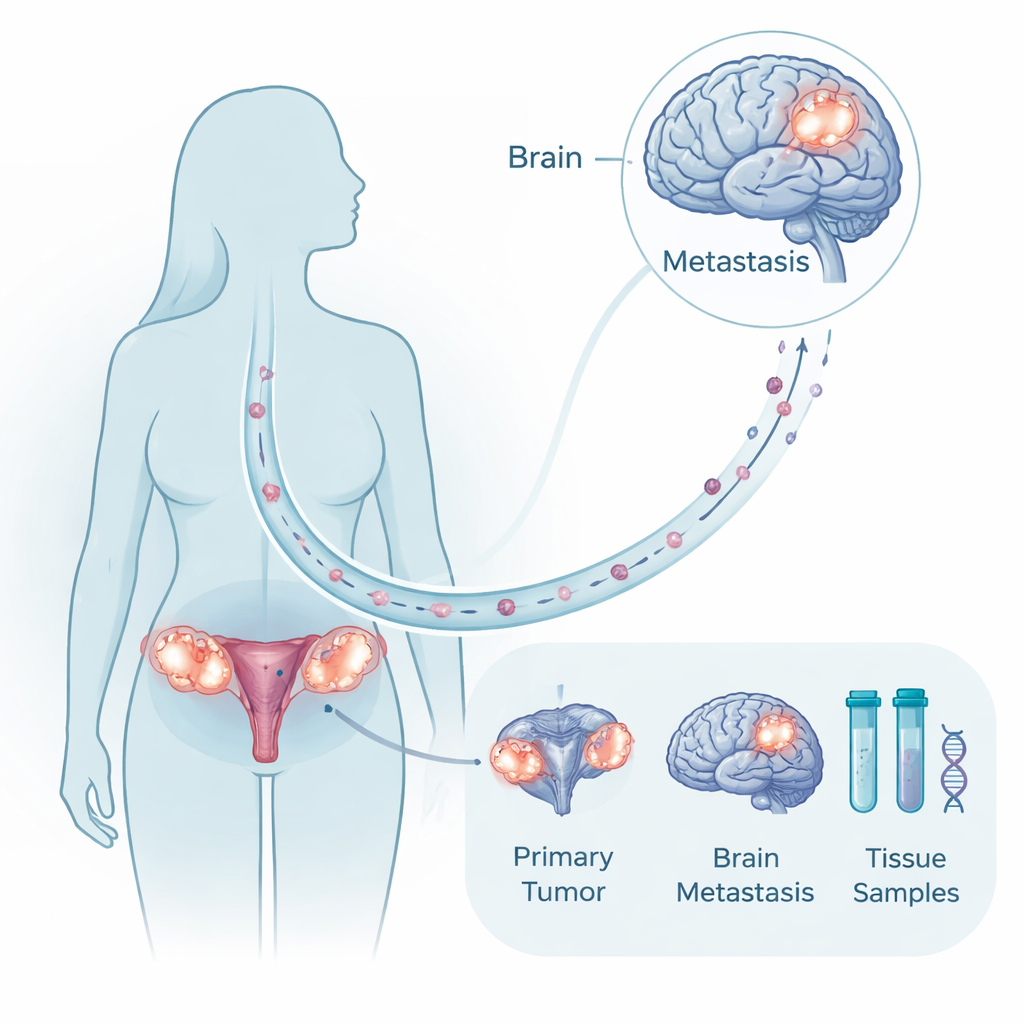
En sällsynt men värdefull vävnadssamling
Eftersom hjärnkirurgi inte är möjlig eller lämplig för många patienter är det ovanligt att ha tumörprover från både den ursprungliga ovarietumören och dess matchande hjärninsättning hos samma kvinna. Forskarna samlade precis denna typ av parade material från tio patienter behandlade under två decennier, tillsammans med jämförelseprover från frisk hjärna och äggstock samt från andra metastaser utanför hjärnan. De analyserade tumör-DNA för att leta efter mutationer och stora kromosomförändringar, och de profilerade RNA för att se vilka gener som var påslagna eller avstängda. Detta multimodala angreppssätt tillät dem att fråga om hjärntumörerna är helt nya sidogrenar eller nära besläktade kusiner till primärcancern, och vilka molekylära program som förändras när cellerna etablerar sig i hjärnan.
Genetisk stabilitet, men nytt beteende
DNA-analysen visade att de ursprungliga ovarietumörerna och deras matchande hjärnmetastaser var anmärkningsvärt lika. Båda bar många av samma cancerdrivande mutationer, särskilt i genen TP53, och delade ett övergripande “monoklonalt” ursprung, vilket betyder att hjärnlesionerna verkade härstamma från samma förfäderscancercell. Stora DNA-vinster och -förluster var något vanligare i hjärnlesionerna men inte överväldigande. Detta tyder på att det inte är förvärvet av en helt ny uppsättning mutationer som möjliggör hjärnspridning. Istället verkar det avgörande skiftet ske på nivån för genaktivitet: vilka instruktioner som läses från DNA och används av cancercellerna när de anpassar sig till hjärnans unika miljö.
Hur ovarietumörer lär sig att leva i hjärnan
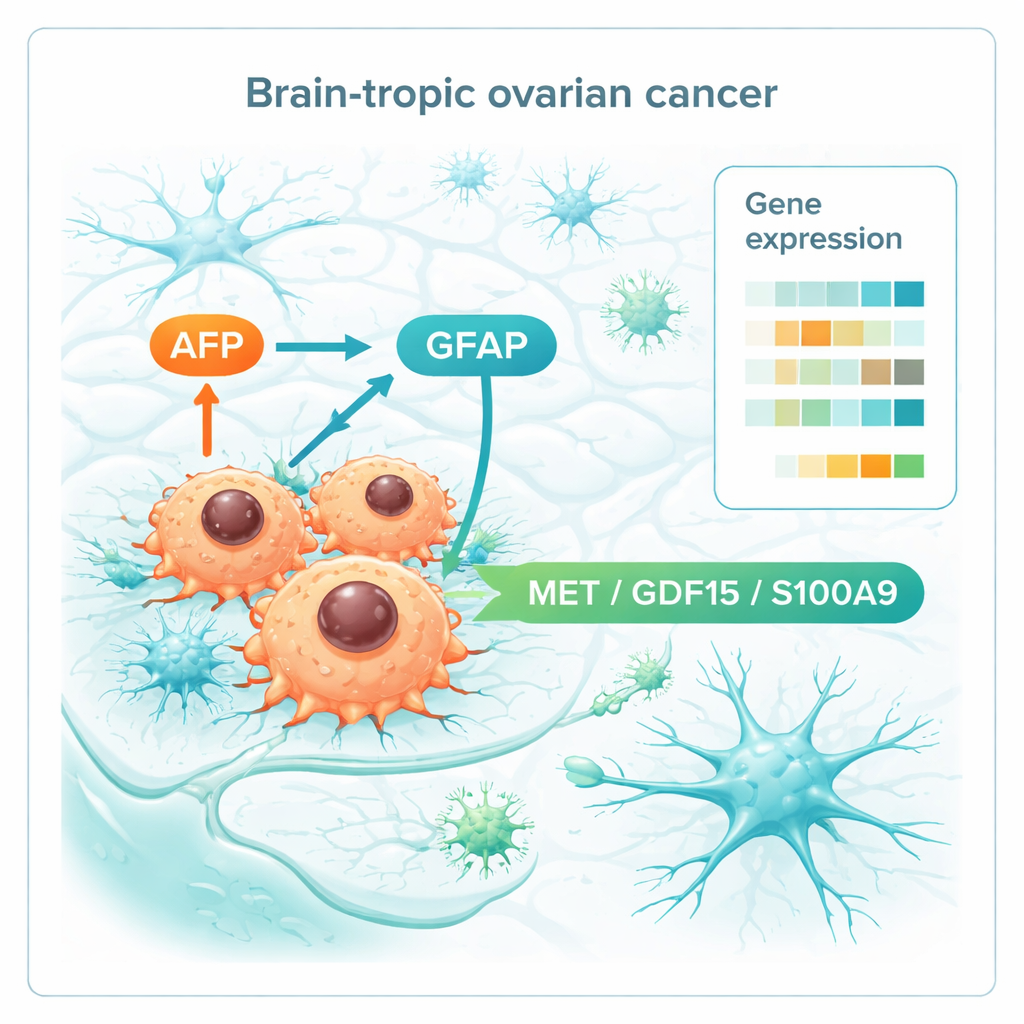
När teamet jämförde genaktivitet över alla vävnader framträdde en distinkt hjärnmetastatisk signatur. Hjärnlesionerna visade tecken på aggressiv tillväxt, med aktivering av cellcykelprogram drivna av välkända cancerregulatorer såsom MYC och E2F. De ändrade också proteiner som bildar och ombyggar vävnadens stomme, vilket hjälper cellerna att invadera och fästa i hjärnvävnaden. Slående nog aktiverades några gener kopplade till nerv- och gliaceller, vilket antyder att ovariecancerceller delvis efterliknar hjärnceller för att passa in. Bland de mest anmärkningsvärda var AFP, vanligtvis aktiv i fostret och i vissa tumörer, och GFAP, ett kännetecken för stödjeceller i hjärnan. Författarna identifierade också en liten uppsättning gener som redan var förhöjda i de primära ovarietumörerna hos kvinnor som senare utvecklade hjärnmetastaser men inte hos långtidsöverlevare utan hjärninvolvering. Detta ”premetastatiska” mönster innefattade immunmodulation, kommunikation med nervliknande signaler och förändringar i metabolismen.
Tidiga varningssignaler och molekylär dialog
Genom att gräva djupare fokuserade forskarna på molekyler som sitter på cellytan eller utsöndras, eftersom dessa är starka kandidater för blodtester eller läkemedelsmål. De identifierade tre aktörer — MET, GDF15 och S100A9 — som konsekvent var högre både i primärtumörer som var på väg att ge upphov till hjärnmetastaser och i själva hjärnmetastaserna. Dessa molekyler är involverade i cellrörelse, stress- och näringskänning samt formandet av den immunsvarande miljön, vilket tyder på att de hjälper ovariecancerceller att kommunicera med och omforma hjärnvävnad till sin fördel. Tillsammans med AFP och GFAP bildar de en kort lista över potentiella biomarkörer som en dag kunna flagga högriskpatienter eller peka på läkemedel som stör tumor–hjärn-kommunikationen.
Vad detta betyder för patienter
För närvarande kommer detta arbete inte omedelbart att förändra behandlingen, och författarna medger att deras patientgrupp är liten. Genom att visa att hjärnmetastaserande ovariecancer behåller stora delar av sitt ursprungliga genetiska innehåll samtidigt som den omkopplar hur generna används, lyfter studien fram nya sätt att upptäcka problem tidigt. Om framtida forskning bekräftar att markörer som AFP, GFAP, MET, GDF15 och S100A9 pålitligt signalerar en benägenhet att sprida sig till hjärnan, kan läkare komma att övervaka vissa patienter tätare, anpassa terapival eller pröva läkemedel som blockerar dessa vägar. I grunden börjar studien omvandla en skrämmande sen komplikation till en process som kan mätas, förstås och så småningom avbrytas.
Citering: Trozzi, R., Salvi, M., Karimi, M. et al. Deciphering brain metastasis in epithelial ovarian cancer: multimodal analysis and potential biomarkers. npj Precis. Onc. 10, 83 (2026). https://doi.org/10.1038/s41698-025-01206-y
Nyckelord: äggstockscancer, hjärnmetastaser, biomarkörer, genuttryck, precisionsonkologi