Clear Sky Science · sv
Målinriktade immunoterapier och nanomedicin för ovarialcancer: vägen framåt
Varför detta är viktigt för kvinnors hälsa
Ovarialcancer är en av de dödligaste cancerformerna som drabbar kvinnor, till stor del därför att den ofta upptäcks sent och behandlas med hårda, icke specifika läkemedel. Denna översiktsartikel undersöker hur en ny våg av immunbaserade behandlingar och mycket små magnetiska partiklar, så kallade magnetiska nanopartiklar, skulle kunna förändra vården av ovarialcancer — göra den mer exakt, mer personlig och i slutändan mer effektiv, med färre biverkningar.
Utmaningen att upptäcka och behandla ovarialcancer
Ovarialcancer växer ofta tyst. Tidiga symtom är vaga — uppblåsthet, lätt bukobehag — och vanliga bilddiagnostiska verktyg som ultraljud, CT och MRT kan missa små eller tidiga tumörer som gömmer sig djupt i buken. När många patienter väl får diagnosen har sjukdomen redan spridit sig inom bukhålan, vilket gör operation svårare och ökar risken för återfall. Cytostatika och målinriktade läkemedel kan hjälpa, men de skadar också frisk vävnad, och tumörer lär sig ofta att undkomma deras effekter. Dessa begränsningar har fått forskare att söka smartare sätt att både upptäcka och angripa ovarialcancerceller.
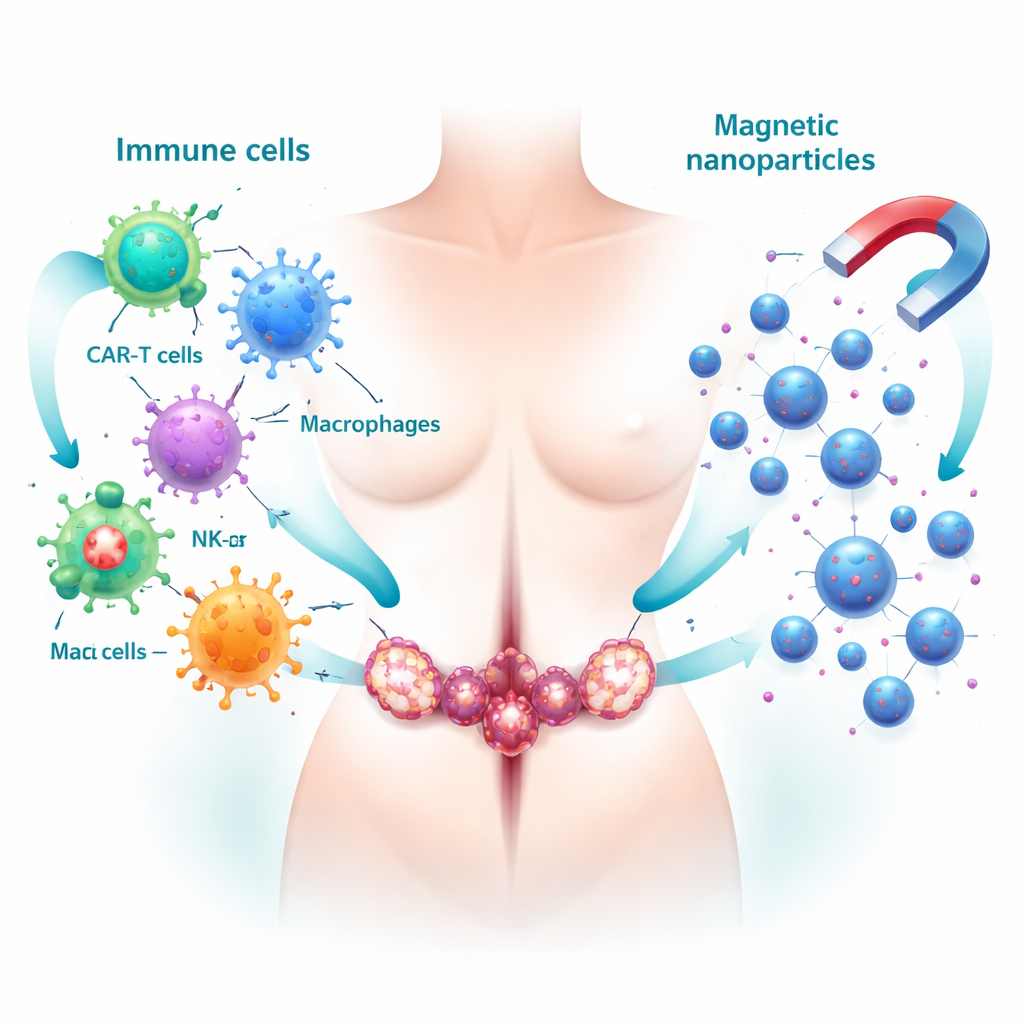
Lära immunsystemet att jaga tumörer
En huvudstrategi är att utnyttja kroppens egna försvar. Särskilt konstruerade T‑celler, kända som CAR‑T‑celler, designas i laboratoriet för att känna igen markörer som främst finns på ovarialcancerceller. När de återförs till patienten kan de söka upp och döda dessa celler med hög precision. Natural killer‑celler (NK‑celler) erbjuder en annan försvarslinje; de kan expandera eller genmodifieras för att bättre känna igen ovarialtumörer och fungerar ännu kraftfullare i kombination med målinriktade antikroppar eller checkpoint‑hämmare som tar bort ”bromsarna” på immunreaktionen. Samtidigt belyser artikeln tumörmiljöns mörka sida: tumörassocierade makrofager, en typ av immuncell som ofta omprogrammeras för att skydda snarare än bekämpa cancern. Att vända eller omutbilda dessa celler tillbaka till tumörbekämpare framstår som ett lovande sätt att få immunoterapi att fungera bättre.
Magnetiska nanopartiklar som intelligenta cancerverktyg
Den andra pelaren i översikten är nanomedicin, särskilt magnetiska nanopartiklar tillverkade av järnbaserade material. Eftersom de reagerar på magneter och syns tydligt på MRT, kan de fungera som små, styrbara verktyg inne i kroppen. Genom att belägga deras yta med molekyler som känner igen ovarialcancermarkörer kan dessa partiklar söka sig till tumörer och bära cytostatika direkt dit, vilket kraftigt ökar läkemedelsnivåerna i cancern samtidigt som friska organ skonas. Under ett alternerande magnetfält kan samma partiklar säkert värma en tumör till cirka 42–45 °C — tillräckligt varmt för att försvaga eller döda cancerceller och göra dem mer känsliga för standardbehandlingar, men inte så varmt att omgivande normal vävnad tar allvarlig skada.
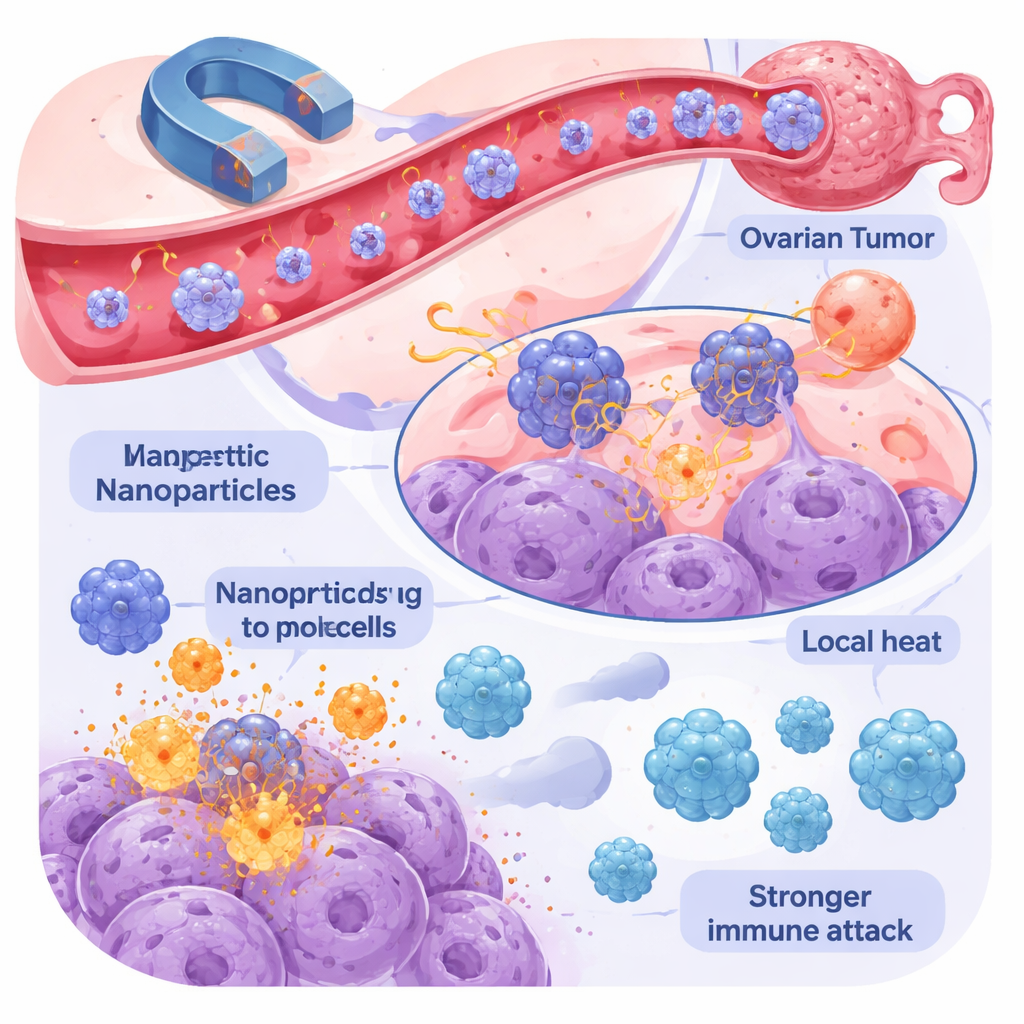
Kombinera värme, läkemedel och immunitet
Det verkliga intresset ligger i att kombinera immunoterapi med magnetisk nanomedicin. När magnetiska nanopartiklar levererar läkemedel, genererar värme eller bidrar till att avlägsna tumörer, får de cancerceller att dö på sätt som frigör ”fara‑signaler” och tumörfragment i den lokala miljön, vilket i praktiken förvandlar tumören till ett eget vaccin. Detta kan attrahera och aktivera T‑celler och NK‑celler, vilket gör det lättare för checkpoint‑hämmare och CAR‑baserade terapier att fungera. Forskare använder också nanopartiklar för att föra immunstimulerande molekyler och antikroppar direkt in i tumören, vilket ökar deras lokala koncentration samtidigt som systemiska biverkningar minskar. Tidiga djurstudier visar kraftigare tumörkrympning, färre återfall och starkare infiltration av immunceller när dessa metoder kombineras.
Hinder, säkerhet och vägen framåt
Trots dessa framsteg återstår utmaningar. Ovarialtumörer är fläckiga och spridda i buken, vilket gör jämn fördelning av nanopartiklar svår, och icke‑nedbrytbara partiklar kan ansamlas i organ som levern om de inte är noggrant utformade. Tät, ärrliknande vävnad runt tumörer kan hindra djup penetration. Artikeln går igenom tekniska lösningar — såsom biologiskt nedbrytbara beläggningar, ”själv” cellmembrans‑kamouflage och enzymer som luckrar upp tumörbarriärer — som förbättrar säkerhet, målinriktning och eliminering. Den understryker också vikten av att skräddarsy behandlingar efter varje patients genetik och immunsprofil samt att använda avancerad bilddiagnostik för att följa var nanopartiklarna hamnar och hur väl de fungerar.
Vad detta kan innebära för patienter
I praktiska termer pekar arbetet som beskrivs i denna översikt mot en framtid där ovarialcancer upptäcks tidigare och behandlas mildare men mer effektivt. Magnetiska nanopartiklar skulle kunna styra läkemedel och värme exakt dit de behövs, samtidigt som immunbaserade terapier koordinerar en varaktig, kroppsomfattande attack mot eventuellt kvarvarande cancerceller. Om kommande kliniska prövningar bekräftar de löften som setts i laboratorie‑ och djurstudier kan kvinnor med ovarialcancer få nytta av behandlingar som är mer målinriktade, mer personliga och långt mindre plågsamma än dagens standardbehandlingar.
Citering: Li, Y., Dou, J., Fu, Y. et al. Targeted immunotherapies and nanomedicines for ovarian cancer: the way forward. npj Precis. Onc. 10, 80 (2026). https://doi.org/10.1038/s41698-025-01204-0
Nyckelord: ovarialcancer, immunoterapi, nanomedicin, magnetiska nanopartiklar, målinriktad läkemedelsleverans