Clear Sky Science · sv
Metoder för randomiserad, blindad, kontrollerad utvärdering av föreslagna sjukdomsinterventioner i multilaboratoriska, prekliniska utvärderingsnätverk
Varför detta spelar roll för vardagshälsan
Många lovande medicinska behandlingar ser effektiva ut i djurstudier men misslyckas sedan i stora, kostsamma kliniska prövningar. Denna artikel visar, i konkret detalj, hur forskare kan utforma om de tidiga djurförsöken så att resultaten blir mer tillförlitliga och mer sannolikt förutsäger vad som händer hos verkliga patienter—med stroke som fallstudie. 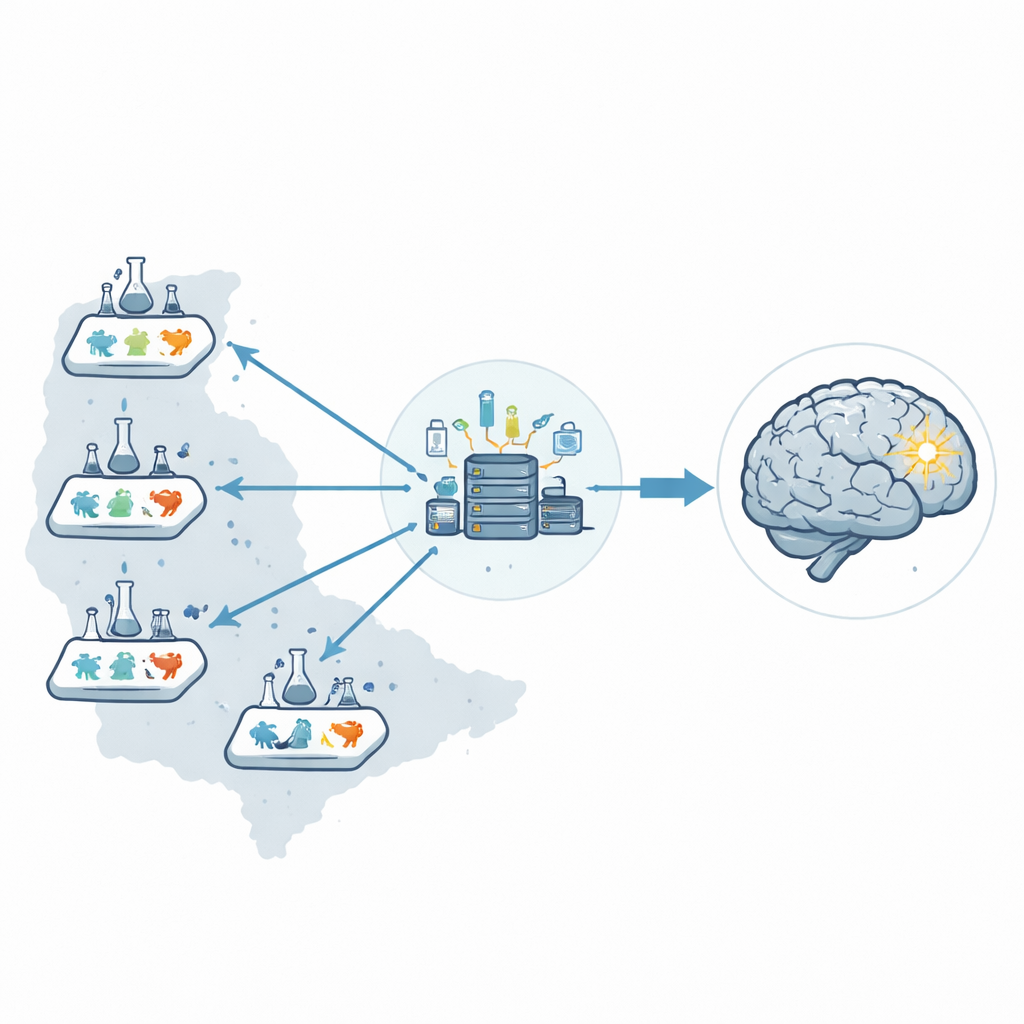
Bygga ett nätverk istället för ett enskilt labb
I stället för att förlita sig på ett laboratorium skapade forskarna ett prekliniskt nätverk med sex laboratorier i hela USA, kallat Stroke Preclinical Assessment Network. Ett centralt koordineringscenter hanterade hela operationen: skickade kodade läkemedelsflaskor, tilldelade behandlingar slumpmässigt, tog emot all data och körde statistiken. Genom att separera dessa roller från de personer som utförde kirurgi eller bedömde utfall minskade de risken att mänskliga förväntningar subtilt påverkar resultaten.
Att omsätta rättvisa och maskering i praktiken
För att efterlikna reglerna i en bra klinisk prövning skrevs varje djur in, märktes och följdes från det ögonblick det anlände till ett laboratorium. Behandlingar doldes i identiska flaskor så att kirurger inte kunde skilja verkliga läkemedel från placebobehandlingar medan de framkallade stroke och gav terapi. En strukturerad randomiseringsplan säkerställde att hanar och honor, olika strokemodeller och samtliga sex platser bidrog jämnt till varje behandlingsgrupp. Även om ett djur dog eller ett ingrepp misslyckades så behölls det i registret så att förluster inte tyst kunde ignoreras, vilket hjälpte till att undvika dolda snedvridningar.
Testa behandlingar i realistiska strokemodeller
Nätverket använde fem olika gnagarmodeller som tillsammans fångade viktiga aspekter av mänsklig stroke, inklusive ålder, högt blodtryck och kostinducerad fetma. Stroke framkallades på samma sätt över platser genom att tillfälligt blockera en större hjärnartär och sedan återställa blodflödet—liknande moderna procedurer för borttagning av proppar hos människor. Djur fick en av sex kandidatbehandlingar med skyddande effekt eller en matchande kontroll. Teamet följde dem sedan med enkla rörelsetester, såsom hur de svängde i ett hörn eller gick på ett galler, och med hjärnavbildningar för att mäta skadans storlek över 30 dagar.
Blindad poängsättning, delade data och smart statistik
För att hålla bedömningarna opartiska spelades beteendetester in på video och laddades upp till ett centralt arkiv. Dessa videor, befriade från identifierande information, skickades till tränade bedömare vid andra laboratorier som poängsatte dem utan att veta vilken behandling djuret fått eller var det testats. Magnetresonansbilder kördes genom en automatiserad analysrutin som segmenterade hjärnan och skadeområdet med minimal mänsklig inblandning. Alla resultat matades in i en multiarmad, multistegs statistisk design som gjorde det möjligt att testa flera behandlingar parallellt: svaga eller klart ineffektiva kandidater kunde plockas bort tidigt medan lovande fortsatte till senare faser. 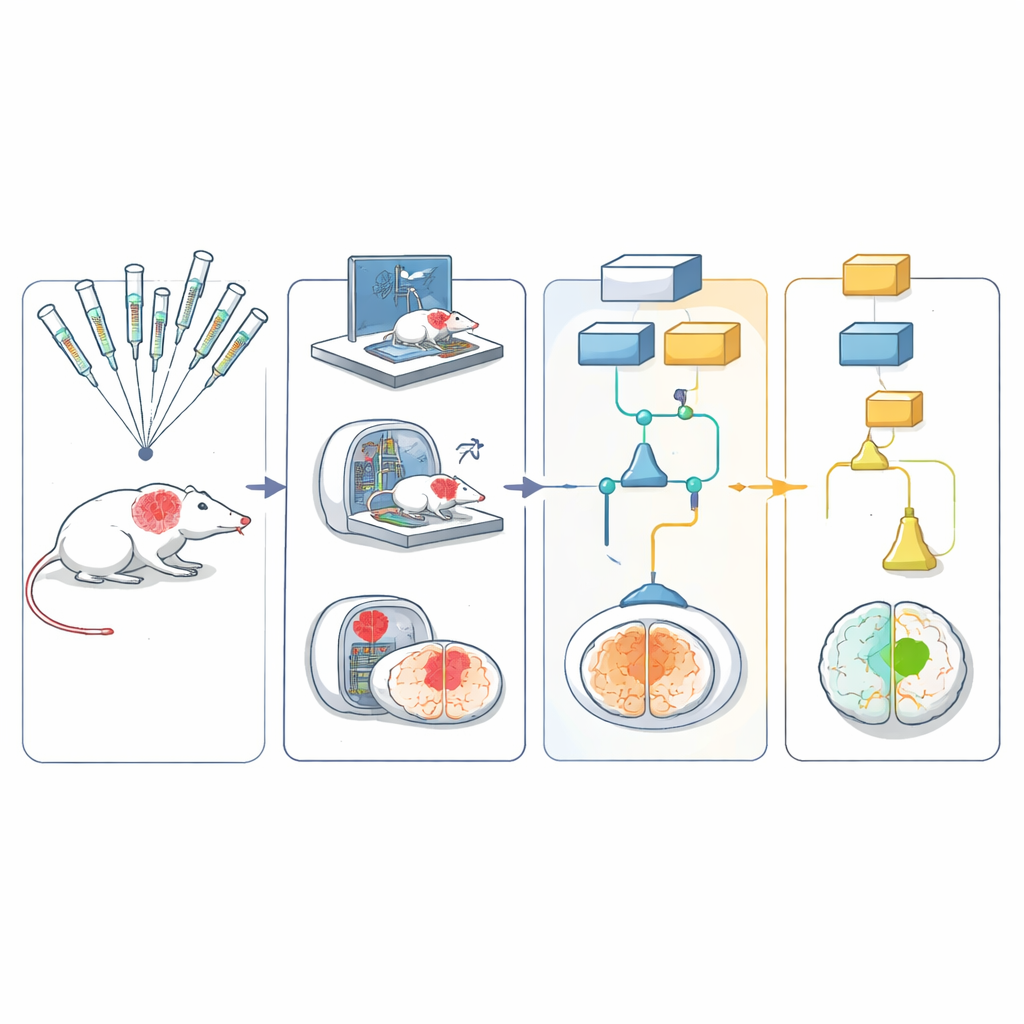
Vad resultaten visade om stroketerapier
Över fyra stadier och 2 615 djur visade systemet sig fungera även under störningarna från COVID-19-pandemin. Metoderna höll konsekvent behandlingsgrupperna balanserade, minimerade doseringsfel och visade förbättrad datakvalitet i takt med att platserna klättrade på inlärningskurvan. I slutändan avfärdades fem av sex behandlingar, medan en—urat, en fria radikalfångare—uppfyllde det förplanerade tröskelvärdet för nytta. Samtidigt avslöjade arbetet begränsningar hos vissa populära modeller, såsom mycket höga dödstal hos åldrade möss, vilket tyder på att de kanske inte är praktiska eller realistiska för framtida studier.
Större bild: en mall för mer tillförlitlig preklinisk vetenskap
För en lekmannaläsare är huvudbudskapet att hur vi testar behandlingar i djur är lika viktigt som vad vi testar. Genom att införa skyddsmekanismerna från moderna kliniska prövningar—randomisering, blindning, full redovisning av varje subjekt och noggrann statistik—i djurforskning visar detta nätverk att tidiga studier kan vara både mer rigorösa och mer effektiva. Den detaljerade manual de tillhandahåller kan anpassas till andra sjukdomar och erbjuder en väg mot laboratoriefynd som står sig vid replikation och ger läkare, patienter och finansiärer större förtroende för att en behandling verkligen har en chans att fungera i kliniken.
Citering: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Nyckelord: stroke, prekliniska prövningar, djurmodeller, forskningsnoggrannhet, multicenterstudier