Clear Sky Science · sv
PiggyBac-medierad transgenes och CRISPR–Cas9‑knockout hos den större vaxmott, Galleria mellonella
En liten larv med stor medicinsk potential
Tänk dig att testa nya antibiotika eller studera farliga infektioner utan att använda möss eller andra däggdjur. Larverna av den större vaxmott, Galleria mellonella, framträder som ett kostnadseffektivt och etiskt tilltalande alternativ för sådana experiment. Denna studie visar hur forskare tagit ett stort steg framåt genom att ge dessa larver samma typ av genetiska verktyg som gjorde fruktflugor och zebrafiskar så kraftfulla för biomedicinsk forskning.
Varför denna insekt är viktig för människors hälsa
Galleria mellonella‑larver efterliknar förvånansvärt väl hur människokroppen reagerar på mikrober. De kan hållas vid 37 °C — vår kroppstemperatur — och kan infekteras med ett brett spektrum medicinskt viktiga bakterier och svampar. När de blir sjuka mörknar deras kroppar genom en process som kallas melanisering, vilket ger forskare en synlig indikator på hälsotillståndet. Eftersom de är ryggradslösa undviker de många lagliga och etiska hinder som följer med arbete på ryggradsdjur, och de är billiga att föda upp i stora mängder. Larverna har dessutom visat sig kunna bryta ner vanliga plaster, vilket pekar på användningsområden även inom miljöforskning.
Den saknade genetiska verktygslådan
Trots dessa fördelar har vaxmotslarver saknat de sofistikerade genetiska knep som finns i klassiska laboratorieorganismer. Under det senaste decenniet har flera grupper sekvenserat mottens genom och katalogiserat dess aktiva gener och proteiner, men forskare kunde fortfarande inte enkelt slå av eller på gener eller lägga till användbara markörer. Denna brist har begränsat vad som gått att göra med modellen — till exempel att bygga djur som lyser upp vid infektion eller att ta bort specifika gener för att testa deras roll i immunitet. Den aktuella artikeln tar itu med detta genom att anpassa två kraftfulla genredigeringssystem, kända som PiggyBac och CRISPR–Cas9, för användning i Galleria mellonella.
Att skapa lysande rapporterlarver
Forskarna studerade först tidpunkten för tidig embryonal utveckling hos motten och fann ett ungefär sex timmar långt fönster efter att äggen lagts då alla delande kärnor fortfarande delar ett gemensamt inre. Genom att injicera DNA under denna period kan nytt genetiskt material föras in i alla senare vävnader, inklusive framtida spermier och ägg. Med detta fönster införde teamet DNA‑konstruktioner baserade på transposonen PiggyBac, ett "klipp‑och‑klistra"‑element som sätter in stora DNA‑stycken i genomet. Efter att ha testat olika hjälpplasmider identifierade de en version som bar ett hyperaktivt PiggyBac‑enzym och som framgångsrikt gav upphov till transgena linjer. Dessa larver uttryckte gröna och röda fluorescerande proteiner i olika vävnader, och DNA‑analys visade att den genetiska kassetten landade i ett ofarligt avsnitt mellan infödda gener.
Att följa celler och slå ut gener
Därefter skapade författarna mer specialiserade rapportlinjer. En konstruktion märkte ett strukturprotein kallat tubulin med grön fluorescens för att belysa cellens inre skelett, medan en annan fäste en röd markör vid ett histonprotein som lindas runt DNA i cellkärnan. Dessa linjer lyste i karaktäristiska mönster i tarm, fettkropp, spolkörtlar och andra vävnader, vilket gjorde det möjligt för forskarna att visualisera cellstrukturer i levande eller fixerade larver. För att gå bortom att lägga till gener och istället inaktivera dem vände sig teamet till CRISPR–Cas9. De injicerade förmonterade CRISPR protein–RNA‑komplex som riktade in sig mot den gröna fluorescensmarkören i embryon som redan bar rapportkassetten. Många av avkommorna visade partiell eller komplett förlust av det gröna signalen samtidigt som den röda ögonfluorescensen bibehölls, och DNA‑sekvensering bekräftade små insertioner och deletioner vid den avsedda CRISPR‑skärplatsen.
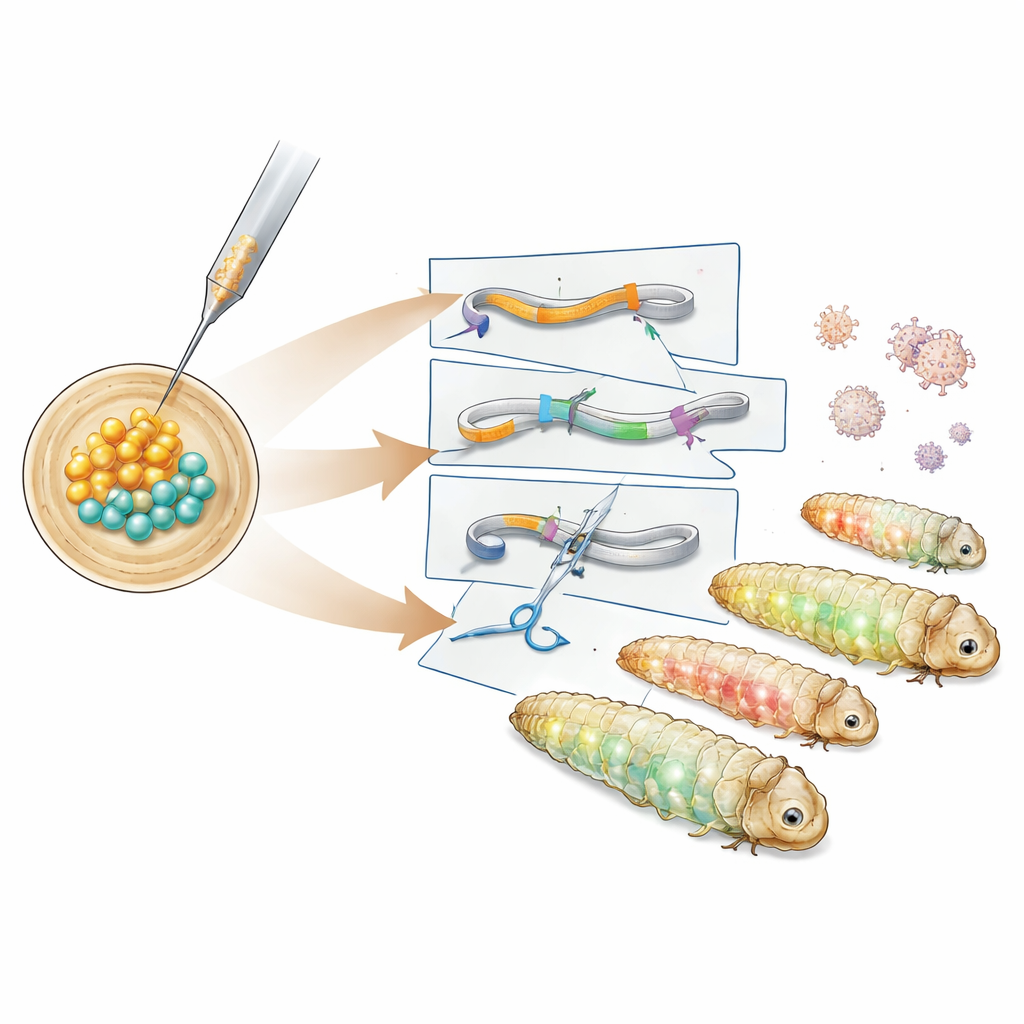
Från tekniskt framsteg till praktisk påverkan
Även om effektiviteten för både PiggyBac och CRISPR i dessa möss fortfarande är måttlig jämfört med vissa andra insekter, beskriver författarna tydliga vägar för förbättring genom att justera promotorer, enzymvarianter och injektionstekniker. Även i sin nuvarande form är verktygslådan tillräckligt kraftfull för att generera stabila linjer som visualiserar viktiga cellkomponenter eller bär riktade genknockouter. För icke‑specialister är huvudpoängen att Galleria mellonella nu kan manipuleras nästan lika flexibelt som bättre kända försöksdjur. Det innebär att forskare kan bygga larver som rapporterar om infektioner, modellera aspekter av mänskliga sjukdomar eller testa nya läkemedel på sätt som är snabbare, billigare och mer humana, med potential att minska beroendet av däggdjursmodeller inom infektionsbiologi och närliggande fält.
Citering: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Nyckelord: Galleria mellonella, modell för infektion hos ryggradslösa, genetisk ingenjörskonst, PiggyBac‑transgenes, CRISPR‑knockouter