Clear Sky Science · sv
Rikta in sig på canceruttryckt EGFR med en humaniserad monoklonal antikropp
Att hitta cancerns dolda flaggor
Cancerbehandlingar kämpar ofta med att finna balans mellan att angripa tumörceller och skona frisk vävnad. Denna artikel beskriver en ny laboratorieframställd antikropp, kallad A10, som kan skilja cancerösa celler som bär en särskild form av en tillväxtsignalsreceptor från normala celler. Genom att rikta in sig på en form som framträder främst när receptorn är ändrad eller överuttryckt på tumörceller öppnar A10 dörren för terapier som både är starka och mer selektiva än många nuvarande alternativ.
Varför denna tillväxtbrytare spelar roll
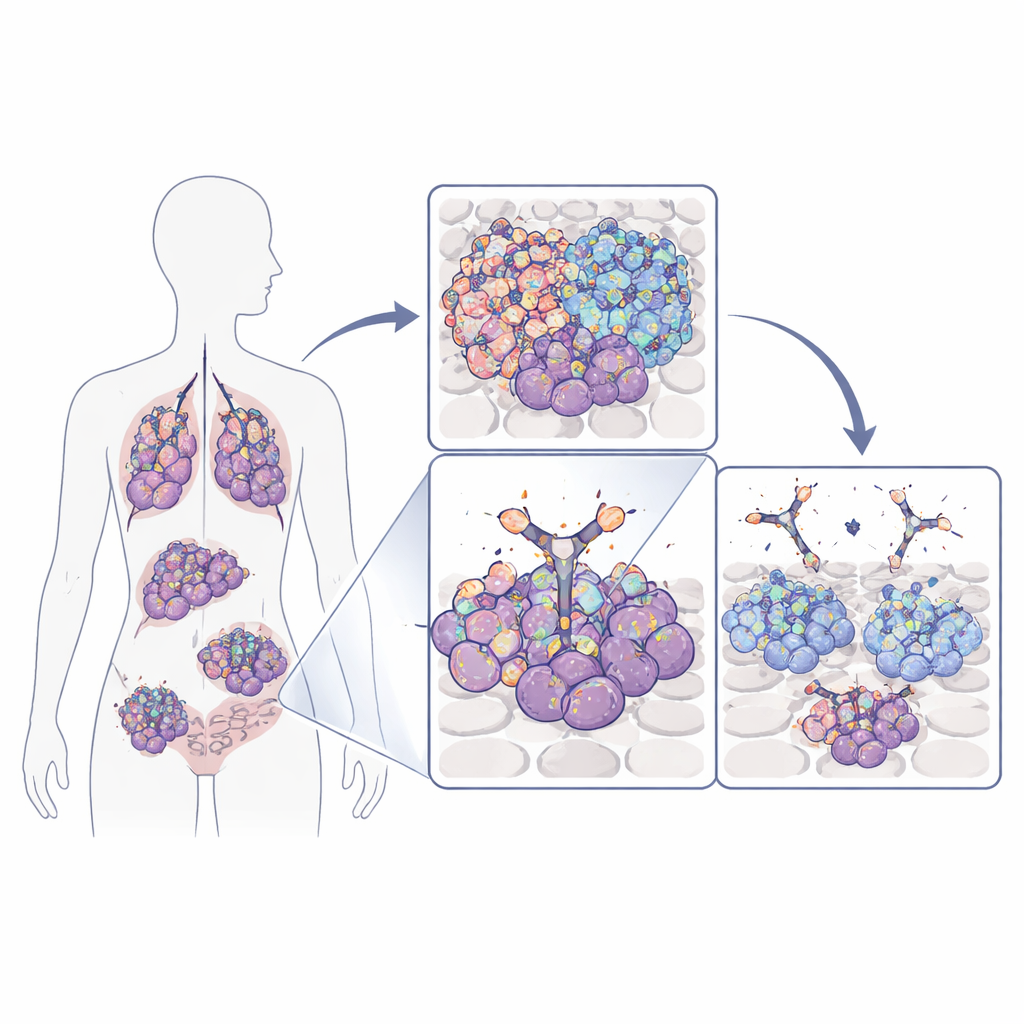
Många tumörer, inklusive aggressiva former i hjärnan, lungan, bröstet och tjocktarmen, är beroende av ett ytprotein kallat epidermal tillväxtfaktorreceptor (EGFR) för att växa och överleva. Tumörceller kan öka denna receptor genom att antingen amplifiera dess gen, mutera den eller producera en förkortad, ständigt aktiv variant känd som EGFRvIII. Standardläkemedel som blockerar EGFR träffar ofta både cancerceller och normal vävnad eftersom de känner igen delar av receptorn som finns överallt. Forskargruppen bakom denna studie fokuserade istället på en liten slinga av EGFR som blir tydligt exponerad främst på cancerceller—antingen därför att EGFR finns i abnormt höga mängder eller eftersom receptorn är trunkerad i EGFRvIII. Denna slinga fungerar som en cancer‑specifik ”flagga” som i princip kan riktas in på ett betydligt säkrare sätt.
Att göra en musantikropp till ett mänskligt läkemedel
Forskarna hade tidigare upptäckt en musantikropp, 40H3, som kände igen denna exponerade slinga på canceruttryckt EGFR. Musantikroppar kan dock framkalla immunsvar vid upprepad administrering till patienter. För att övervinna detta använde gruppen proteiningenjörstekniker för att grafta de avgörande bindningssegmenten från 40H3 på humanantibodyramverk och genererade fjorton ”humaniserade” kandidater plus ett kimeriskt referensmolekyl. När de testade dessa varianter på cancerceller som överproducerar EGFR band tre versioner särskilt väl, och en—A10—stod ut som den starkaste bindaren samtidigt som den ignorerade normala celler med måttliga EGFR‑nivåer. Över ett brett panel av tumörcellinjer med olika EGFR‑mutationer och kopietal visade A10 konsekvent högre bindning än den ursprungliga musantikroppen och upprätthöll en stark preferens för maligna celler.
Att se hur antikroppen griper sitt mål
För att förstå varför A10 är så selektiv löste gruppen en högupplöst 3D‑struktur av den aktiva delen av antikroppen bunden till EGFR‑slingan. Slingan viker sig till en tät hårnålshårstruktur stabiliserad av en disulfidbindning, och A10 omsluter denna form i en fåra mellan sina två armar, med många laddade kontakter som låser den på plats. Jämförelse av denna struktur med kända former av hela EGFR‑molekylen avslöjade en viktig insikt: i både den inaktiva ”tethered” formen och den aktiva dimerformen av normal EGFR ligger slingan till största delen dold eller delvis skärmad av närliggande domäner. Det innebär att A10 inte lätt når sitt bindningsställe på typiska receptorer med måttligt uttryck. I kontrast, i den cancer‑specifika EGFRvIII‑varianten saknas frontdelen av receptorn, vilket lämnar slingan starkt exponerad och tillgänglig. Data tyder på att A10 främst känner igen EGFR under vissa övergångsformer och i överfulla eller trunkerade varianter som förekommer i preferens på tumörceller.
Att beväpna antikroppen för att döda tumörceller
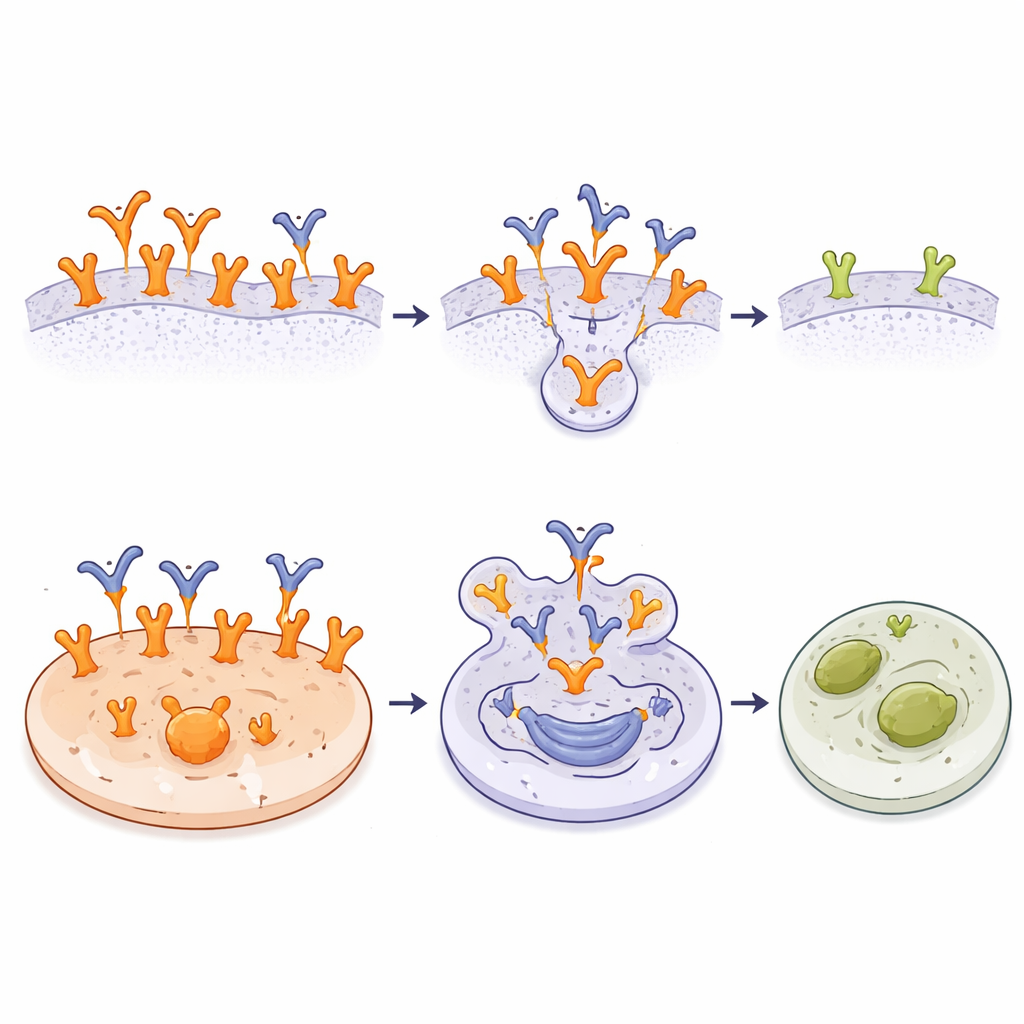
Att känna igen en tumörspecifik flagga är användbart i sig, men forskarna gick vidare genom att göra A10 till ett antikropp‑läkemedelskonjugat (ADC). De kopplade kemiskt en potent cell‑dödande förening, monometyl auristatin E (MMAE), till A10 med en länk som kan klyvas inne i celler. Detta A10‑MMAE ADC band till cancerceller lika väl som den okonjugerade antikroppen. I laboratorietester över många cellinjer var ADC:n mest effektiv mot tumörer med mycket höga EGFR‑nivåer eller EGFRvIII, där A10 hade rikligt med bindningsställen. I dessa celler räckte mycket små mängder av konjugatet för att utlösa celldöd. Tumörlinjer med färre A10‑mål eller med inneboende resistens mot MMAE påverkades mindre, och normala fibroblastceller med vildtyp‑EGFR förblev oskadda trots att de var känsliga för fritt MMAE. Resultaten visar att kombinationen av selektiv bindning och intern läkemedelsfrigöring kan fokusera toxiciteten skarpt mot cancerceller.
Vad detta kan betyda för framtidens cancervård
Enkelt uttryckt visar detta arbete att det är möjligt att bygga en antikropp som ”ser” EGFR endast när den ser ut och beter sig som en cancerdrivande receptor, samtidigt som den i stort sett ignorerar dess vardagliga form på frisk vävnad. Genom att kartlägga exakt hur A10 greppar en dold slinga på EGFR och visa att ett A10‑baserat läkemedelskonjugat effektivt kan döda receptor‑rika tumörceller men skona normala celler ger studien en stark grund för utveckling av säkrare, högt riktade terapier. Om dessa fynd kan översättas till patienter kan framtida behandlingar baserade på A10 leverera kraftfulla läkemedel direkt till EGFR‑beroende cancerformer samtidigt som resten av kroppen i stor utsträckning lämnas oberörd.
Citering: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Nyckelord: EGFR, antikroppsläkemedelskonjugat, riktad cancerterapi, glioblastom, EGFRvIII