Clear Sky Science · sv
Strukturella och mekanistiska insikter i α2β1- och α5β1-integrinmålinriktning av bioingenjörsframställda extracellulära vesiklar härstammande från lungcancerceller
Cancerens dolda budbärare
Lungcancer upptäcks ofta sent, när behandlingsalternativen är begränsade. Ett lovande sätt att bekämpa sjukdomen är att leverera läkemedel enbart till cancerceller och därigenom skona frisk vävnad. Denna studie undersöker ett mycket litet, naturligt transportsystem—extracellulära vesiklar, eller EV:er—som cancerceller redan använder för att skicka meddelanden. Genom att omkonstruera dessa vesiklar med en kort målsökande tagg visar forskarna hur de kan fästa vid specifika dockningsställen på tumörceller, vilket banar väg för mer precisa och mindre toxiska cancerterapier.
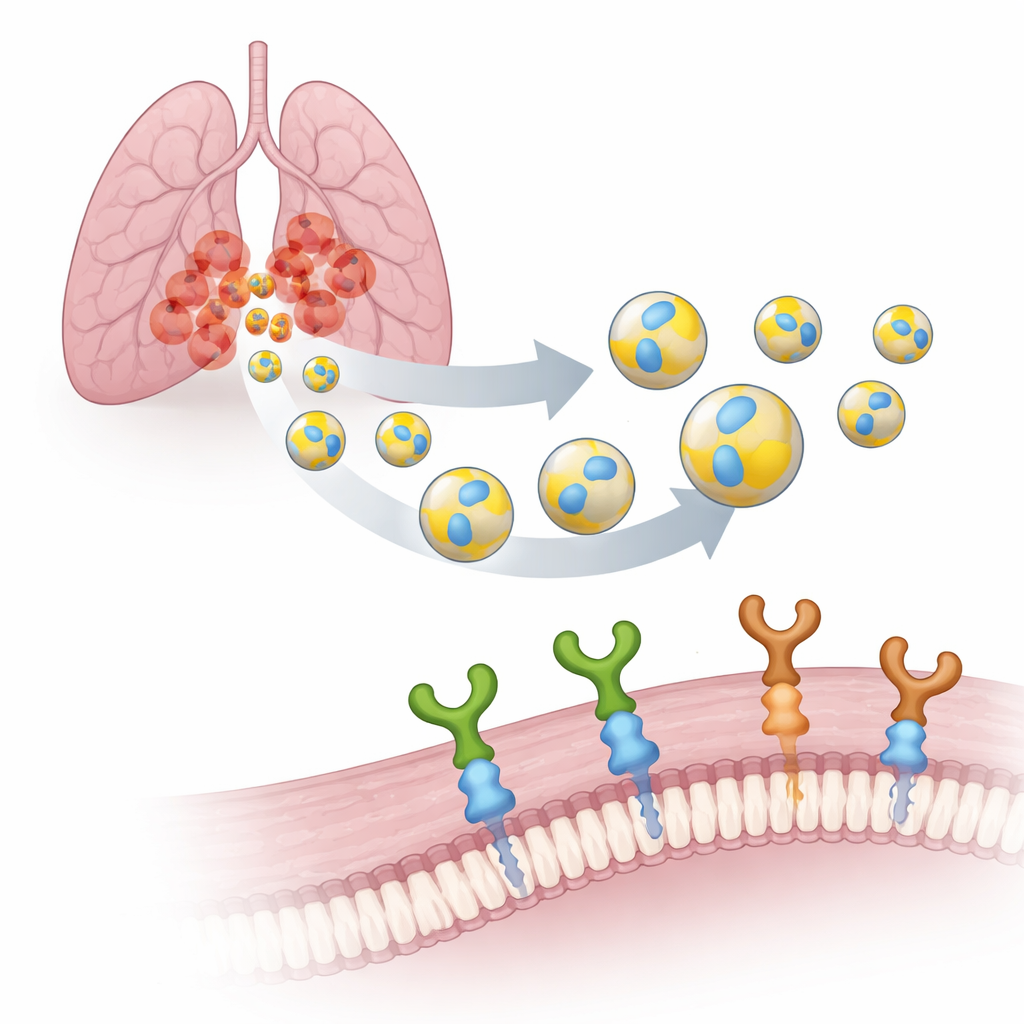
Förvandla naturliga paket till smarta kurirer
Varje cell i vår kropp avger EV:er: nanoskaliga bubblor omslutna av ett membran, lite som mikroskopiska tvålbubblor. Eftersom de är skapade av våra egna celler är EV:er biologiskt nedbrytbara, tar sig lätt igenom biologiska barriärer och är mindre benägna att framkalla biverkningar än syntetiska bärare. Teamet fokuserade på EV:er producerade av humana lungcancerceller (A549) och dekorerade deras yta med en liten sju-byggstenstagg kallad PTHTRWA. Tidigare experiment visade att denna tagg får EV:er att söka sig till lungcancerceller hos möss, binder betydligt starkare till tumörceller än till normala lungceller samtidigt som den endast är svagt toxisk.
Hitta rätt dockningsportar på tumörceller
För att omvandla dessa taggade vesiklar till verkligt riktade verktyg behövde forskarna identifiera vilka “portar” på cancercellerna de känner igen. De undersökte två närbesläktade ytreceptorer, α2β1- och α5β1-integriner. Dessa är molekylära gripkrokar som hjälper celler att fästa vid omgivningen och att skicka signaler inåt. I lungtumörer är α5β1 starkt kopplat till aggressivt beteende, spridning och sämre överlevnad, medan α2β1 har associerats med resistens mot kemoterapi. Med en känslig teknik kallad ytplasmonresonans jämförde teamet hur starkt PTHTRWA-dekorerade EV:er binder till båda integrinerna. De fann att vesiklar utan tagg knappt interagerade, medan taggade EV:er bildade täta, stabila komplex med båda receptorerna under nära-fysiologiska förhållanden.
Zooma in på det molekylära omfamningen
För att förstå vad som händer atom för atom när taggen möter integrinerna använde forskarna datorsimuleringar. De byggde tredimensionella modeller av taggen bunden till nyckelregioner på integrinerna och lät systemen utvecklas i virtuellt vatten under hundratals nanosekunder. Beräkningarna visade att PTHTRWA sitter tätt i en grund fåra på α2β1-receptorn och bildar ett nätverk av vätebindningar och hydrofoba kontakter som stabiliserar komplexet. Avgörande var att bindningen gynnade en mer “öppen” form av receptorn—dess högaffinitets-, signalberedda tillstånd—över det “stängda” vilotillståndet. När de testade lätt modifierade versioner av taggen såg de att små kemiska förändringar i ena änden subtilt kan omforma hur peptiden ligger i fåran och hur starkt den föredrar det ena integrinet framför det andra.
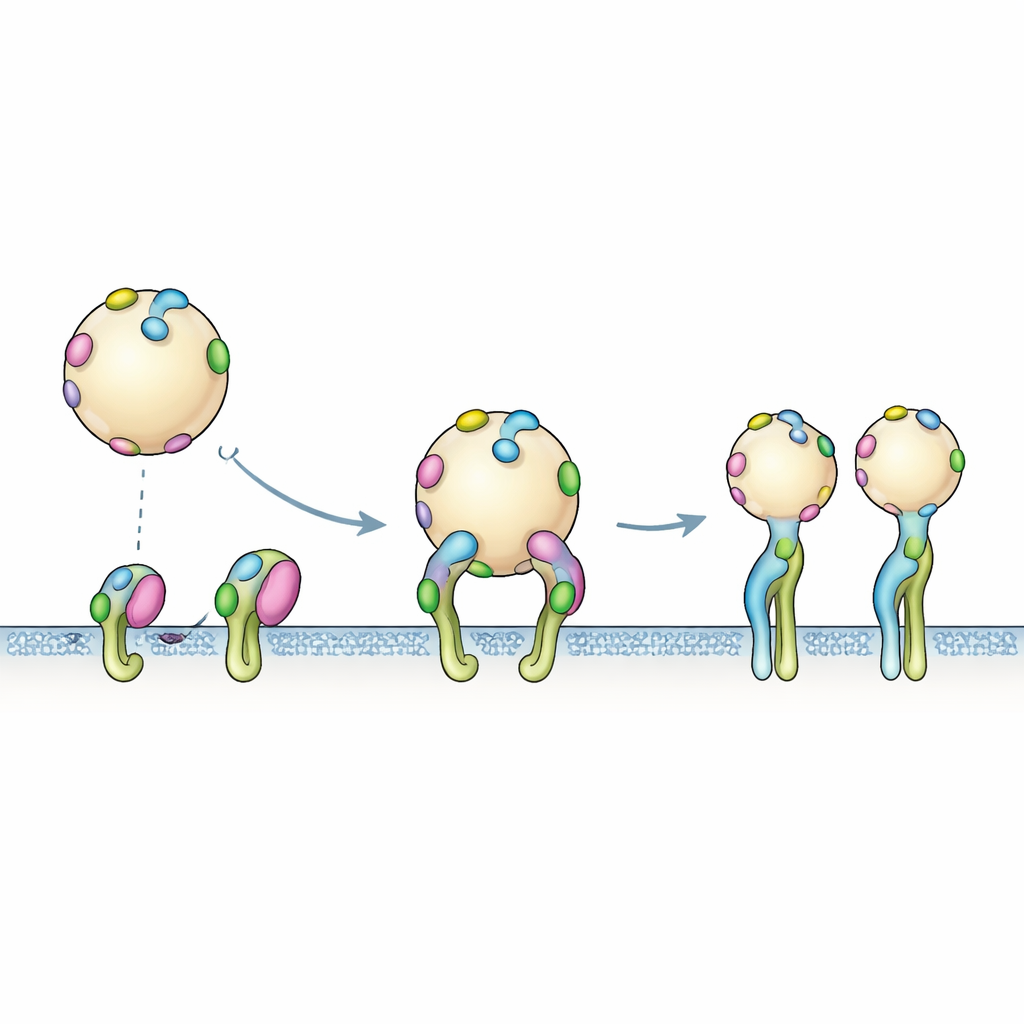
Från enstaka taggar till multivalenta grepp
Datorsimuleringar fångar en tagg som rör en receptor åt gången, men den verkliga EV-ytan är full av många kopior av PTHTRWA. Bindningsexperimenten speglade denna multivalenta verklighet: när en taggad vesikel närmar sig ett område med integriner kan flera taggar engagera sig samtidigt. Sensordatan passade bäst till en tvåstegsprocess. Först dockar vesikeln kortvarigt genom snabba, reversibla möten. Sedan sker en långsammare omarrangemang där integrinerna skiftar till sin öppna form och det övergripande greppet förstärks. Denna samverkande, månghandiga fattning förklarar varför den uppenbara bindningsstyrkan för hela vesiklar är högre än vad som skulle förutses från en enskild tagg ensam.
Vad detta kan innebära för framtida behandlingar
Enkelt uttryckt visar studien att EV:er beväpnade med PTHTRWA-tagg kan selektivt känna igen integriner som är överaktiva i lungcancer, och att de gör detta genom att knuffa dessa receptorer mot ett öppet, tätt bundet tillstånd. Genom att kartlägga dessa interaktioner i detalj ger forskarna designregler för nästa generationens vesikelbaserade bärare som kan leverera läkemedel, avbildningsagentier eller andra laster direkt till maligna celler samtidigt som frisk vävnad i stort sett ignoreras. Även om mer arbete i djur och människor kommer att krävas, för detta integrinriktade tillvägagångssätt visionen om personaliserad, EV-baserad cancermedicin ett steg närmare verklighet.
Citering: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Nyckelord: lungcancer, extracellulära vesiklar, integriner, riktad läkemedelsleverans, molekylära simuleringar