Clear Sky Science · sv
Bevis på koncept för extraktion av cellfritt DNA från plasma med vattenbaserat tvåfasesystem för flytande biopsi
Varför ett blodprov är viktigt för cancer och andra sjukdomar
Många moderna medicinska tester letar efter små DNA-fragment som flyter fritt i vårt blod. Dessa bitar, kända som cellfritt DNA, kan avslöja om en tumör släpper genetiskt material, om ett transplanterat organ hålls på väg att stöta bort eller hur en graviditet utvecklas. Men eftersom dessa DNA-fragment är få, korta och blandade med en soppa av proteiner och andra molekyler är det förvånansvärt svårt att isolera dem rent och snabbt. Denna studie presenterar ett nytt, enklare sätt att extrahera dessa fragment från blodplasma med en skonsam vattenbaserad separationsmetod, vilket potentiellt kan göra avancerade ”flytande biopsi”-tester mer tillgängliga och prisvärda.
Utmaningen att fånga små DNA-bitarsom
Läkare och forskare använder flytande biopsier för att läsa genetiska ledtrådar från ett enkelt blodprov istället för att skära ut vävnad. Problemet är att cellfritt DNA i plasma vanligtvis finns i bara några tiotals nanogram per milliliter och är upphackat i korta bitar. En liten andel av detta material kan komma från en tumör eller från ett transplanterat organ, så varje fragment räknas. Standardkit för extraktion fångar DNA genom att få det att fastna på kiselbaserade ytor i närvaro av starka salter, följt av flera tvätt- och centrifugeringssteg. Dessa kit fungerar bra men tar tid, kräver specialutrustning och kan vara dyra. De kan också ha svårt att återvinna de kortaste fragmenten och kan dra med sig oönskat långt normalt genomiskt DNA, vilket kan dölja sällsynta sjukdomsrelaterade signaler.
En tvålagersvattentrick för att fånga DNA
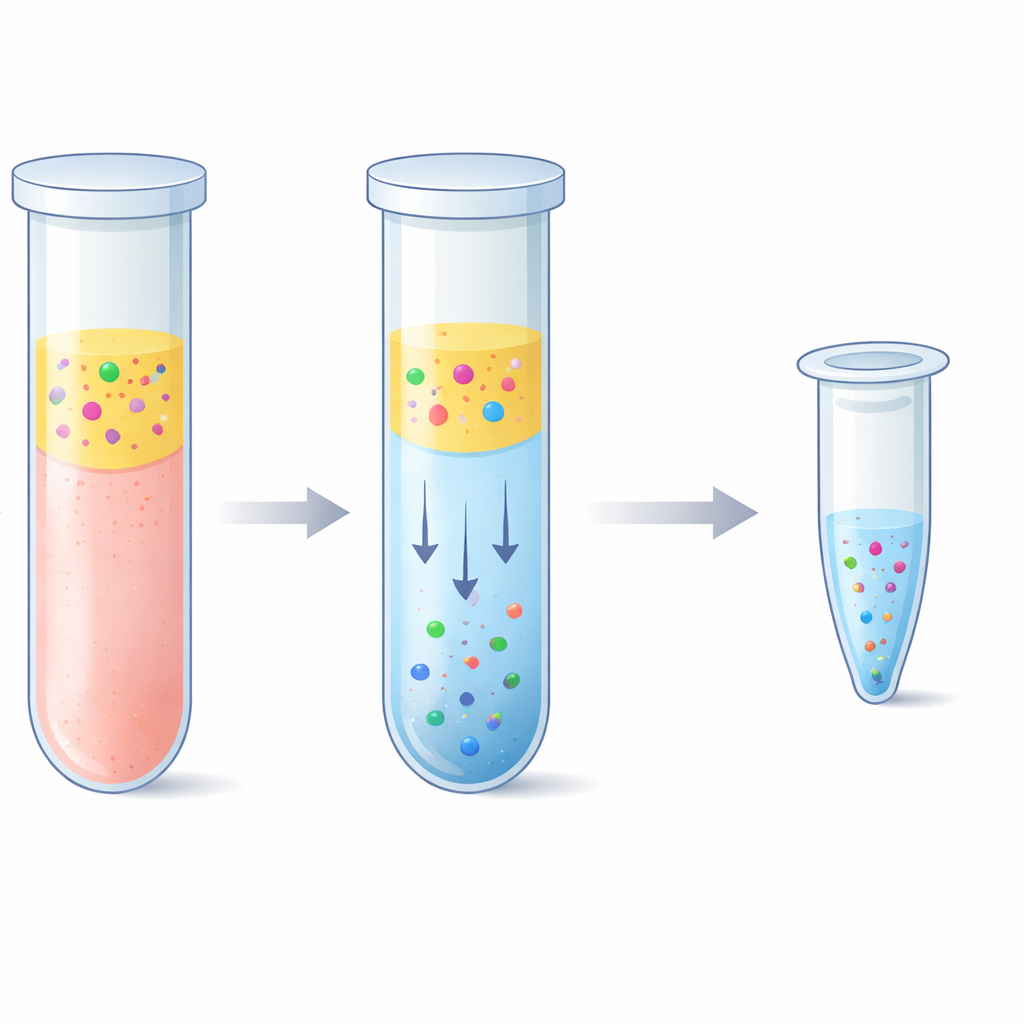
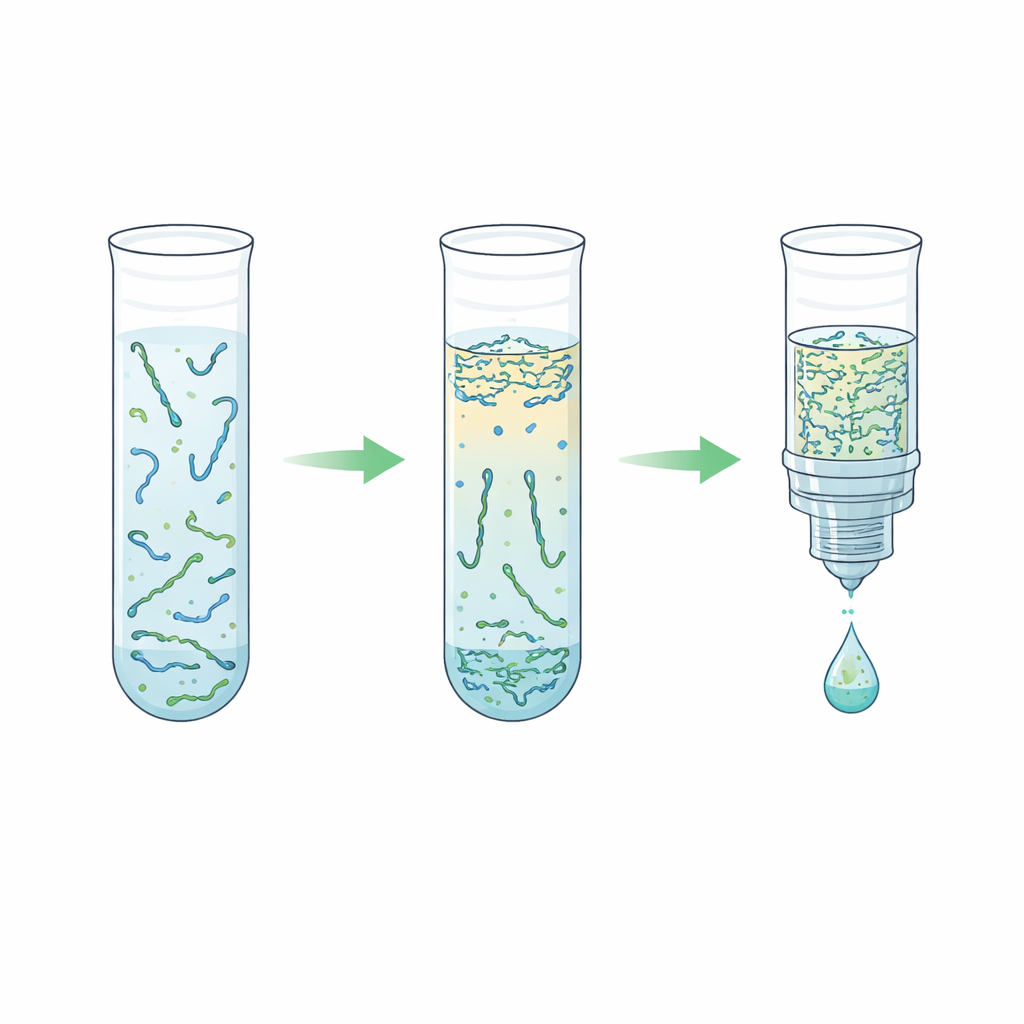
Teamet utforskade ett alternativ baserat på ett "aqueous two-phase system"—i klartext två vattenrika vätskor som inte blandar sig helt, ungefär som olja och vinäger men båda mestadels bestående av vatten. Genom att kombinera plasma med en polymer kallad polyetylenglykol och enkla fosfatsalter separerade blandningen naturligt i ett övre och ett nedre skikt. Anmärkningsvärt nog föredrog de korta DNA-fragmenten starkt det salt-rika nedre skiktet, medan de flesta blodproteiner och långa DNA-strängar stannade i det övre skiktet eller vid gränsytan. Forskarlaget finjusterade receptet så att det nedre skiktet förblev tillräckligt litet för att koncentrera DNA men fortfarande skonsamt nog för att undvika skador. De kombinerade sedan detta steg med en ”reverse elution”-rening, där det saltrika nedre skiktet pressas genom en porös matris för att ta bort salt och minska slutvolymen, vilket resulterar i en renare och mer koncentrerad DNA-lösning.
Förfina processen för verklig användning
Genom många testomgångar justerade författarna balansen mellan polymer och salt, centrifugeringshastigheter, volymer och frivilliga lysssteg som bryter upp protein–DNA-komplex. De fann att ökat polymerinnehåll längs vissa sammansättningslinjer fördubblade DNA-koncentrationen utan att skada återhämtningen, och att starkare konditionering i reverse elution-steget ungefär fyrdubblade koncentrationen jämfört med deras tidigare arbete. Överraskande upptäckte de att det ofta fungerade bäst att hoppa över hårda lysssteg innan tvålagersseparationen; lysering tenderade att störa faserna och minska utbytet. Ett strömlinjeformat, i hög grad lyssfritt arbetsflöde avlägsnade cirka 99,7 % av plasmaproteinerna samtidigt som upp till ungefär två tredjedelar av det korta DNA-ingångsmaterialet återvanns i en fyrfaldigt mindre volym — allt inom ungefär tio minuters total bearbetningstid och bara ett par minuters handpåläggning.
Hur den nya metoden står sig
Forskarna jämförde sitt tillvägagångssätt med ett allmänt använt kommersiellt kiselkit. Standardkitet gav något högre total DNA-avkastning och starkare koncentration eftersom det eluera i mycket små volymer. Däremot visade tvåfasesmetoden konsekventa återvinningar över 60 % över ett spann av DNA-ingångar, även vid mycket små startmängder, och krävde betydligt färre manuella steg och mindre utrustning. Viktigt var att den nya processen fungerade som ett inbyggt filter för fragmentlängd: den berikade för kort, cellfritt-liknande DNA samtidigt som långa strängar som kan komma från sönderfallna blodceller i hög grad uteslöts. Tester med kvantitativ PCR visade att de rengjorda extrakten inte hämmande efterföljande amplifiering. När teamet använde ett kommersiellt referensprov som innehöll kända cancerrelaterade mutationer kunde det DNA som återvanns med deras metod göras till sekvenseringsbibliotek, köras på en höggenomströmningsekvenserare och användas för att upptäcka alla förväntade varianter vid rätt frekvenser.
Vad detta kan innebära för framtida blodprov
Enkelt uttryckt visar detta arbete att en relativt enkel, vattenbaserad separation kan ersätta mer komplex fast-yte-kemi för att förbereda cellfritt DNA från plasma. Även om den nya metoden för närvarande ger något mindre DNA än de bästa kommersiella kiten erbjuder den snabb bearbetning, kraftfull borttagning av oönskade proteiner och långt DNA samt god kompatibilitet med PCR och next-generation sequencing. Om metoden valideras vidare på verkliga patientprover och förfinas för automation kan detta tillvägagångssätt sänka kostnader och förenkla laboratoriearbetsflöden, vilket kan hjälpa till att göra precisa, genetiskt baserade blodtester för cancer, transplantation och andra tillstånd mer allmänt tillgängliga.
Citering: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
Nyckelord: flytande biopsi, cellfritt DNA, cancertest i blodet, DNA-extraktion, next-generation sequencing