Clear Sky Science · sv
Undersökning av interaktioner mellan Escherichia coli Colicin E9-immunitetsprotein och DNA-gyras från Pseudomonas aeruginosa: avancerad beräkningsmetod för utveckling av nya antibiotikastrategier
Att omvandla bakterievapen till nya läkemedel
När antibiotikaresistens sprider sig börjar läkare få allt färre verktyg för att stoppa farliga infektioner. Några av de mest svårhanterliga gärningsmännen, som Pseudomonas aeruginosa, kan stå emot många läkemedel. Denna studie söker nya idéer i bakterierna själva och utforskar hur ett mikrobs inbyggda skyddsprotein skulle kunna återanvändas för att inaktivera ett avgörande enzym i en annan mikroorganism. Genom avancerade datorsimuleringar visar forskarna hur ett litet ”immunitetsprotein” kan fästa tätt vid ett nyckelenzym, vilket antyder en ny väg för framtida antimikrobiella medel.
Ett litet skydd mot ett dödligt toxin
Vissa stammar av Escherichia coli producerar kraftfulla proteintoxiner kallade coliciner som kan döda närliggande bakterier. För att undvika att förgifta sig själva tillverkar dessa bakterier även motsvarande immunitetsproteiner. Ett sådant skyddsprotein, känt som Colicin E9-immunitetsproteinet (ofta kallat Im9), hakar i toxinets klippdomän och förhindrar att det skadar värdcellens DNA. Eftersom detta partnerskap är så specifikt och starkt har forskare länge misstänkt att en detaljerad förståelse kan ge nya sätt att kontrollera skadliga bakterier. I detta arbete frågar författarna om Im9 också skulle kunna binda till DNA-gyras, ett essentiellt enzym i Pseudomonas aeruginosa som hanterar hur dess DNA är vridet och kopieras.
Att rikta in sig på ett sårbart enzym i en svårbehandlad bakterie
Pseudomonas aeruginosa är en betydande sjukhuspatogen som kan överleva i hårda miljöer och är resistent mot många läkemedel. DNA-gyras är ett av dess viktigaste enzymer och ansvarar för att hålla bakteriens långa DNA-strängar korrekt tvinnade så att de kan replikeras. Eftersom blockering av detta enzym kan stoppa bakterietillväxt är det redan ett beprövat mål för vissa antibiotika. Författarna använde ett djupinlärningsverktyg för att skanna den tredimensionella strukturen av Pseudomonas DNA-gyras och markera sannolika ”hotspots” — kluster av aminosyror på dess yta som är viktigast för bindning till partner. Dessa regioner utgör enzymets aktiva ficka, där normal DNA-hantering sker och där en potentiell hämmare helst skulle fästa.
Att simulera ett molekylärt handslag
För att se om Im9 kunde gripa tag i dessa hotspots använde forskarna molekylära dockningsprogram som virtuellt låter proteiner ”passa” ihop som 3D-pusselbitar. De rengjorde och kompletterade först tillgängliga strukturer för både Im9 och DNA-gyras, reparerade en saknad slinga i enzymet och körde korta simuleringar för att avspänna utsatta regioner. Därefter använde de två kompletterande dockningsverktyg, ClusPro och LightDock, för att generera många kandidatkomplex. Ur dessa valde de de mest lovande arrangemangen och utsatte dem för långa molekylärdynamiska simuleringar som spände över hundratals nanosekunder. Dessa tidsupplösta ”filmer” lät dem observera hur de två proteinerna anpassade sig, böjde sig och stabiliserade sina former när de bundit till varandra.
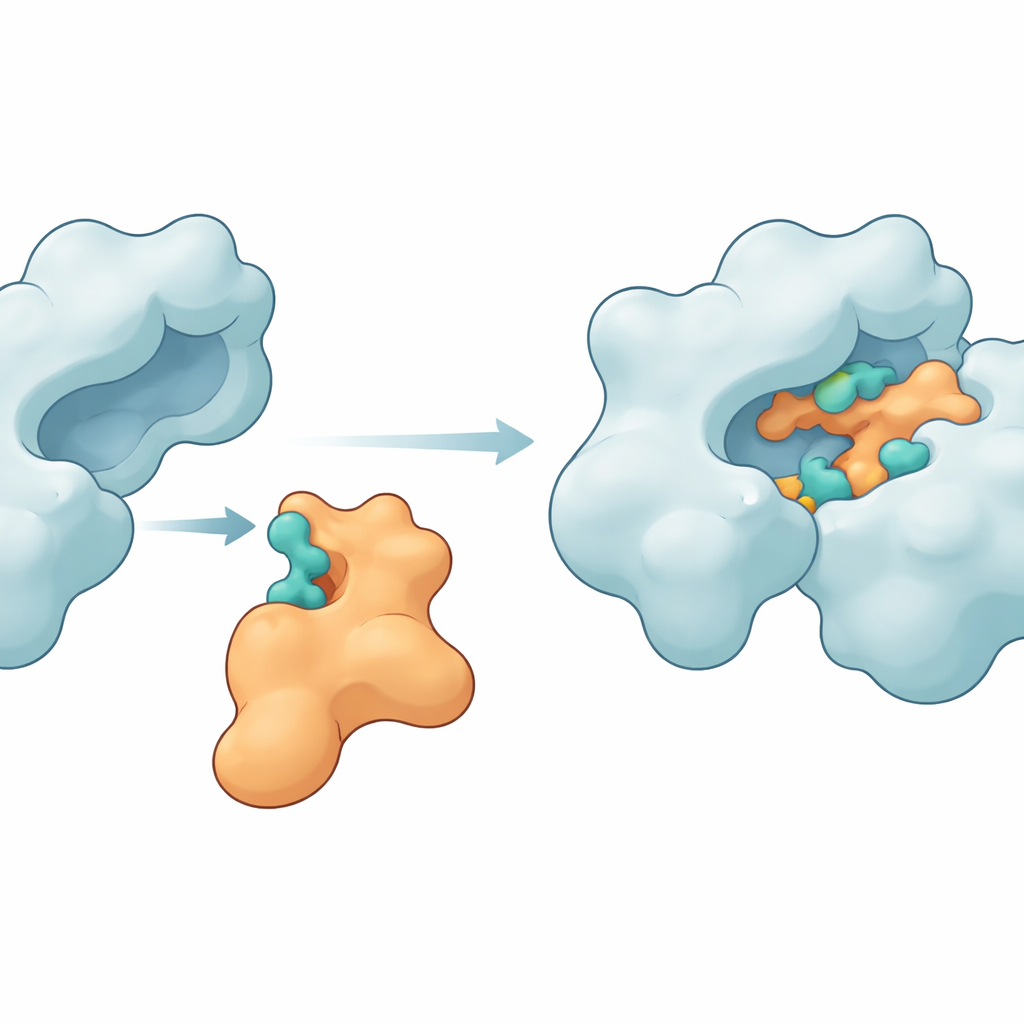
Nyckelkontaktpunkter som håller proteinerna samman
Simuleringarna visade att Im9 faktiskt kan bilda ett tätt och bestående komplex med DNA-gyras. Flera aminosyror på enzymet — såsom MET27, ASP47, LYS105, LEU198, ASN199, ARG191 och GLU194 — bildade upprepade gånger vätebindningar och andra attraktiva krafter med matchande ytor på Im9. I en framstående modell behöll de två partnerna mellan sex och tio vätebindningar under större delen av simuleringen, ett tecken på ett starkt och välordnat gränssnitt. Andra strukturella mått, inklusive hur kompakta proteinerna förblev och hur mycket deras former fluktuerade, visade att enzymet förblev intakt medan immunitetsproteinet flexade precis tillräckligt för att forma sig runt gyrasyta. Energiberäkningar med MM-GBSA-metoden stödde ytterligare idén att dessa kontakter ger en gynnsam, om än måttlig, bindningsfri energi, dominerad av elektrostatiska och van der Waals-bidrag.
Från datormodeller till framtida antimikrobiella medel
Tillsammans tyder resultaten på att Colicin E9-immunitetsproteinet kan binda stabilt till den aktiva regionen i Pseudomonas DNA-gyras och bilda ett långlivat komplex som i princip skulle kunna blockera enzymets normala roll i DNA-hantering. Även om dessa fynd helt bygger på datormodeller och fortfarande kräver experimentell verifiering, ger de en detaljerad ritning för var och hur en proteinbaserad hämmare skulle kunna fästa. För icke-specialister är huvudbudskapet att naturens egna bakterievapen och skydd kan inspirera nya strategier mot svårbehandlade infektioner. Genom att förstå detta mikroskopiska handslag på atomär nivå tar forskare ett steg närmare att utforma nya antimikrobiella medel som stänger ner viktiga bakterieenzymer utan att skada människoceller.
Citering: Alfaraj, R., Alkathiri, F. & Chikhale, R. Investigating Escherichia coli Colicin E9 immunity protein interactions with DNA gyrase of Pseudomonas aeruginosa: advanced computational approach for developing novel antimicrobial strategies. Sci Rep 16, 10786 (2026). https://doi.org/10.1038/s41598-026-44427-2
Nyckelord: antibiotikaresistens, DNA-gyras, protein–protein-interaktioner, beräkningsbaserad läkemedelsdesign, Pseudomonas aeruginosa