Clear Sky Science · sv
Kristallografiska data för Pyrococcus furiosus dolichylfosfat-mannossyntas antyder att enzymet kan vända sitt glykolipidprodukt
Hur värmeälskande mikrober håller sitt cellskikt i form
Många mikrober som frodas i kokheta miljöer överlever tack vare en skyddande sockerkappa på cellens yta. För att bygga denna kappa behövs särskilda fett–socker-molekyler som måste tillverkas på ena sidan av cellmembranet och sedan flyttas till den andra. Denna studie dissekerar ett sådant molekyltillverkande enzym från en värmeälskande mikroorganism och föreslår att samma protein, anmärkningsvärt nog, också kan hjälpa till att vända sitt produkt över membranet — och därmed göra två jobb på en gång.
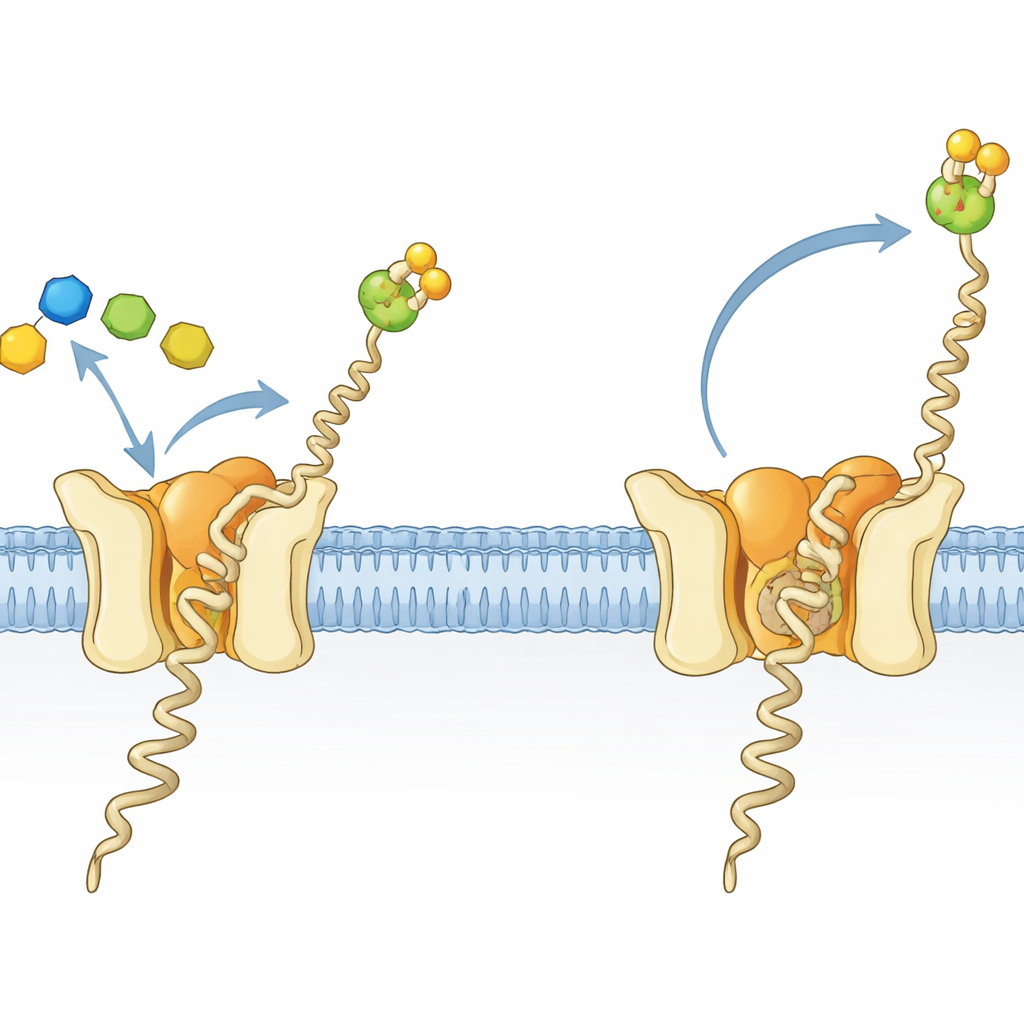
En liten fabrik för en avgörande socker–fettsubstans
Cellernas proteiner i alla livets domäner dekoreras med sockerkedjor, en process som är nödvändig för korrekt veckning, stabilitet och cell–cell-kommunikation. I arkéer och eukaryoter är en nyckelkomponent för dessa dekorationer en socker–fettsubstans kallad dolichylfosfat mannose (Dol-P-Man). Den består av en lång fet svans förankrad i membranet och ett socker–fosfat-huvud som sticker ut i den vattenrika omgivningen. Dol-P-Man bildas av enzymet dolichylfosfat-mannossyntas (DPMS), som överför en mannossocker från en löslig donor till ett membranbundet lipid. I den hypertermofila arkenen Pyrococcus furiosus är DPMS ett en-kedjigt protein, betecknat typ-III DPMS, med en löslig katalytisk region fäst vid en fyr-helix membranpassage vars roll tidigare varit oklar.
Fånga enzymet in action
Forskarna kristalliserade P. furiosus DPMS tillsammans med dess substrat och följde reaktionen med röntgenkristallografi. Deras nya struktur, kombinerad med tre tidigare, fångar en serie ögonblicksbilder runt det tillfälle då sockret överförs. I ett tillstånd är donormolekylen (GDP-mannos) och en Dol-P–lik acceptor bundna i en exakt geometri som placerar mannosens reaktiva kol direkt framför fosfatgruppen på Dol-P — en idealisk ”för-överföring”-konfiguration. Slingor i enzymet fungerar som fram- och bakdörrar: de stänger för att hålla donorn och metalljonen på plats, för att sedan omorganisera sig och öppna en väg för Dol-P att komma in och för den använda GDP att lämna när sockret har överförts. Dessa detaljer klargör hur enzymet säkerställer effektiv och noggrann sockeröverföring vid membranytan.
En upp-och-ned-produkt dold i membranet
Mer överraskande var ett andra, distinkt tillstånd som observerades i samma kristaller. Här ligger den färdiga Dol-P-Man-molekylen inte i det aktiva stället utan sitter djupare inne i den membranpassande delen av proteinet, i en ”upp-och-ner”-orientering. Dess socker–fosfat-huvud sitter i en polar ficka mellan två par helixar (TMD1 och TMD2), medan den feta svansen löper längs en fåra formad av helixarna. En nyckelaminosyra, en fenylalanin, tycks fungera som en grind som antingen kan blockera eller öppna tillgången till denna ficka. Elektrontätheten och sättet proteinet packas i kristallen talar för att denna omvända Dol-P-Man inte är en artefakt av kristallkontakter, utan ett genuint, välbefolkat tillstånd som enzymet kan anta.
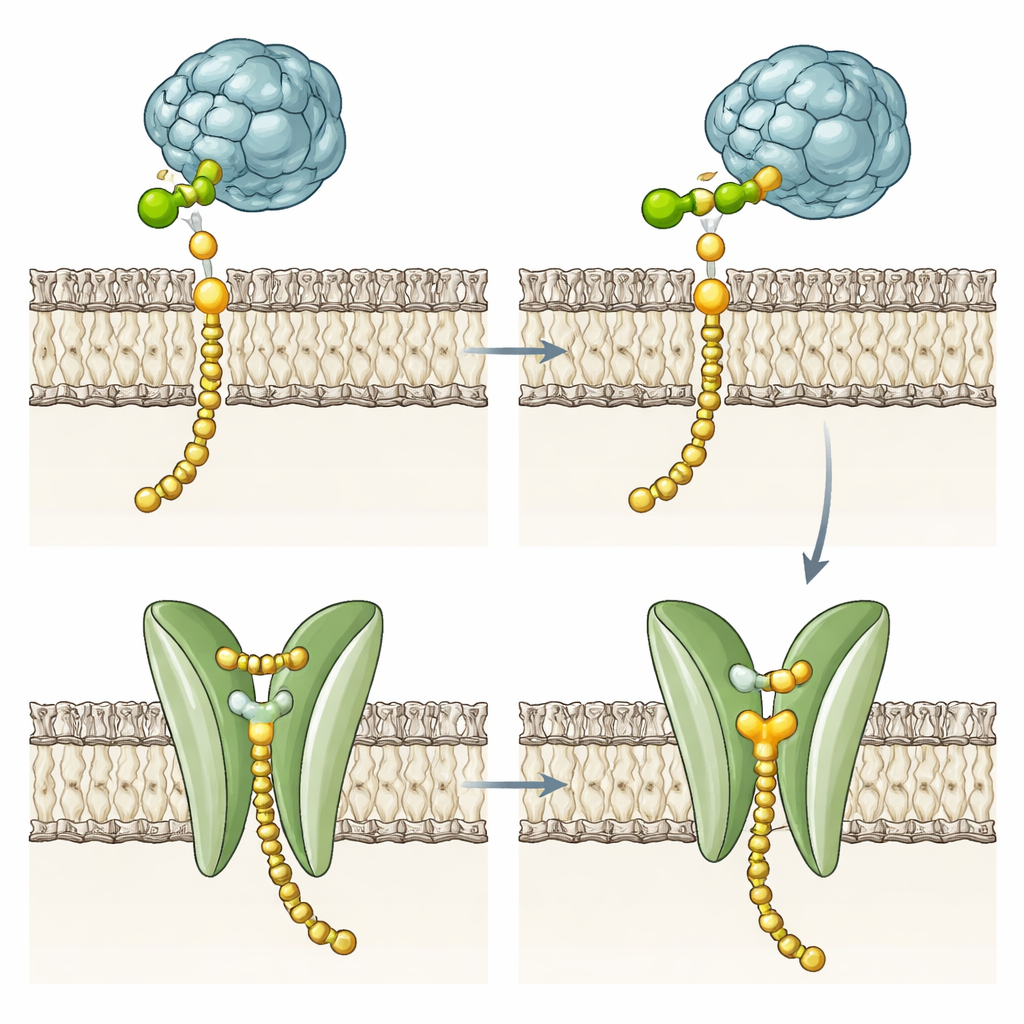
Mutanta enzymer pekar på ett andra jobb
För att testa om den membranpassande domänen krävs för sockeröverföringskemin konstruerade teamet flera varianter. De tog bort de flesta eller alla helixarna, bytte ut dem mot ett annat membranselement från jäst-DPMS, eller förändrade viktiga fickresiduer och fenylalanin-grinden. Anmärkningsvärt nog producerade dessa mutanter fortfarande Dol-P-Man i liknande takt som det intakta enzymet, även om vissa var något mindre stabila i membranet. Detta visar att kärnkemin ligger i den lösliga katalytiska regionen och att fyr-helix-bunten inte är nödvändig för att fästa mannos på Dol-P. Istället antyder dess konservade polära ficka, fåran och grindresiduen en specialiserad roll i hanteringen av den färdiga produkten, särskilt i hypertermofila arkéer vars styva membran gör spontan lipidflippen energimässigt kostsam.
Varför ett tvåfunktionellt enzym är betydelsefullt
Sammantaget föreslår författarna, utifrån strukturella och mutagenesdata, att typ-III DPMS är ett ”moonlighting”-protein. Först syntetiserar det Dol-P-Man på den inre sidan av arkéns plasmamembran; sedan kan dess transmembrandomän hjälpa till att vända socker–fettsubstansen så att huvudgruppen kommer ut på cellens utsida, redo att användas av andra enzymer som bygger cellens sockerkappa. Evolutionen verkar ha favoriserat denna kimeriska design främst i extremt värmeälskande arkéer, där det att placera syntesstället nära en dedikerad flippfåra kan minimera förluster och termisk skada. Även om detta arbete ännu inte bevisar flip-aktivitet direkt, erbjuder det en konkret strukturell modell för hur ett enzym både kan skapa och omplacera ett viktigt lipidintermediat över en krävande membranbarriär.
Citering: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Nyckelord: dolichylfosfat mannose, lipidflippas, arkéer, proteinglykosylering, membranenzym