Clear Sky Science · sv
Modellering av Clostridioides difficile‑toxins patogenes och antiserumskydd i en immunokompetent tarm‑på‑chip‑plattform
Varför denna modell för tarminfektion är viktig
Antibiotika räddar liv, men kan också lämna tarmen sårbar för farliga infektioner. En av de värsta boven är Clostridioides difficile, en bakterie som kan orsaka svår diarré och livshotande inflammation i tjocktarmen, särskilt hos inneliggande patienter. Denna studie presenterar en miniatyriserad “tarm på en chip” som återskapar centrala egenskaper hos den mänskliga tarmen, inklusive blodkärl och immunceller, för att i realtid följa hur C. difficile-toxiner skadar tarmen och hur antikroppsbehandlingar kan stoppa den skadan.
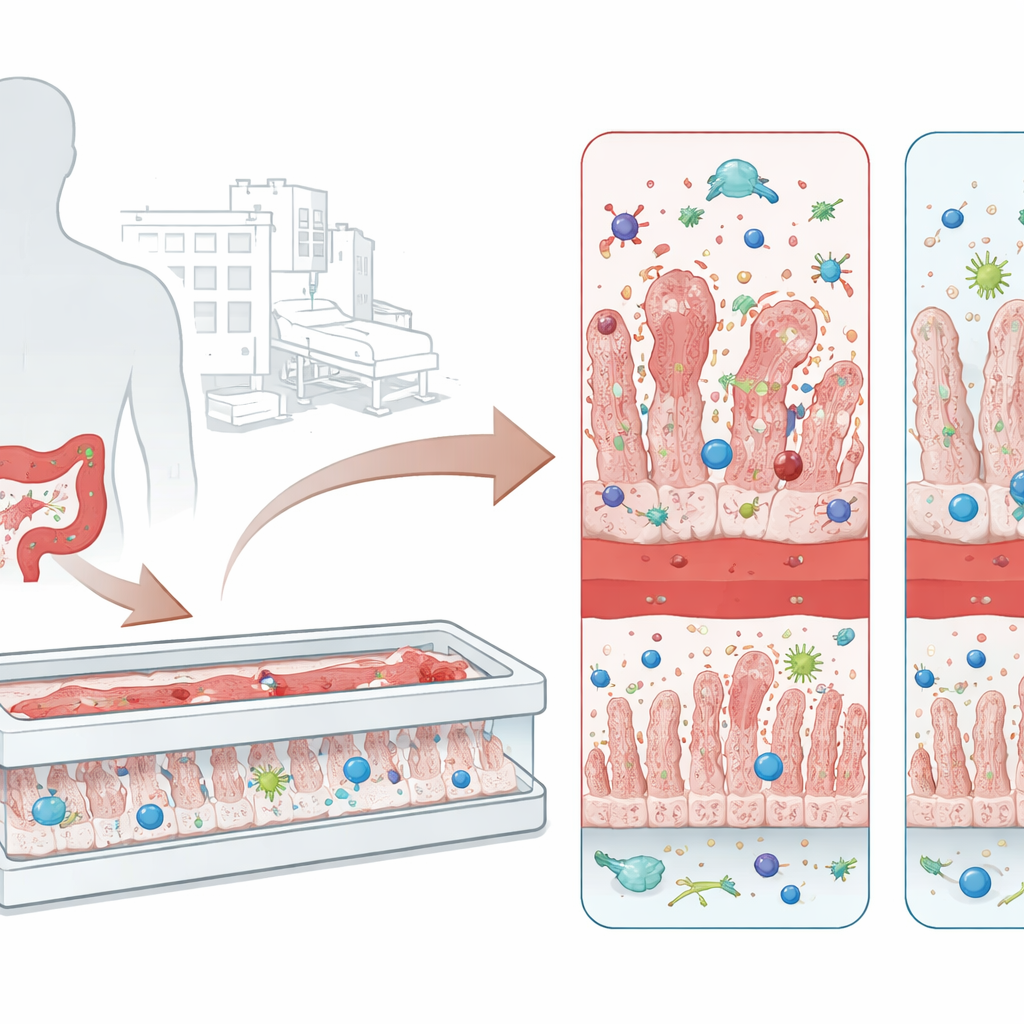
Från envis sjukhusbakterie till tarmskada
C. difficile trivs hos personer vars normala tarmflora har störts, ofta efter en kur med bredspektrumantibiotika. Mikroben överlever ogynnsamma förhållanden som tåliga sporer och, när den väl etablerat sig i tjocktarmen, utsöndrar den två huvudtoxiner kända som TcdA och TcdB. Dessa toxiner angriper tarmceller, lossar tätningarna mellan dem och utlöser inflammatoriska vågor. Resultatet kan variera från besvärlig diarré till pseudomembranös kolit, ett tillstånd präglat av lager av död vävnad och immunceller som täcker tarmväggen. Nuvarande behandlingar bygger mest på mer antibiotika och ibland fekal transplantationsbehandling, men många patienter drabbas av återkommande infektioner, vilket visar på behovet av bättre metoder för att studera sjukdomen och testa toxin‑blockerande terapier.
Att bygga en liten levande tarm på en chip
Traditionella laboratoriemodeller odlar ett plant skikt av tarmceller i en petriskål. Dessa tvådimensionella kulturer är användbara men saknar blodkärl, immunceller och den milda vätskeflöde som formar en riktig tarm. Forskarna använde istället en mikroingenjörskonstruerad “tarm‑på‑chip”‑enhet med två parallella kanaler separerade av ett poröst membran. Ena sidan är beklädd med tarmceller som växer ut i fingerliknande veck som liknar villi och bildar en tät barriär. Motsatta sidan innehåller mänskliga blodkärlsceller. I denna miniatyrvävnad tillsatte teamet monocyt‑deriverade makrofager som bosätter sig i tarmväggen och cirkulerande neutrofiler som kan färdas genom kärlkanalen och infiltrera vävnaden, vilket skapar en immunokompetent tarm‑på‑chip (i‑IoC) som bättre efterliknar en levande tarm.
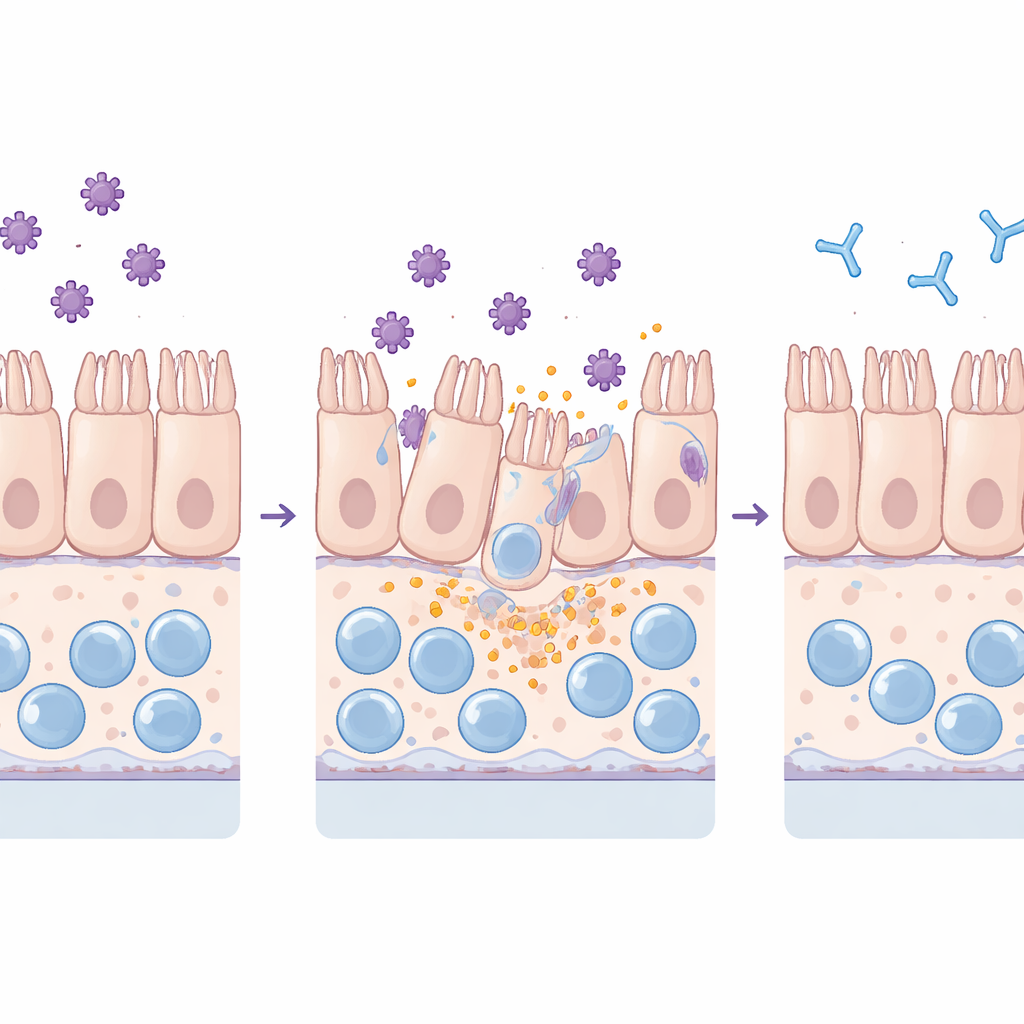
Att se hur toxiner skadar barriären
Teamet exponerade både standardiserade platta kulturer och den mer komplexa chipen för renade TcdA och TcdB. De övervakade hur väl tarmbarriären höll ute fluorescerande färgämne, undersökte junction‑proteiner som håller intilliggande celler ihop, och mätte inflammatoriska molekyler och markörer för cellskada i den omgivande vätskan. Båda toxinerna skadade vävnaden, men på olika sätt: TcdA störde främst tight junctions och fick cellerna att dra ihop sig, medan TcdB ledde till omfattande cellförlust från lagret. Avgörande var att chipet upptäckte dessa effekter vid mycket lägre toxinnivåer än de platta kulturerna, vilket speglar dess högre känslighet och mer livliknande beteende under kontinuerligt flöde.
Immunceller eldar på inflammationen — och kan skyddas
Tillsats av makrofager och neutrofiler i chipet förstärkte reaktionen mot toxinerna. Makrofager ökade frisättningen av viktiga inflammatoriska budbärare som IL‑6 och IL‑8 men förbrukades själva, i linje med en inflammatorisk form av celldöd. Neutrofiler fastnade på kärlväggen och migrerade in i tarmvävnaden, vilket speglar den immuncellsinfiltration som ses hos patienter. Längre toxinexponering skadade inte bara tarmens epitel utan så småningom även kärllagret. När forskarna däremot förblandade toxinerna med toxinneutraliserande antikroppsera minskade strukturella skador, barriärläckage, cytokinstormar, makrofagförlust och neutrofilinfiltration markant. I förlängda experiment kunde vävnader skadade av TcdB delvis återhämta sig när toxinerna togs bort, medan TcdA orsakade mer bestående skada, vilket antyder olika reparationsförmåga efter respektive toxin.
Vad detta betyder för patienter och terapier
För en allmän läsare är huvudbudskapet att denna lilla, levande tarmmodell realistiskt kan efterlikna hur C. difficile-toxiner skadar tarmen och väcker immunsystemet, samtidigt som den visar hur väl antitoxinantikroppar kan skydda vävnaden. Jämfört med enkla cellager är tarm‑på‑chip mer känsligt, inkluderar blodkärl och immunceller, och kan köras i flera dagar för att fånga både tidig skada och försök till återhämtning. Det gör den till en lovande testplattform för nästa generations behandlingar och vacciner som neutraliserar toxiner utan att ytterligare störa tarmfloran, och potentiellt ett verktyg för att skräddarsy terapier med patient‑härledda celler i framtiden.
Citering: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Nyckelord: Clostridioides difficile, tarm‑på‑chip, tarminfektion, neutraliserande antikroppar, organ‑på‑chip‑modeller