Clear Sky Science · sv
Etikettfri multiphotonmikroskopi och maskininlärning för identifiering av hepatocellulärt karcinom
Varför detta är viktigt för personer med levercancer
Levertumörer, särskilt hepatocellulärt karcinom, är både vanliga och dödliga, och kirurgi är ofta den enda chansen till bot. Under en operation måste kirurger ta bort hela tumören samtidigt som så mycket frisk lever som möjligt sparas — en svår avvägning när redan sjuk levervävnad ser onormal ut. Denna studie undersöker ett nytt sätt att "se" cancer i realtid under operation, utan färgämnen eller tidskrävande laboratoriearbete, genom att kombinera avancerad laserbaserad mikroskopi med artificiell intelligens. Målet är att hjälpa kirurger att snabbare och mer exakt hitta tumörens verkliga kant, vilket potentiellt kan förbättra patientutfallen.
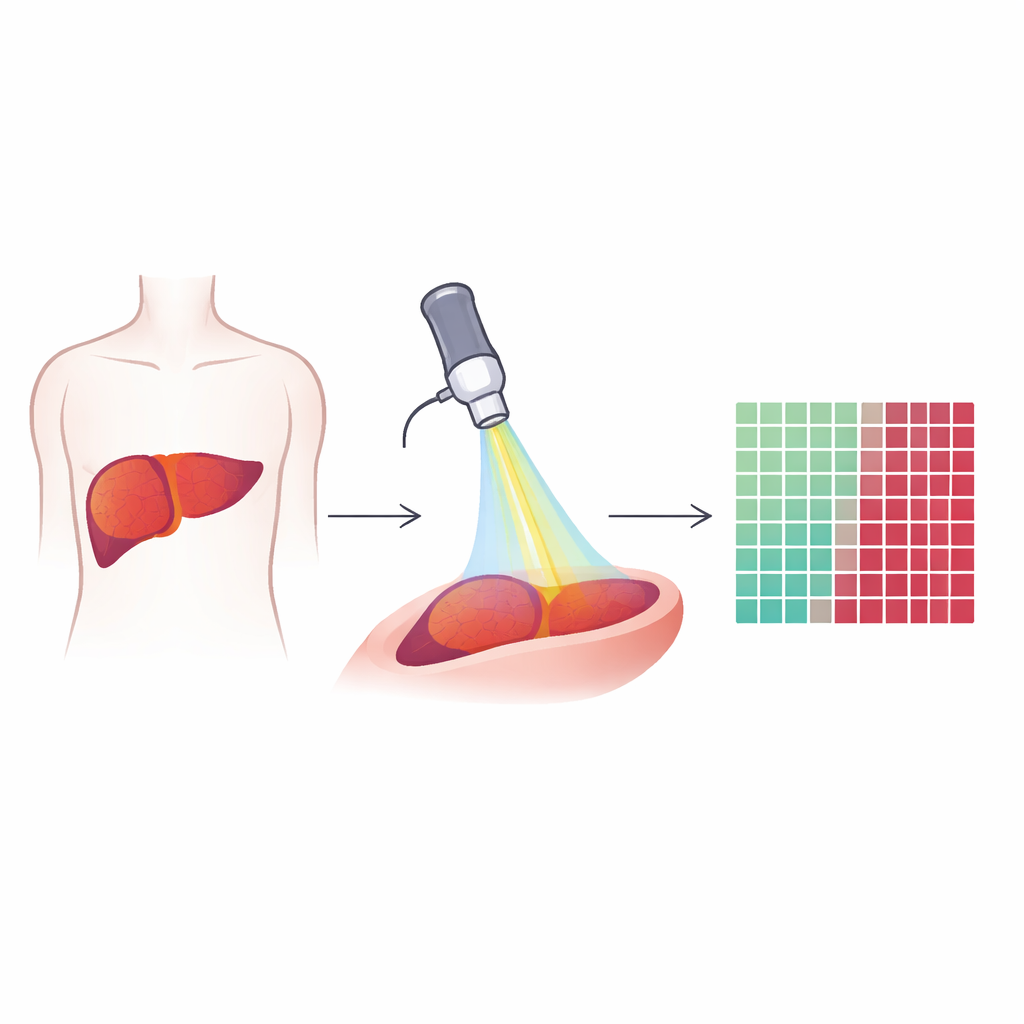
Att titta in i vävnad med särskilt ljus
Forskarna använde en teknik som kallas multiphotonmikroskopi, vilken bygger på mycket korta laserpulser för att få naturliga molekyler i vävnaden att lysa eller generera signaler. Istället för att tillsätta färgämnen eller kontrastmedel läser metoden av vad som redan finns: lipider, kollagenfibrer och naturligt fluorescerande ämnen i cellerna. Tre typer av signaler registrerades från varje litet synfält i levrar: en som framhäver lipider, en som visar autofluorescens från molekyler som NADH och vitamin A, och en som avslöjar styva kollagenfibrer. Tillsammans skapar dessa signaler färgrika, högupplösta bilder som visar både enskilda celler och den övergripande arkitekturen i levervävnad och tumörer.
Att fånga levercancerns många uttryck
Teamet undersökte vävnad från 76 patienter som genomgått operation för levercancer, och tittade både på tumören och på den omgivande levern. De visade att denna etikettfria avbildning kan återge klassiska växtmönster för hepatocellulärt karcinom, såsom tunna eller tjocka cellplattor, solida skikt och körtelliknande strukturer. Den avslöjar också förändringar i omgivande lever, inklusive fettinlagring och ärrbildning, vilket är vanligt hos patienter med kronisk leversjukdom. Viktigt är att dessa mönster var synliga även när bilderna förvärvades i relativt låg upplösning, liknande vad framtida endoskopiska enheter inuti kroppen skulle kunna leverera. Detta tyder på att tillvägagångssättet kan vara praktiskt i operationssalen, inte bara i ett laboratorium.
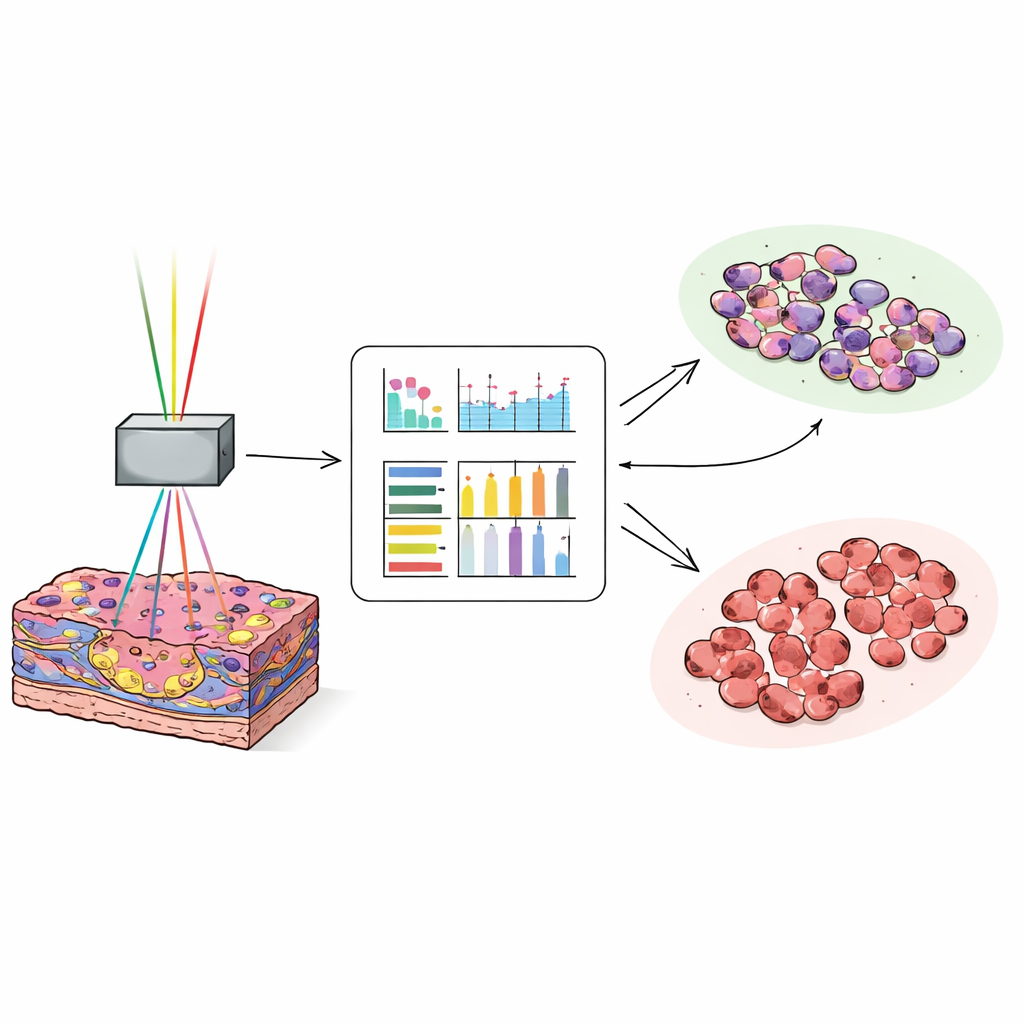
Att lära en dator att hitta tumörkanten
För att omvandla rika men komplexa bilder till snabba beslut omvandlade forskarna varje bild till siffror som beskriver textur, till exempel hur slät, grov eller varierad pixelmönstren är. För varje bildkanal beräknade de 17 sådana mått och tränade sedan ett neuralt nätverk på cirka 25 000 bilder från 35 patienter för att skilja tumörvävnad från icke-cancerös lever. De testade sedan modellen på omkring 27 000 nya bilder från ytterligare 38 patienter. När datorn använde en kombination av autofluorescens- och kollagensensitiva signaler klassificerade den bilder som tumör eller normal korrekt i ungefär 97 av 100 fall. Även de mest subtila, väl differentierade tumörerna, som kan vara svåra för patologer att känna igen på snabba frysta snitt, klassificerades med hög noggrannhet.
Vad ljusmönstren avslöjar om cancer
Genom att jämföra olika signal kombinationer fann studien att autofluorescens bar den mest användbara informationen för att skilja cancer från icke-cancer. Detta sken uppstår från många naturliga molekyler i cellerna och från strukturer som elastin och kollagen, så det kodar celltäthet, kärnornas storlek och form (synliga som mörkare områden), fettdroppar och sammansättningen av omgivande vävnad. Att lägga till den kollagenspecifika signalen skärpte ytterligare kontrasten mellan tumör och bakgrundslever och speglade kända skillnader i hur fibrer och blodkärl är ordnade. Överraskande bidrog den lipidfokuserade signalen mindre till automatisk klassificering, en praktisk insikt eftersom det kan möjliggöra enklare enhetsdesigner som förlitar sig på en laserstråle istället för mer komplexa tvåstråliga system.
Från bänken i laboratoriet till operationssalen
För att efterlikna verklig kirurgisk användning applicerade teamet också sin bästa modell på vävnadsprover som inkluderade den faktiska gränsen mellan tumör och lever och skapade sannolikhetskartor som markerade var cancern slutade och normal vävnad började. Dessa kartor överensstämde i allmänhet väl med konventionell histologi, även om mycket feta eller kollagentrika områden ibland förvirrade klassificeraren. Författarna pekar på kvarstående hinder innan tekniken kan vägleda levande operationer, inklusive den begränsade optiska avbildningsdjupet, behovet av robusta, sterila endoskop, rörelser och blod i operationsfältet samt utmaningen att validera artificiell intelligens på stora, verkliga dataset. Trots det visar arbetet att etikettfri multiphotonavbildning, kombinerad med maskininlärning, kan fungera som ett snabbt, digitalt mikroskop som en dag kan hjälpa kirurger att skära mer precist och säkert, öka sannolikheten att all cancer avlägsnas samtidigt som så mycket frisk lever som möjligt bevaras.
Citering: Galli, R., Korn, S., Aust, D. et al. Label-free multiphoton microscopy and machine learning for recognition of hepatocellular carcinoma. Sci Rep 16, 8734 (2026). https://doi.org/10.1038/s41598-026-43831-y
Nyckelord: levercanceravbildning, multiphotonmikroskopi, autofluorescens, kirurgiska marginaler, maskininlärning