Clear Sky Science · sv
Klargör sambandet mellan affinitet och potens i prestandan hos terapeutiska IgE
Vända allergiantikroppar mot cancer
Allergiker vet hur kraftfulla IgE-antikroppar kan vara – molekylerna som utlöser kliande ögon och plötsliga nysningar. Denna studie ställer en överraskande fråga: kan samma kraftfulla biologi riktas om för att bekämpa cancer, och i så fall hur exakt bör dessa antikroppar justeras för att fungera bäst? Forskarna fokuserade på bröstcancer som uttrycker proteinet HER2, inklusive fall där HER2 finns i mycket låga nivåer och där befintliga läkemedel ofta misslyckas.
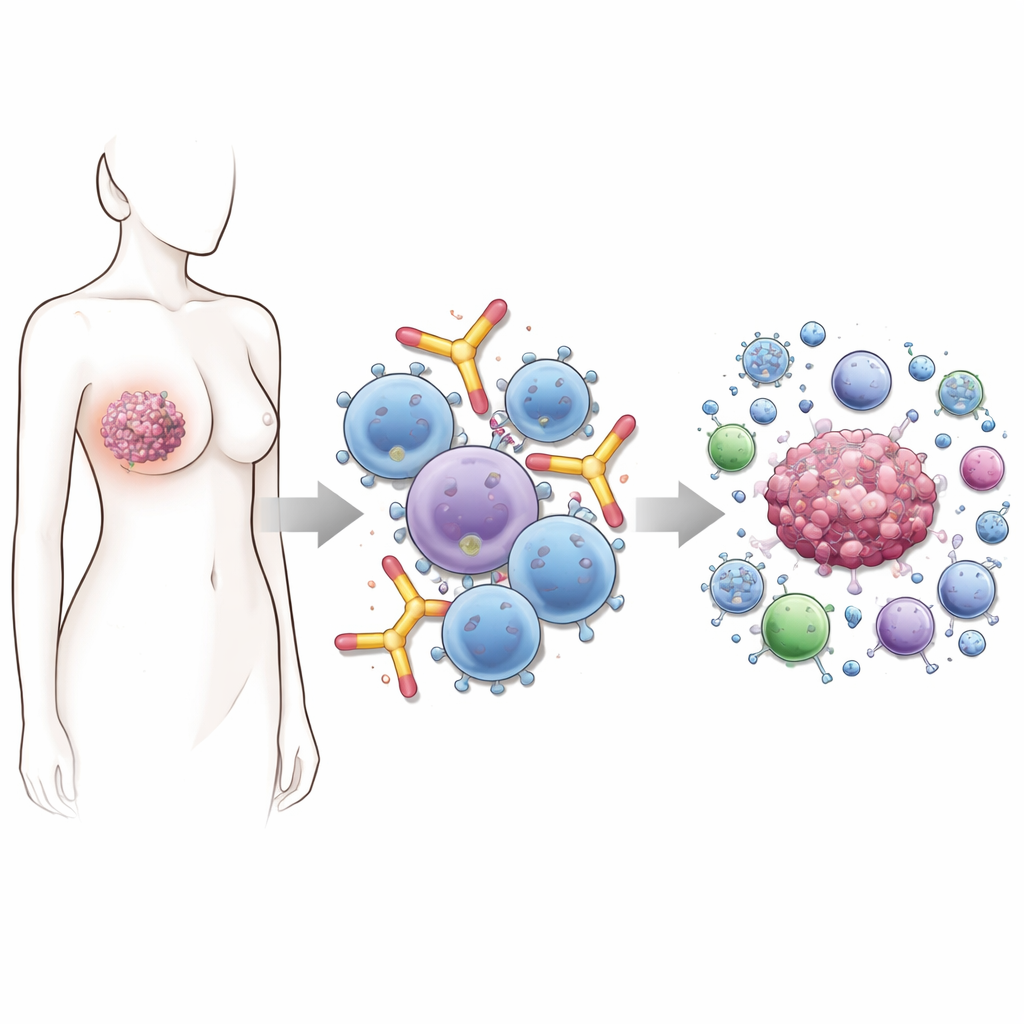
Varför denna antikroppsklass är så speciell
De flesta antikroppsbaserade läkemedel på marknaden idag tillhör IgG-klassen. De är arbetsdjur inom modern cancerterapi men har begränsningar – särskilt när tumörer undviker angrepp genom att sänka mängden av måltavleproteinet på sin yta. IgE-antikroppar skiljer sig. De fäster naturligt mycket hårt vid immunceller som mastceller, basofiler, monocyter och makrofager och förbereder dem för snabba svar. Vid allergi betyder det explosionsartade reaktioner mot pollen eller mat. I cancer skulle samma koppling kunna innebära snabba, fokuserade angrepp mot tumörceller så fort IgE möter sitt mål på tumörytan.
Designa en skarpare cancersökande IgE
Teamet hade tidigare skapat en IgE-antikropp, kallad EPS 226, som känner igen HER2 på bröstcancerceller och kan bromsa tumörtillväxt i experimentella modeller. I detta nya arbete ville de besvara en subtil men avgörande konstruktionsfråga: förbättrar en starkare bindning till HER2 verkligen förmågan att mobilisera immunsystemet, eller gör IgE:s naturliga ”många-händer”-bindning (kallad aviditet) redan det mesta av jobbet? För att undersöka detta använde de riktad mutagenes och selektion i bakterier för att generera miljontals små variationer av den HER2-bindande regionen och fiskade sedan fram 12 nya IgE-varianter som band HER2 starkare än den ursprungliga antikroppen.
Testa kraften på celler och i djur
Dessa förbättrade antikroppar utsattes sedan för hårda tester i en serie cellbaserade experiment. När de laddades på mastceller och utsattes för HER2-positiva cancerceller utlöste de flesta av de starkare bindande IgE:erna kraftigare degranulation – ett aktiveringssvar som frigör potenta immunkemikalier. En variant, omdöpt till EPS 232, utmärkte sig genom sin förmåga att aktivera celler samtidigt som den fortfarande band effektivt till HER2 på mänskliga och råtttumörceller. Ytterligare tester visade att EPS 232 bättre rustade immunceller för att döda cancer: den ökade dödandet av celler av basofiler och främjade effektivare fagocytos av HER2-positiva tumörceller av både konstruerade immunceller och primära mänskliga makrofager. Intressant nog hjälpte ökad bindningsstyrka bara upp till en viss gräns; varianter med extremt hög affinitet överträffade inte EPS 232, vilket tyder på att det finns en "sweet spot" där greppet är tillräckligt starkt för att vara effektivt men inte så starkt att det hindrar hur många antikroppar och immunceller som kan engagera varje tumörcell.
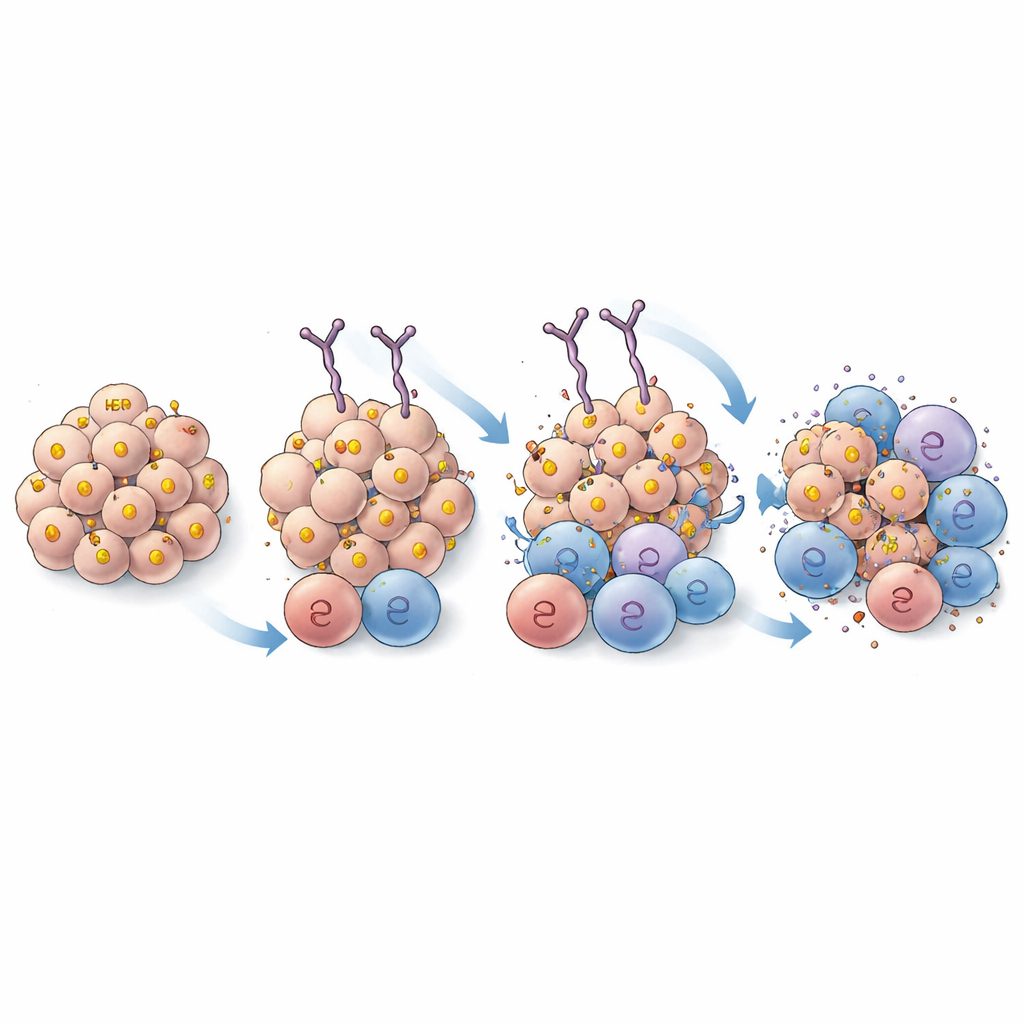
Fördjupning i hur antikroppen binder
För att säkerställa att förbättringarna kom från starkare grepp snarare än från igenkänning av en ny del av HER2 använde forskarna högupplöst kryo-elektronmikroskopi för att visualisera hur EPS 232 och ursprungliga EPS 226 sitter på HER2-proteinet. Strukturerna visade att båda antikropparna dockar på samma region av HER2 och använder mycket liknande kontaktpunkter, med endast subtila skillnader som inte förväntades ändra det övergripande bindningsstället. Detta stöder idén att den förbättrade prestandan hos EPS 232 uppstår från förbättrad affinitet snarare än en förändring av målet.
Från bänk till tumörkontroll
Det verkliga testet kom i djurmodeller. I möss med mänskliga brösttumörer och försedda med mänskliga immunceller minskade EPS 232 tumörtillväxten effektivare och vid lägre doser än EPS 226. I råttor med en aggressiv bröstcancermodell som uttrycker ultralåga nivåer av HER2 – liknande vissa trippelnegativa bröstcancerformer – saktade en anpassad råttversion av EPS 232 inte bara tumörtillväxt mer än sin föregångare, utan förlängde också överlevnaden. Tumörer från behandlade djur visade ökad infiltration av T‑celler och makrofager, vilket indikerar att den förbättrade antikroppen var bättre på att omforma tumörmiljön till en som gynnar immunangrepp.
Vad detta betyder för framtida cancerterapier
För en allmän läsare är huvudbudskapet att finjustering av hur hårt en IgE-antikropp greppar sitt cancermål kan göra verklig skillnad för hur väl den fungerar, även om IgE redan bildar många samtidiga kontakter med celler. Studien identifierar EPS 232 som en ledande kandidat för IgE-läkemedel mot HER2-positiv och HER2‑low bröstcancer, inklusive former som i dag saknar bra behandlingsalternativ. Mer generellt visar den att "allergi‑stil" antikroppar kan konstrueras med rätt balans i bindningsstyrka för att förvandla ett lättutlöst system som vanligtvis orsakar nysningar till ett som hjälper immunsystemet att söka upp och eliminera tumörer.
Citering: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
Nyckelord: terapeutisk IgE, HER2 bröstcancer, antikroppsaffinitet, cancerimmunterapi, trippelnegativ bröstcancer