Clear Sky Science · sv
Mot helt automatisk syntetisk ECV‑kvantifiering: en öppen maskininlärningsbaserad metod för snabb, blodprovfri CMR
Varför detta är viktigt för hjärthälsan
Läkare förlitar sig i ökande grad på hjärt‑MRI för att upptäcka tidig ärrbildning i hjärtmuskeln, en subtil förändring kopplad till många allvarliga hjärtsjukdomar. I dag kräver denna information vanligtvis både tidskrävande bildanalys och ett blodprov. Denna studie visar att en dator automatiskt kan läsa särskilda hjärt‑MRI och uppskatta samma information utan blodprov, vilket öppnar för snabbare, mer bekväm och potentiellt mer tillgänglig avancerad hjärtdiagnostik.
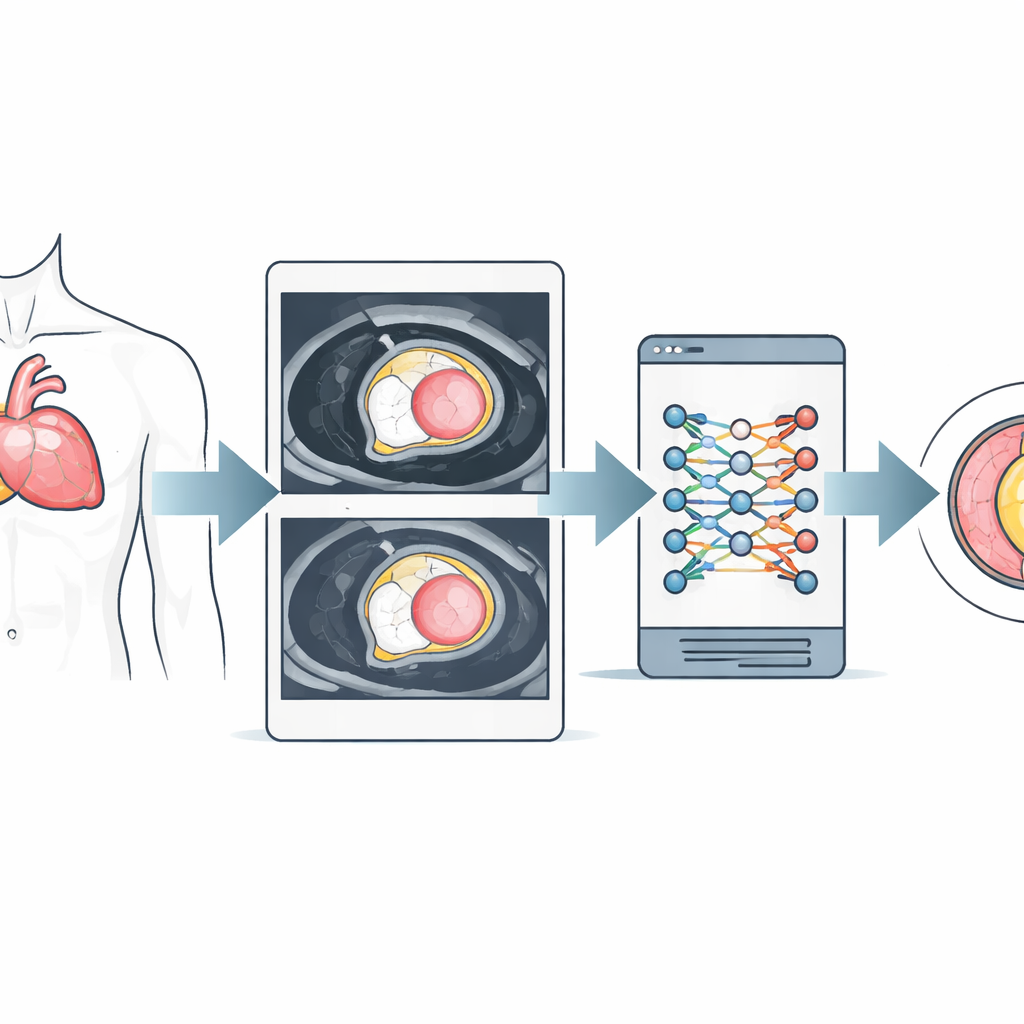
Att se dolda ärr i hjärtat
Många kroniska hjärttillstånd orsakar fibros—små områden av ärrliknande vävnad som stelnar hjärtmuskeln och försämrar långsiktiga utsikter. Modern hjärt‑MRI kan mäta något som kallas extracellulär volym (ECV), vilket speglar hur stor del av hjärtmuskeln som upptas av vätska och fibrös vävnad snarare än friska celler. ECV har blivit en kraftfull bildmarkör för diffus fibros, men att mäta den i praktiken är bökigt. Det kräver vanligtvis manuellt rytande av regioner i flera MRI‑bilder, noggrann korrigering för rörelser och ett aktuellt blodprov för att bestämma hematokrit, andelen röda blodkroppar i blodet.
Problemet med blodprov och manuellt arbete
I verkliga sjukhusmiljöer är detta traditionella arbetsflöde en flaskhals. Inte alla center kan ta ett blodprov i anslutning till MRI‑undersökningen, och hematokrit kan dessutom variera med faktorer så enkla som kroppsställning. Bildanalysen är också beroende av utbildade experter, specialiserad programvara och flera manuella steg där personer skissar upp hjärtats strukturer skiva för skiva. Dessa steg tar tid och kan variera mellan läsare och center, vilket gör det svårare att jämföra resultat mellan sjukhus eller i stora forskningsstudier.
Att lära en dator att läsa hjärtmappar
Byggt på tidigare arbete som visade att hematokrit kan uppskattas direkt från MRI‑signalen i hjärtats blodpool, satte författarna upp att automatisera resten av processen. De använde MRI‑data från över 1000 patienter som undersökts vid två olika magnetfältstyrkor. I träningsfasen skissade experter noggrant upp gränserna för hjärtmuskeln och blodkammare på särskilda T1‑"kartor" tagna före och efter kontrastinjektion. Dessa exempel användes för att träna en djupinlärningsmodell (en U‑net‑typ av neuralt nätverk) att hitta samma strukturer automatiskt. Algoritmen tillämpade också bildbehandlingssteg för att separera blod från närliggande vävnad och något krympa gränserna för att undvika oskärpa från rörelser.
Från råa bilder till syntetisk ECV i ett steg
När modellen var tränad testades den på en separat patientgrupp. För varje person mätte den automatiskt typiska T1‑värden i hjärtmuskeln och blodet, matade in dessa värden i publicerade formler som uppskattar hematokrit från MRI ensam, och beräknade därefter en "syntetisk" ECV—helt utan blodprov eller manuella konturer. Forskarna jämförde denna helt automatiska syntetiska ECV med den konventionella ECV som hade beräknats med expertkonturer och laboratoriemätt hematokrit. Övergripande överensstämde de två metoderna väl: medelvärdena var nästan identiska och korrelationen mellan dem var stark. Överensstämmelsen var särskilt god i det kliniskt viktiga intervallet upp till cirka 35 % ECV, där de flesta patienter ligger.
Vad som fungerade bra och var det kämpar
De automatiska konturerna bedömdes generellt som acceptabla till utmärkta av oberoende hjärtbildspecialister, och modellen hanterade bilder från båda MRI‑fältstyrkorna på ett tillförlitligt sätt. Skillnader mellan de automatiska och konventionella mätningarna ökade dock vid mycket höga ECV‑värden, ett intervall som ofta speglar svår sjukdom. Författarna föreslår att detta delvis beror på att sådana extrema fall var sällsynta i datamängden, och delvis på att bildkvalitet och komplex anatomi kan förvirra algoritmen. De noterar också att referensen i den traditionella metoden använder en liten region i hjärtats septum, medan den automatiska metoden tar medelvärde över hela skivan, vilket naturligtvis ger vissa skillnader.
Vad detta betyder framöver
För närvarande bör denna metod ses som ett forskningsverktyg snarare än en färdig klinisk ersättning. Den visar ändå att en dator kan ta standardiserade pre‑ och postkontrast hjärt‑MRI‑kartor och, utan blodprov och med minimal mänsklig inblandning, producera ECV‑värden som i de flesta patienter följer dagens arbetsintensiva mätningar väl. Eftersom koden och den tränade modellen är fritt tillgängliga kan andra center testa, förfina och anpassa metoden till sina egna skannrar. Om den valideras ytterligare—särskilt hos patienter med mycket hög ECV—kan helt automatisk, blodfri ECV göra bedömningen av avancerad fibros snabbare, mer konsekvent och mer allmänt tillgänglig.
Citering: Beyer, R.E., Hüllebrand, M., Doeblin, P. et al. Towards fully automated synthetic ECV quantification: an open-access machine learning-based approach for fast blood draw-free CMR. Sci Rep 16, 8552 (2026). https://doi.org/10.1038/s41598-026-43624-3
Nyckelord: hjärt‑MRI, myokardfibros, extracellulär volym, djupinlärning, automatisering av medicinsk bilddiagnostik