Clear Sky Science · sv
Naturlig genetisk variation påverkar komplementinhiberande aktivitet hos PFam54-ortologer från asiatiska Borrelia bavariensis
Varför det här är viktigt för Lyme-sjukdomen
Lyme-sjukdomen är redan den vanligaste fästingöverförda infektionen på norra halvklotet, men inte alla bakterier som orsakar Lyme beter sig likadant i våra kroppar. Denna studie undersöker Borrelia bavariensis, en nära släkting till huvudagenten, och ställer en enkel fråga med stora följder: ändrar naturliga genetiska skillnader mellan asiatiska och europeiska stammar hur väl dessa bakterier undviker en av kroppens första försvarslinjer, komplementssystemet i blodet? Svaret hjälper till att förklara hur dessa mikrober sprider sig, hur de orsakar sjukdom och var vi eventuellt kan rikta framtida behandlingar eller vacciner.
En berättelse om två kontinenter
Borrelia bavariensis cirkulerar mellan smådjur och fästingar i Eurasien och kan orsaka Lyme-sjukdom hos människor. Europeiska stammar visar ofta en stark preferens för nervsystemet och dyker upp i fall av neuroborrelios, medan asiatiska stammar verkar mindre knutna till hjärn- och nervinfektioner. Genetiska studier antyder att europeiska stammar härstammar från en mer divergerad asiatisk förfader och att de passerade en flaskhals när de anpassade sig till en annan fästingart i Europa. Denna evolutionära avvikelse kan ha omformat delar av bakteriens genom, inklusive en genkluster kallat PFam54 på en plasmid benämnd lp54. Många PFam54-gener kodar för ytliga proteiner som hjälper bakterierna att överleva i blod genom att störa komplementet, ett proteinnätverk som kan borra hål i angripande celler.
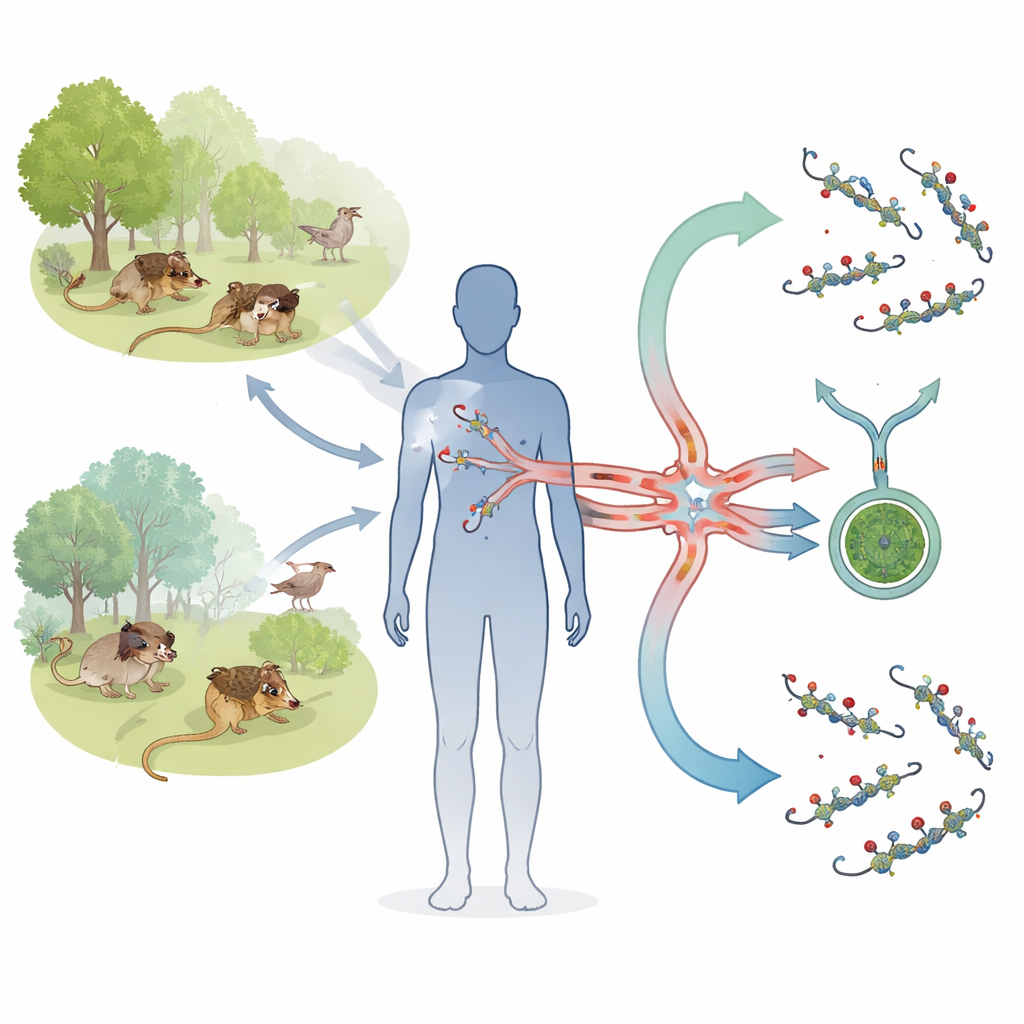
Hur bakterierna undviker blodets angrepp
Komplementsystemet kan föreställas som ett molekylärt larm som, när det utlöses, leder till bildandet av ett ”membranattackkomplex” som borrar porer i bakteriella membran. Tidigare arbete i en europeisk referensstam visade att två PFam54-proteiner, BGA66 och BGA71, sitter på bakterieytan och binder sena komplementkomponenter (C7, C8, C9), vilket blockerar sammansättningen av denna terminala por. Asiatiska B. bavariensis-stammar bär dock ofta en annan uppsättning PFam54-gener, och vissa saknar till och med de exakta BGA66- och BGA71-generna som finns i Europa. Forskarna undrade om dessa asiatiska varianter fortfarande fungerar som komplementsköldar, och om nya, Asien-specifika PFam54-familjemedlemmar kan ge alternativt skydd.
Att utforska mångfalden med genetik och struktur
Forskargruppen skannade först PFam54-gener över flera dussin asiatiska och europeiska B. bavariensis-genom. Som väntat visade asiatiska stammar större sekvensdiversitet i denna familj, men de övergripande mönstren antydde att proteinerna fortfarande är under selektion för att behålla sin grundläggande funktion. Med hjälp av AlphaFold för att förutsäga 3D-strukturer fann de att de asiatiska versionerna av BGA66 och BGA71, liksom flera närbesläktade proteiner, veckade sig till mycket snarlika helixdominerade former trots många aminosyraförändringar. Dessa mutationer tenderade att samlas på ytexponerade regioner—precis där interaktioner med komplement skulle ske—vilket tyder på att finjustering av bindning, snarare än total funktionsförlust, kan ha utvecklats.
Att pröva proteinerna i praktiken
För att se vad dessa skillnader innebar i praktiken uttryckte forskarna asiatiska PFam54-proteiner i bakterier och testade dem i mänskligt serum. Två japanska B. bavariensis-isolat, NT24 och JHM1114, visade sig vara mycket motståndskraftiga mot dödande av aktivt mänskligt komplement, liknande den europeiska referensstammen. Purifierade proteiner från dessa stammar blandades sedan med mänskliga komplementkomponenter i kontrollerade assay. Asiatisk BGA66 kunde fortfarande blockera bildandet av membranattackkomplexet, om än mindre effektivt än sin europeiska motsvarighet. En asiatisk BGA71-variant hindrade delvis ett sent steg i kaskaden men krävde högre doser för att ge effekt. Påfallande nog hämmade ett nytt, enbart asiatiskt protein, BGA67b, starkt den terminala vägen utan att direkt blockera C9-polymerisation, vilket tyder på ett annat sätt att stoppa porbildning. När dessa PFam54-proteiner producerades på ytan av en annars komplementkänslig surrogatstam gjorde de den stammen serumresistent, vilket bekräftade deras skyddande roll.
Vad detta betyder för patienter och framtida forskning
I praktiska termer visar arbetet att både asiatiska och europeiska B. bavariensis-stammar är utrustade med effektiva molekylära ”sköldar” som skyddar dem från att slås sönder av blodets komplement. De specifika sköldproteinerna och deras effektivitet skiljer sig åt, men den övergripande strategin—att störa sent i angreppssekvensen för att förhindra porbildning—är bevarad över kontinenterna. Det innebär att komplementundvikande via PFam54-proteiner ensam inte förklarar varför europeiska stammar oftare kopplas till nervsystemssjukdom. Andra faktorer, såsom ytterligare ytliga proteiner, vävnadstropism eller skillnader i värd- eller fästingekologi, måste också spela in. Samtidigt lyfter studien fram en begränsad uppsättning bevarade proteinformer och interaktionsytor som är avgörande för bakteriens överlevnad i blod och som därför framstår som lovande mål för läkemedel eller vacciner avsedda att blottlägga bakterierna för vårt medfödda immunförsvar.
Citering: Langhoff, L., Kapfer, P., Röttgerding, F. et al. Natural genetic variation impacts complement inhibitory activity of PFam54 orthologs of Asian Borrelia bavariensis. Sci Rep 16, 9080 (2026). https://doi.org/10.1038/s41598-026-43598-2
Nyckelord: Borrelia (Lyme-sjukdom), Borrelia bavariensis, komplementsystemet, immundrägeri, PFam54-proteiner