Clear Sky Science · sv
Stratifiering efter ordinerad dos förbättrar djupinlärningsbaserad VMAT-dosförutsägelse vid lokalt avancerad NSCLC
Varför smartare strålbehandlingar är viktiga
När läkare behandlar avancerad lungcancer med strålning balanserar de mellan att leverera tillräcklig energi för att kontrollera tumören och att skydda känsliga närliggande organ. Att utforma dessa planer är tidskrävande, komplext och beroende av planerarens skicklighet. Denna studie undersöker hur artificiell intelligens kan förutsäga strålningsmönstret i bröstkorgen och visar, vilket är avgörande, att träning av AI med noggrant grupperade dosnivåer gör dess förutsägelser mer precisa och kliniskt användbara.
Hur lungcancer behandlas med fokuserade strålar
De flesta med lokalt avancerad icke-småcellig lungcancer kan inte opereras bort. Istället får de ofta kemoterapi tillsammans med starkt formade strålfält som sveper runt bröstkorgen i bågar — en teknik som kallas VMAT. Målet är att ge tumören en hög, jämn dos samtidigt som exponeringen för lungor, hjärta, matstrupe och ryggmärg begränsas. Att nå denna balans kräver vanligtvis flera omgångar av försök och justeringar, vilket tar tid och kan fördröja behandlingsbeslut. Om läkare snabbt kunde uppskatta vilket dosmönster som realistiskt kan uppnås för en given patient, skulle de kunna välja bästa behandlingsstrategi tidigare.
Att lära en algoritm att se dosmönster
Forskarna använde djupinlärning, en form av AI som lär sig mönster direkt från bilder. De samlade in CT-bilder och färdiga behandlingsplaner från 72 lungcancerpatienter behandlade med VMAT. För varje patient beräknade de om hur samma strålningskonfiguration skulle leverera tre olika totaldoser: 50, 54 och 60 gray (Gy), de standardenheterna för strålning. Varje fall konverterades till ett tredimensionellt rutnät som markerade tumören, viktiga organ och den underliggande CT-bilden. Dessa nio informationskanaler matades in i en 3D U-Net, en vanlig nätverksarkitektur som kan lära sig hur dos tenderar att fördelas genom kroppen utifrån anatomiska förhållanden.
Varför gruppering efter ordinerad dos spelar roll
En central fråga var hur man hanterar att patienter ordineras olika totaldoser. Teamet byggde fyra i övrigt identiska AI-modeller. Tre var ”enspråksdos”-modeller, var och en tränad endast på planer med en dosnivå (50, 54 eller 60 Gy). Den fjärde modellen blandade 50- och 60 Gy-fallen utan att informera nätverket om vilken ordination det rörde sig om. Vid test på nya patienter matchade de dospecifika modellerna verklig dos i tumören bättre, med både täckning och högdosområden nära de kliniska planerna, vanligtvis inom ett fåtal Gy. I kontrast gjorde den blandade modellen märkbart större fel i tumörens högst doserade regioner och runt ryggmärgen, där dosen måste hållas under strikta säkerhetsgränser.
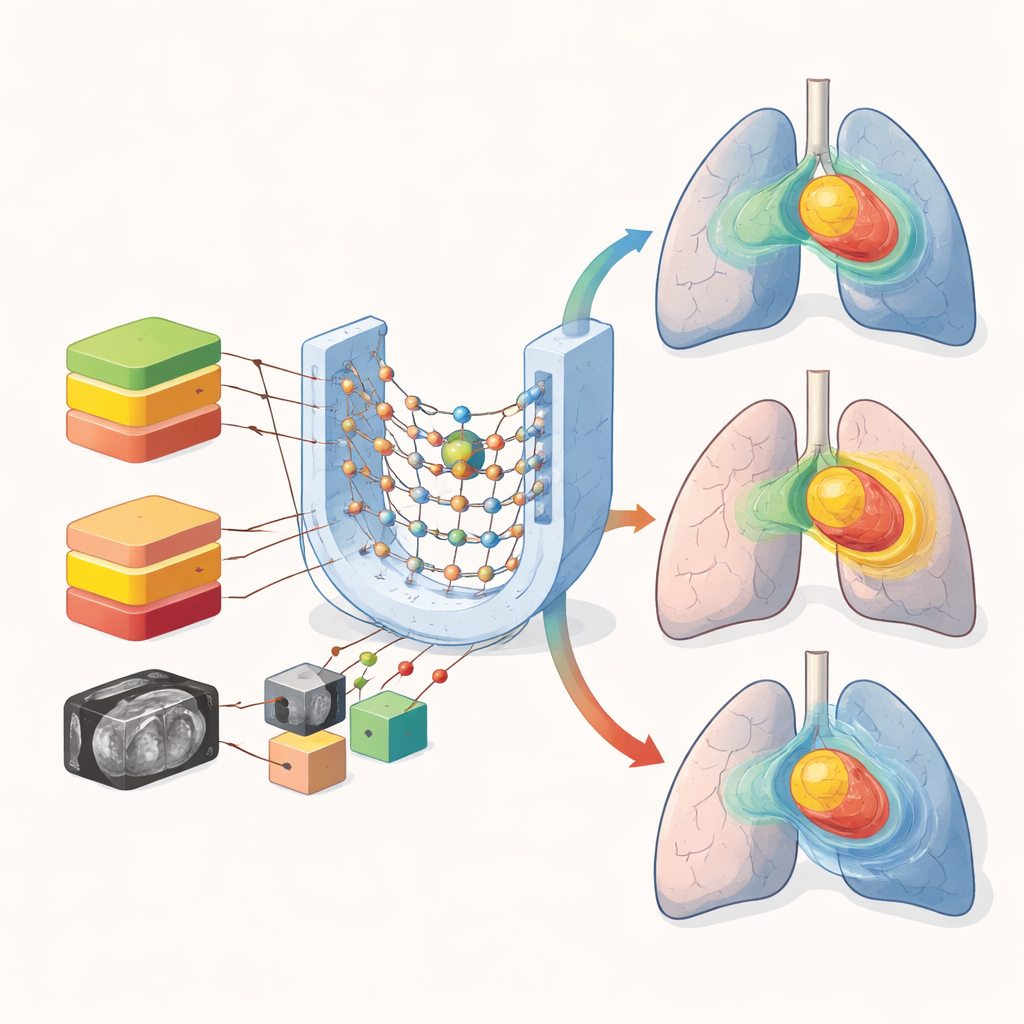
Skydda viktiga organ samtidigt som planeringen snabbas upp
Intressant nog presterade de blandade och stratifierade modellerna likartat för många organ som lungor, hjärta och matstrupe. Genomsnittliga dosfel för dessa större strukturer förblev måttliga över alla angreppssätt. Den största svagheten med att blanda ordinationer framträdde i små, känsliga strukturer som ryggmärgen, där en brant dosavklingning är essentiell. Visuella granskningar av de förutsagda doskartorna visade att alla modeller fångade den övergripande formen av högdosregionen i tumören, men att blandning av ordinationer ledde till mer oskärpa i skarpa gradienter och i lungornas lågdosområden. Dessa skillnader, även om de är subtila numeriskt, kan spela roll när läkare avgör om en högre ordination är säker.
Vad detta betyder för patienter och kliniker
För patienter ersätter detta inte de noggranna dosberäkningar som kliniska system redan utför, men det kan hjälpa till att säkerställa att tid och resurser läggs på planer som faktiskt är genomförbara och säkra. Genom att visa att gruppering av träningsdata efter ordinerad dos avsevärt skärper AI-förutsägelser — särskilt för tumörtäckning och skydd av ryggmärgen — belyser studien ett praktiskt designval som kan göra datorstöd mer pålitligt. Med vidare testning i större och mer varierade patientgrupper kan sådana modeller bli vardagsverktyg som ger läkare en snabb, anatomibaserad förhandsvisning av sannolika strålningsavvägningar och stödjer bättre, mer konsekvent planering.
Citering: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Nyckelord: strålbehandling för lungcancer, djupinlärning dosförutsägelse, VMAT-planering, optimering av behandlingsplan, riskorgan