Clear Sky Science · sv
Utforska den dubbla rollen för extracellulära vesiklar i koagulation och immunmodulation vid glioblastom
Varför blodproppar spelar roll vid hjärntumörer
Personer som diagnostiserats med glioblastom, den mest aggressiva formen av hjärntumör, står ofta inför en oväntad fara: farliga blodproppar i benen eller hjärnan. Dessa proppar kan förkorta överlevnad och komplicera redan krävande behandlingar. Denna studie ställer en enkel men avgörande fråga: vad är det hos glioblastomceller som gör att blodet runt dem så lätt bildar proppar, och hur förändrar de små partiklar de släpper ut i blodet även kroppens immunsvar?
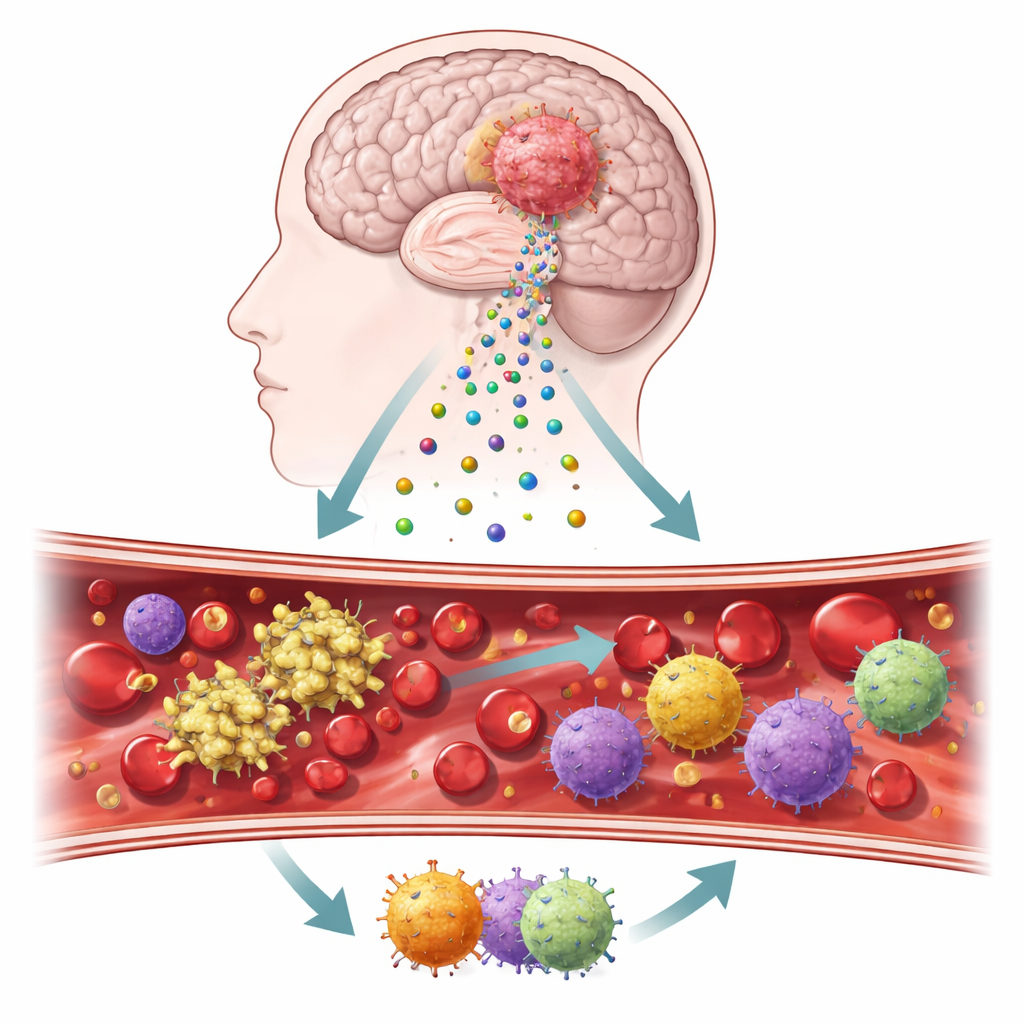
Små budbärare som lämnar en hjärntumör
Forskarna fokuserade på mikroskopiska blåsor kallade extracellulära vesiklar, som avknoppas från tumörceller och färdas genom blod och hjärnvävnad. Dessa vesiklar bär på sin yta två nyckelproteiner, tissue factor och podoplanin, som är kända för att utlösa koagulation och påverka inflammation. Med tumörprover, blod insamlat under operation och cellkulturer odlade från patienternas tumörer byggde teamet ett stegvis arbetsflöde för att följa hur dessa molekyler beter sig hos verkliga patienter och i kontrollerade laboratorietester. De jämförde också tumörvävnad med normal hjärnvävnad för att se hur starkt dessa proppkopplade signaler var aktiverade.
En tyst blodström men en förberedd tumörzon
Standardtester på sjukhuset antydde att många patienters blod såg överraskande normalt ut före operation: vanliga koagulationstider och mått på proppstyrka låg i stort sett inom referensintervallen. När forskarna granskade tumörerna själva framträdde dock en annan bild. Glioblastomvävnad visade konsekvent höga nivåer av tissue factor och podoplanin och mycket låga nivåer av en naturlig broms kallad tissue factor pathway inhibitor. Patient‑härledda tumörcellinjer behöll i stor utsträckning detta mönster i odling, vilket bekräftar att den "proppvänliga" signaturen är en inneboende egenskap hos cancercellerna. När dessa celler, eller de vesiklar de frisatte, blandades med plasma i laboratoriet bildades proppar snabbare, särskilt via den så kallade extrinsiska vägen som är beroende av tissue factor.
Olika tumörceller, olika koagulationsstrategier
Alla glioblastom beter sig inte på samma sätt. Vissa patient‑härledda cellinjer hade mycket höga nivåer av tissue factor, andra hade mer podoplanin, och vissa hade lite av båda. Celler rika på tissue factor var mest effektiva på att förkorta koagulationstiden, medan podoplanin‑rika celler bidrog måttligt via effekter på trombocyter. När en sådan cellinje sorterades i undergrupper som uttryckte endast tissue factor, endast podoplanin, båda eller inget av dem, höll sig inte grupperna stabila särskilt länge. Under tre veckor gled de tillbaka mot blandade profiler, vilket visar en hög grad av plasticitet. Denna dynamiska omformning åtföljdes av förändringar i oxidativ stress inom cellerna, vilket antyder att kemisk stress i tumören kan pressa cellerna mot mer pro‑koagulerande tillstånd.
Vesiklar som formare av hjärn‑ och blodimmunitet
Teamet zoomade sedan in på hur tumör‑härledda vesiklar påverkar hjärnans egna immunceller, kallade mikroglia, samt cirkulerande vita blodkroppar och neutrofiler. Vesiklar från starkt pro‑koagulerande tumörlinjer togs lätt upp av mikroglia och saktade ner deras migration, samtidigt som de skiftade dem mot ett mer inflammatoriskt, "M1‑likt" tillstånd och tecken på cellulär åldrande. I blodomloppet aktiverade vesiklar rika på tissue factor leukocyter, ökade produktionen av reaktiva syreradikaler och främjade frisättningen av klibbiga nätliknande strukturer från neutrofiler, kända som extracellulära fällor. Vesiklar som bar podoplanin var mindre kraftfulla i att driva dessa explosiva immunreaktioner men uppmuntrade starkt ett senescensliknande program, där immunceller slutar dela sig och ändrar sitt beteende. Även vesiklar som saknade båda nyckelproteinerna kunde fortfarande framkalla viss senescens, vilket antyder att annat innehåll också spelar roll.
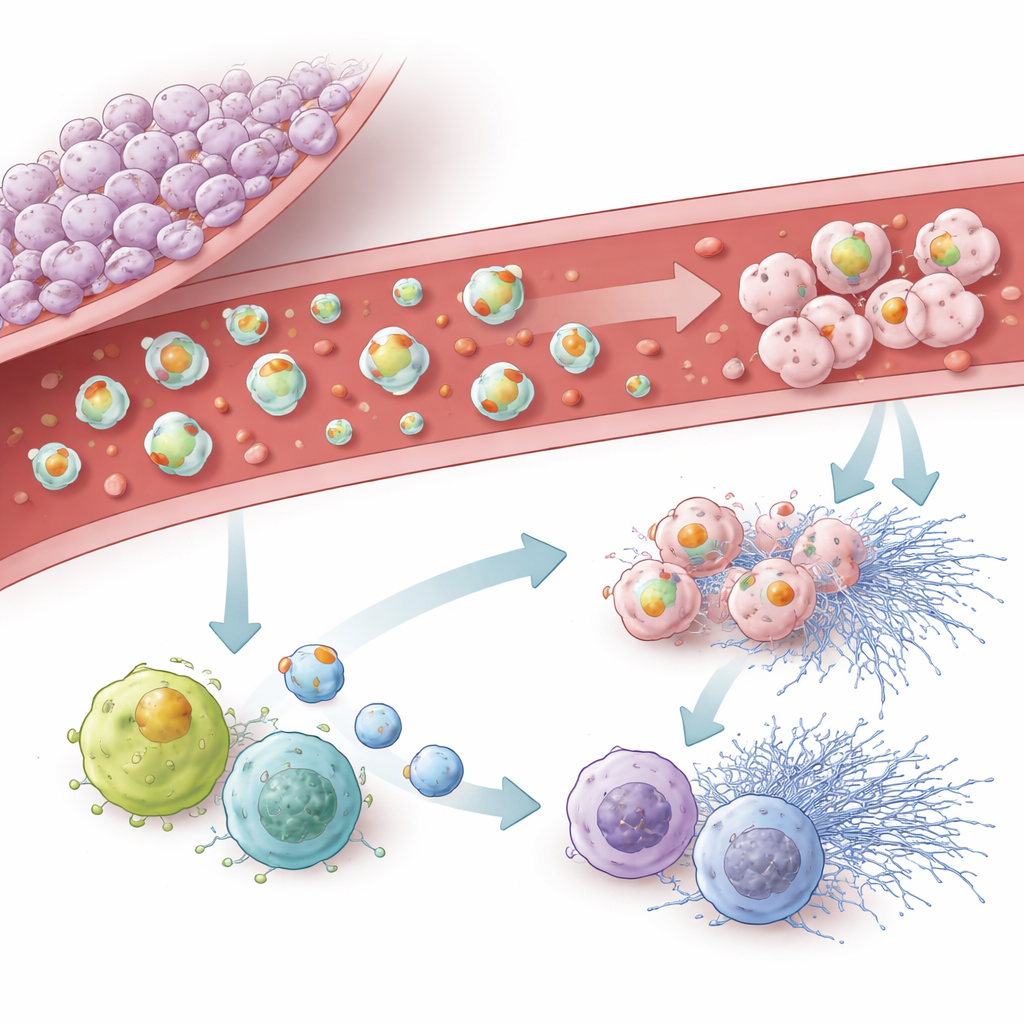
Vad detta betyder för patienter och framtida vård
Sammantaget visar resultaten att glioblastom inte helt enkelt förtjockar blodet överallt. Istället skapar tumören och de vesiklar den frigör en lokaliserad, mycket komplex zon där koagulation och inflammation matar varandra. Tissue factor framstår som huvudmotorn för proppbildning och inflammatorisk aktivering, medan podoplanin bidrar med sin egen påverkan på trombocyter, immunåldrande och mikroglialt beteende. Eftersom dessa vesiklar cirkulerar och speglar tumörens tillstånd kan de fungera som framtida blodbaserade markörer för att identifiera patienter med särskilt hög risk för proppar. De kan också peka mot mer skräddarsydda förebyggande strategier som riktar sig mot tumörens pro‑koagulerande mekanismer utan att allmänt tunna ut blodet.
Citering: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Nyckelord: glioblastom, blodproppar, extracellulära vesiklar, tumörmikromiljö, immunrespons