Clear Sky Science · sv
Utvärdering av Mycobacterium tuberculosis dodecin-stomme som en multimeriseringsplattform för immunogeniciteten hos HPV L2-antigener
Varför denna forskning är viktig för framtida vacciner
Humant papillomvirus (HPV) orsakar nästan alla fall av livmoderhalscancer och en ökande andel av andra cancerformer, men dagens vacciner är komplicerade att tillverka och täcker inte fullt ut alla farliga virustyper. Denna studie undersöker ett nytt sätt att bygga ett enklare, bredare skyddande HPV-vaccin som kan bli billigare, mer stabilt och lättare att använda globalt, särskilt i låg- och medelinkomstländer. Genom att omorganisera hur viktiga virala proteindelar visas för immunsystemet syftar forskarna till att stimulera kroppen att framställa kraftfulla antikroppar mot många HPV-typer samtidigt.
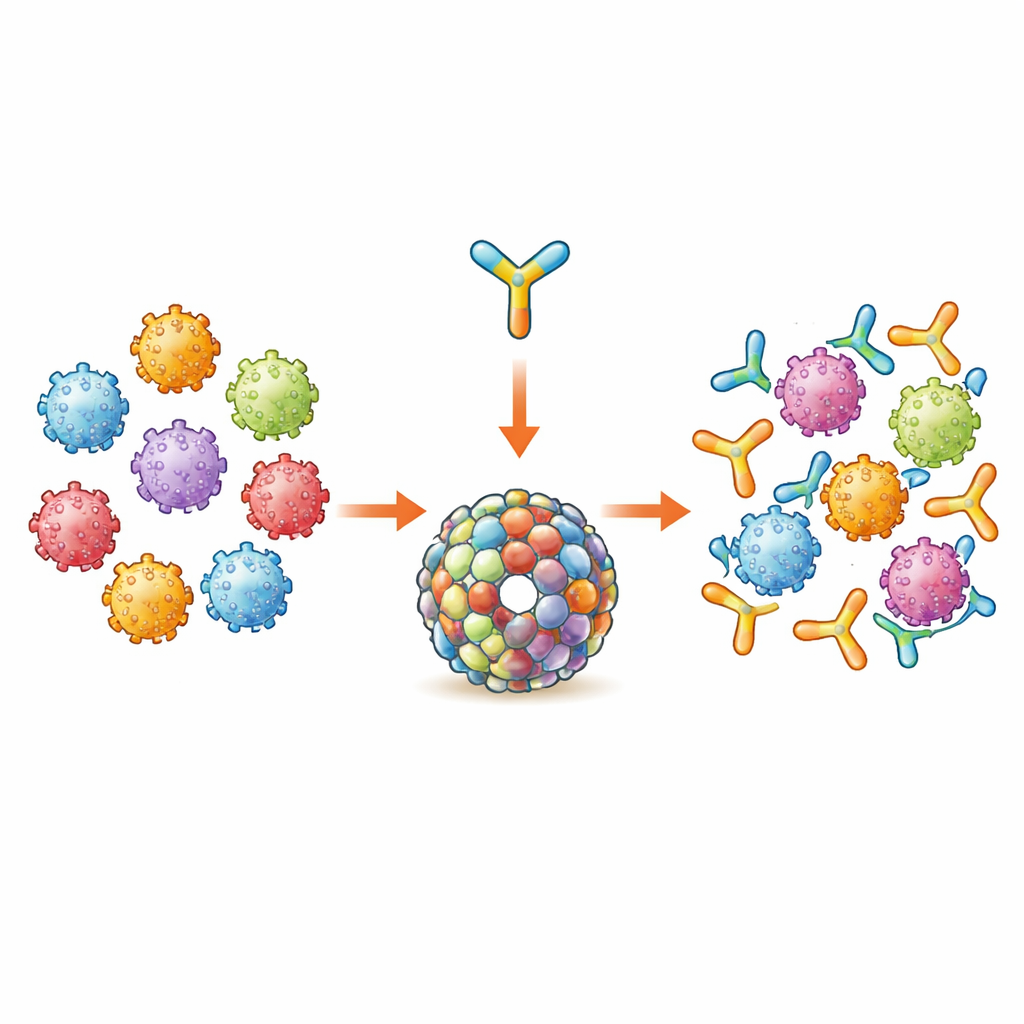
En ny byggsten för HPV-skydd
Dagens HPV-sprutor förlitar sig på ett viralt skalprotein kallat L1, som monteras till virusliknande partiklar som kraftigt stimulerar antikroppar men i huvudsak riktar sig mot de få HPV-typer som ingår i varje vaccin. Teamet fokuserade istället på ett andra viralt protein, L2, som innehåller korta regioner som är likartade över många HPV-typer och därför kan ge bredare skydd. De använde ett tidigare designat antigen kallat Trx-8mer, där små bevarade L2-segment från åtta HPV-typer är hopsydda och visade på ett stabilt bärareprotein. Tidigare arbete hade redan visat att sju av dessa Trx-8mer-enheter hopade i en ringformad komplex (ett vaccin kallat PANHPVAX) ger starka, korsskyddande antikroppssvar och nu testas i tidiga fasstudier på människor.
Att göra ett bakterieprotein till en vaccinplattform
I denna studie försökte forskarna gå bortom sju kopior och packa ännu fler L2-antigener i varje partikel, utifrån teorin att mycket repetitiva mönster är särskilt bra på att aktivera B-celler, immunsystemets antikroppsproducerande celler. De valde ett litet, värmetåligt protein från tuberkulosbakterien, kallat dodecin, som naturligt monterar sig till ihåliga bollar bestående av tolv identiska subenheter. Genom att genetiskt förena Trx-8mer med dodecin skapade de flera nya vaksinkandidater avsedda att självsamla till multimeriska nanopartiklar som visar många kopior av L2. Dessa partiklar kunde produceras i bakterier, renas vid hög temperatur tack vare deras robusthet, och verifieras med flera biofysiska metoder för att bilda de avsedda nanoskaliga strukturerna.
När direkt fusion inte räcker
Överraskande nog gav det inte bättre effekt att enkelt fästa L2-last direkt på dodecin-stommen jämfört med det befintliga heptameriska referensvaccinet PANHPVAX hos möss. Trots att de multimeriska partiklarna bildades som planerat och inducerade neutraliserande antikroppar mot både vaccinskylda och icke-vaccinskylda HPV-typer var titrarna generellt lägre än de som observerades med PANHPVAX. Att lägga till en inbyggd hjälp-T cells-epitop, vilket ibland stärker antikroppssvar, förbättrade heller inte prestationen. Strukturell modellering och funktionella data föreslog att skrymmande, direkt fästa Trx-8mer-enheter kan tränga ihop varandra och dölja kritiska L2-regioner för B-cellreceptorer, vilket försvagar immunsvaret trots att fler antigenkopior teoretiskt finns närvarande.
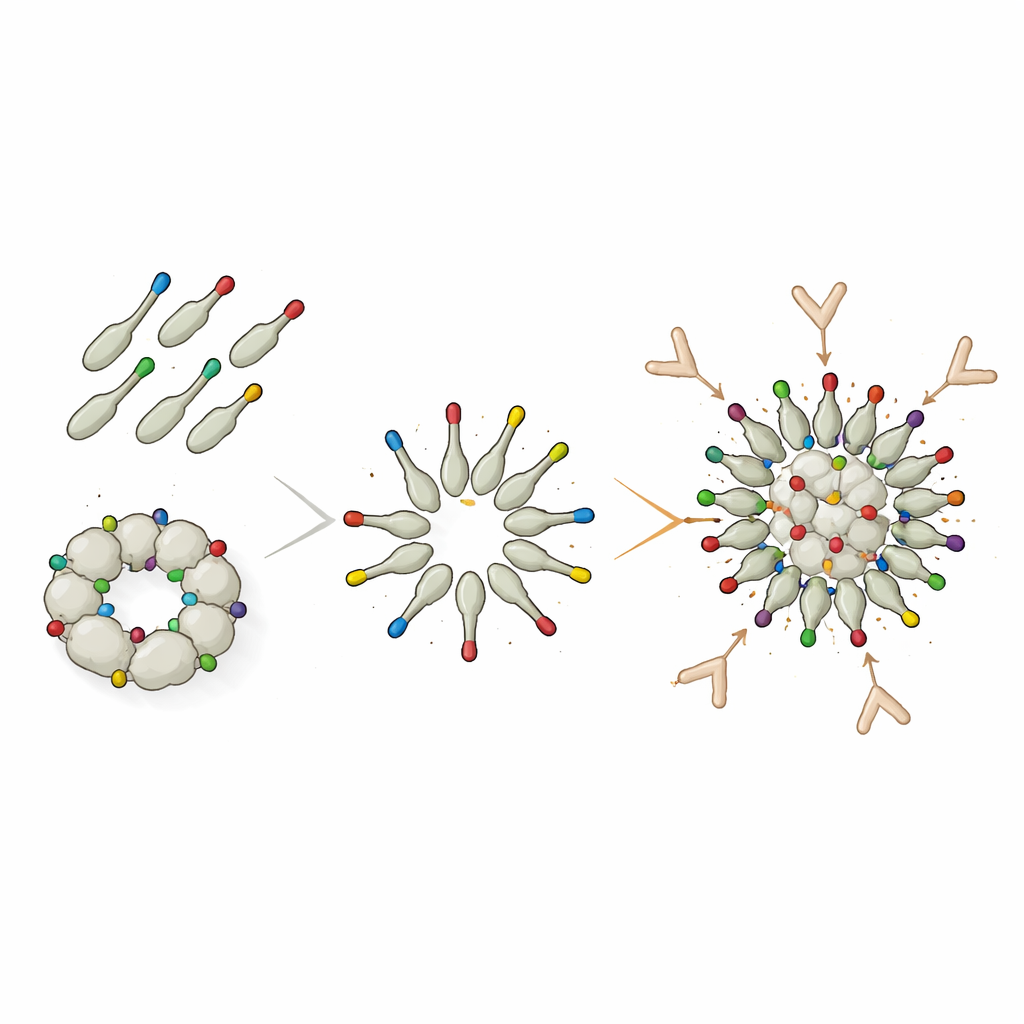
Klick-på-dekoration ger dramatiskt bättre svar
För att övervinna dessa strukturella begränsningar bytte teamet till ett modulärt "proteinlim"-system kallat DogTag/DogCatcher. I denna design producerades dodecin först med endast en liten DogTag-peptid på ytan, vilket tillät att den fritt kunde montera sig till rena nanopartiklar. Separat fusionsades Trx-8mer-antigenet med den matchande DogCatcher-partnern. När de blandades låste sig Tag och Catcher ihop via en spontan kovalent bindning och snäppte fast de L2-bärande Trx-8mer-enheterna på de förmonterade dodecin-partiklarna. Trots att endast omkring hälften av Trx-8mer faktiskt fäste på nanopartiklarna och resten förblev fritt i lösning, producerade möss som immuniserades med denna dekorerade konstruktion mycket högre neutraliserande antikroppstitrar mot flera högrisk-HPV-typer än med direktfusionspartiklarna. För vissa typer, såsom HPV16, överträffade de dekorerade partiklarna till och med PANHPVAX.
Konsekvenser för prisvärda, breda HPV-vacciner
Sammantaget visar studien att hur antigener är arrangerade i rummet kan vara viktigare än hur många kopior som finns på pappret. Att förmontera ett tåligt nanopartikelskelett och sedan snäppa på antigener gav L2-fragmenten bättre avstånd och orientering, vilket ledde till starkare och bredare antikroppssvar hos möss. Eftersom dodecin-baserade partiklar är små, mycket termostabila och produceras i bakterier är de lovande kandidater för nästa generations HPV-vacciner som kan bli billigare att tillverka och mindre beroende av kylkedja. Med ytterligare förfining och testning skulle denna modulära plattform kunna stödja vacciner som skyddar mot många HPV-typer i en enda, lättillgänglig spruta, och kanske även anpassas för att kombinera preventiva och terapeutiska komponenter i samma partikel.
Citering: Kaplan, E., Mariz, F.C., Zhao, X. et al. Assessment of Mycobacterium tuberculosis dodecin scaffold as a multimerization platform on the immunogenicity of HPV L2 antigens. Sci Rep 16, 9086 (2026). https://doi.org/10.1038/s41598-026-42678-7
Nyckelord: HPV-vaccin, nanopartikel-immunogen, L2-antigen, dodecin-stomme, proteinkonjugering