Clear Sky Science · sv
Kartläggning av nattliga uppvaknanden vid sömn- och smärtsjukdomar
Varför oroliga nätter spelar roll
De flesta av oss tänker på sömn som ett jämnt, tyst tillstånd, men under ytan ställer hjärnan ständigt in hur djupt vi vilar. Små aktivitetsutbrott — korta "rörigheter" som inte väcker oss helt — hjälper till att hålla sömnen stabil. Den här studien undersöker hur dessa dolda rörigheter utvecklas över natten i flera tillstånd kopplade till störd sömn: en rörelsestörning där drömmar ageras ut, narkolepsi, nattskräck och sömngång, samt den kroniska smärttillståndet fibromyalgi. Genom att följa dessa ögonblick-till-ögonblick-förändringar istället för att bara räkna timmar i varje sömnstadium hoppas författarna avslöja mönster som en dag kan vägleda diagnos och behandling.
Den dolda rytmen i djupsömn
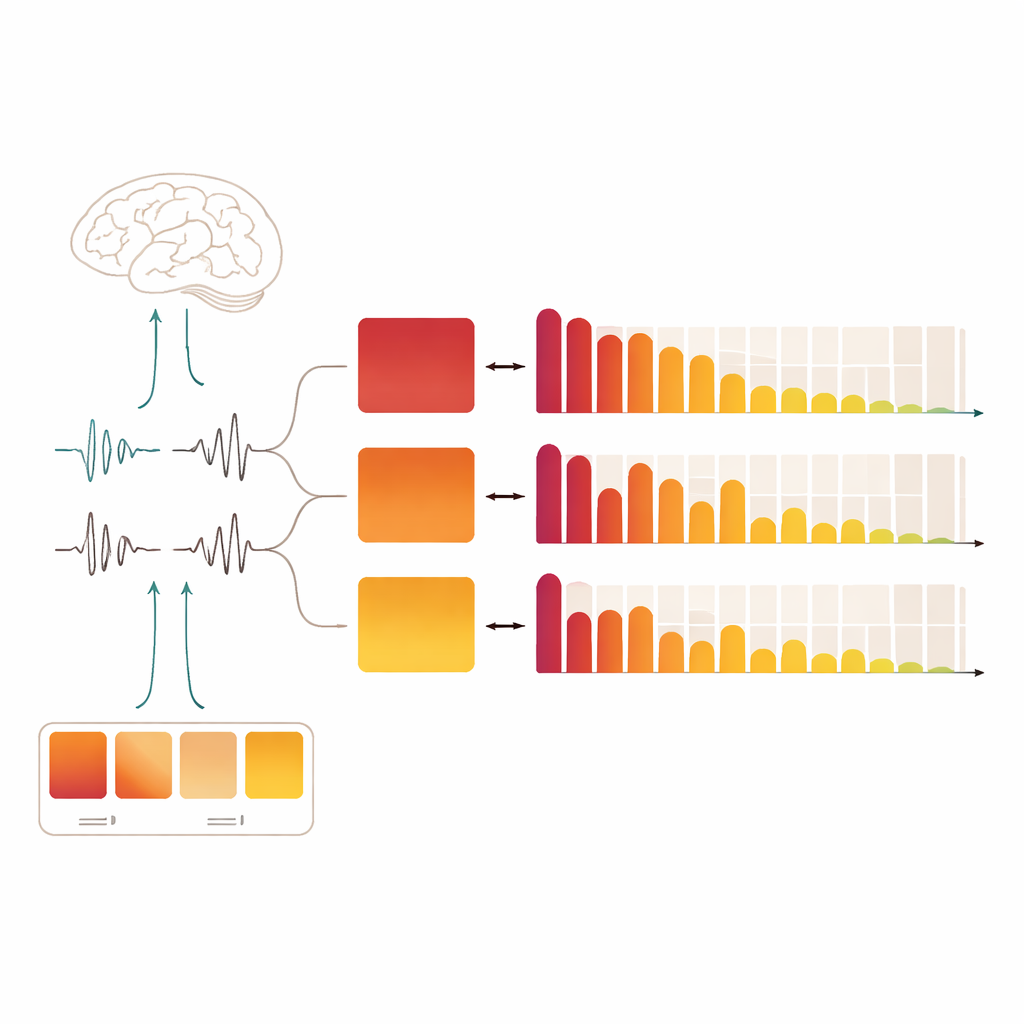
Under icke-REM-sömn alternerar hjärnan mellan lugnare perioder och korta aktivitetsblixtar. Sömnforskare kallar detta det cykliska alternerande mönstret: korta "A‑faser" av aktivering följda av lugnare "B‑faser." Inom A‑faserna framträder tre varianter. Den första subtypen, A1, är starkt kopplad till långsamma, högamplitudvågor och tros hjälpa till att stabilisera djupsömnen. De andra två, A2 och A3, speglar successivt starkare aktivering och för hjärnan närmare uppvaknande. Istället för att betrakta dessa händelser som slumpmässigt brus ser nyare arbete dem som en nyckel till hur hjärnan balanserar att förbli sömnig med att vara lyhörd för omvärlden.
Ett nytt sätt att följa nattligt uppvaknande
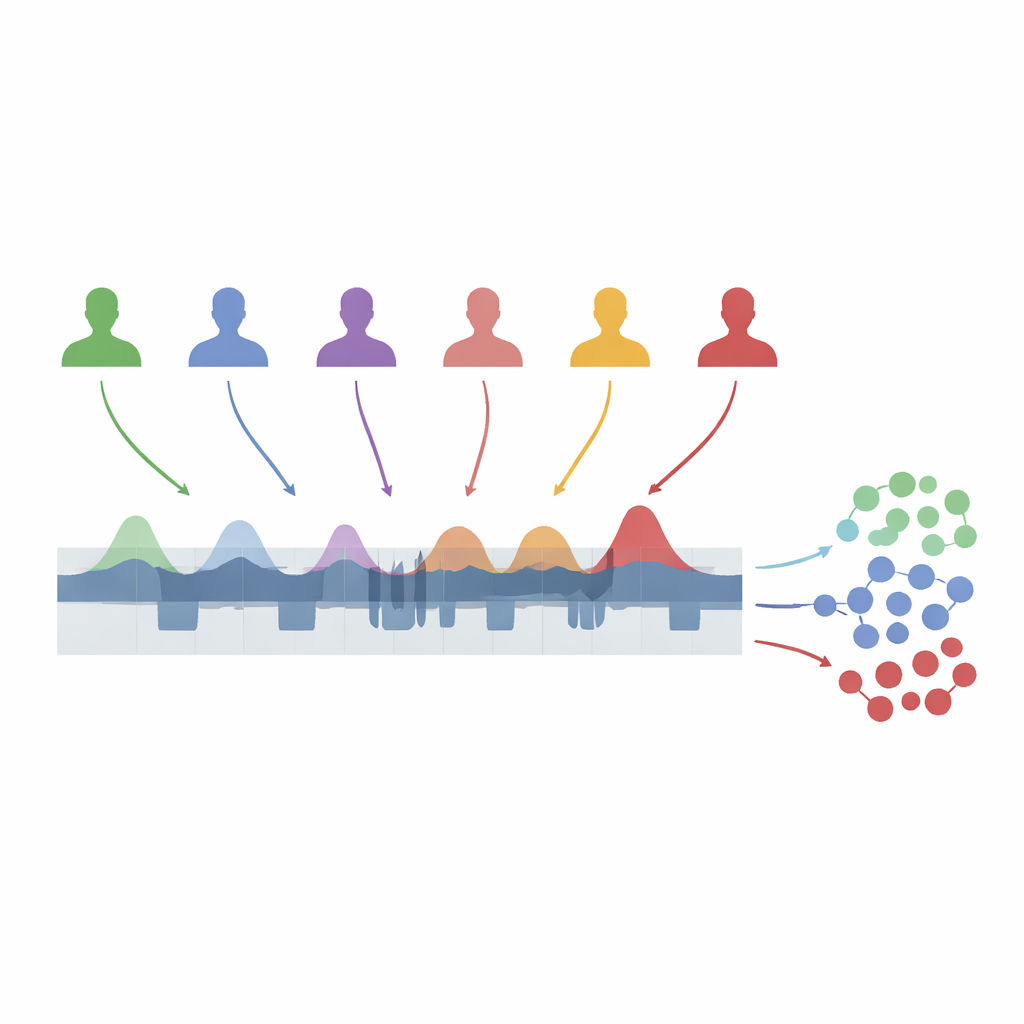
Forskarna analyserade nattliga EEG‑inspelningar från 109 vuxna: friska frivilliga och patienter med idiopatisk REM-sömnbeteendestörning, narkolepsi typ 1, icke-REM-parasomnier och fibromyalgi. Med en automatiserad algoritm tränad på expertmärkta data detekterade de varje ögonblick när hjärnan gick in i A1, A2 eller A3 under icke-REM-sömn. De delade sedan varje persons natt i ettminutsblock och beräknade för varje block vilken andel av tiden som tillbringades i respektive subtyp. Detta "A‑fasindex" ger ett löpande mått på hur mycket hjärnan aktiveras kortvarigt, utan att försöka rekonstruera varje full cykel av aktivering och vila. För att kunna jämföra personer med mycket olika insomningstid och sömnlängd sträckte författarna ut varje natt på en standardiserad skala från släckt ljus till tändt ljus.
Hur olika störningar omformar nattens förlopp
Hos friska sömnare var A1-händelser vanligast tidigt på natten, när sömnttrycket är högt, och avtonade sedan stadigt mot morgonen. Det stämmer med idén att starka, långsamma vågor hjälper till att stabilisera de första djupsömnscyklerna och därefter behövs mindre när hjärnan återhämtat sig. Över alla deltagargrupper var A2 och A3 mindre framträdande och ändrade sig mer måttligt över tiden. I kontrast visade alla fyra kliniska tillstånd en utjämnad version av det friska A1-mönstret. Personer med REM-sömnbeteendestörning och de med narkolepsi hade märkbart färre A1- och A2-händelser i mellan-djupet av icke-REM-sömnen, och de med REM-sömnbeteendestörning saknade också A1 i det djupaste stadiet. Fibromyalgi visade en bred nedgång i både A1 och A2, särskilt i detta mellan-djupa stadium. Icke-REM-parasomnierna stack ut: de visade en tidig nattlig topp i A1 och A2 under lätt sömn, men senare en minskning av A1 i djupsömn. Tillsammans tyder dessa profiler på att varje störning har sitt eget "fingeravtryck" av hur hjärnans korta uppvaknandeblott är invävda genom natten.
Vad mönstren kan betyda för hjärnan
Dessa störningsspecifika fingeravtryck pekar mot olika slags obalanser mellan system som främjar djupa, återhämtande långsamma vågor och system som driver hjärnan mot aktivering. Minskade A1 och A2 vid REM-sömnbeteendestörning och narkolepsi kan spegla svagare rekrytering av stabiliserande slow-wave‑svar, vilket gör sömnen mer skör även när den totala tiden i djupsömn ser normal ut. Vid parasomnier stämmer kombinationen av extra aktivering i lätt sömn och svagare buffring i djupsömn med idén om instabila gränser mellan sömn- och vakentillstånd, vilket kan ge upphov till dramatiska beteenden som sömngång. Vid fibromyalgi kan den utbredda förlusten av A1 och A2 bidra till att förklara varför sömnen upplevs som otillfredsställande trots till synes normala mängder djupsömn: den fintäta, skyddande mikrostrukturen är förändrad, vilket potentiellt ökar känsligheten för smärta och andra sinnesintryck.
Från beskrivande kartor till framtida sömnverktyg
Författarna understryker att arbetet är explorativt: gruppstorlekarna var måttliga, de friska frivilliga var inte perfekt matchade med patienterna, och de fokuserade endast på de aktiva A‑faserna, inte på de fullständiga cyklerna som inkluderar de lugnare B‑faserna. Ändå visar resultaten att det att följa upp- och nedgången av korta uppvaknandehändelser över natten kan avslöja distinkta signaturer för olika sömn- och smärtsjukdomar. Om detta bekräftas i större, prospektiva studier skulle denna typ av natt‑lång kartläggning kunna bidra till nya biomarkörer — objektiva mått som hjälper till att klassificera patienter, följa sjukdomsutveckling och styra behandlingar som finjusterar balansen mellan stabilitet och aktivering i sömnen snarare än att bara slå ut människor.
Citering: Biabani, N., Mendonça, F., Mutti, C. et al. Mapping nocturnal arousal across sleep and pain disorders. Sci Rep 16, 8668 (2026). https://doi.org/10.1038/s41598-026-42639-0
Nyckelord: sömnmikrostruktur, nattligt uppvaknande, cykliskt alternerande mönster, sömnstörningar, fibromyalgi och sömn