Clear Sky Science · sv
GV1001 minskar patologisk 4R-tau och funktionella underskott i modeller relevanta för progressiv supranukleär pares
Varför detta är viktigt för patienter och familjer
Progressiv supranukleär pares (PSP) är en sällsynt men förödande hjärnsjukdom som berövar människor balans, rörelseförmåga och klart tänkande inom bara några år. Det finns i dag inga läkemedel som kan bromsa sjukdomens förlopp. Denna studie undersöker en liten läkemedelsmolekyl kallad GV1001, ursprungligen utvecklad för cancer, och visar att den kan lindra rörelsestörningar och minska centrala sjukdomsrelaterade förändringar i hjärnceller i laboratoriemodeller av PSP. Arbetet antyder en ny väg för att angripa en grupp sjukdomar drivna av en skadlig form av proteinet tau.
Hjärnans trafikhjälpare som går fel
Många hjärnsjukdomar involverar tau, ett protein som normalt hjälper till att stabilisera de inre ”spåren” längs vilka material färdas inne i nervceller. I PSP byggs en särskild form som kallas 4R-tau upp i vissa djupa hjärnregioner, särskilt i mitthjärnan, där den stör cellstrukturen, skadar förbindelser och i slutändan leder till celldöd. Personer utvecklar stelhet, fall, störningar i ögonrörelser och tänkandestörningar, ofta med snabb försämring över fem till åtta år. Till skillnad från Alzheimers sjukdom domineras PSP av denna 4R-tauform, vilket gör den till ett viktigt mål för behandlingar utformade särskilt för rörelserelaterade taustörningar.
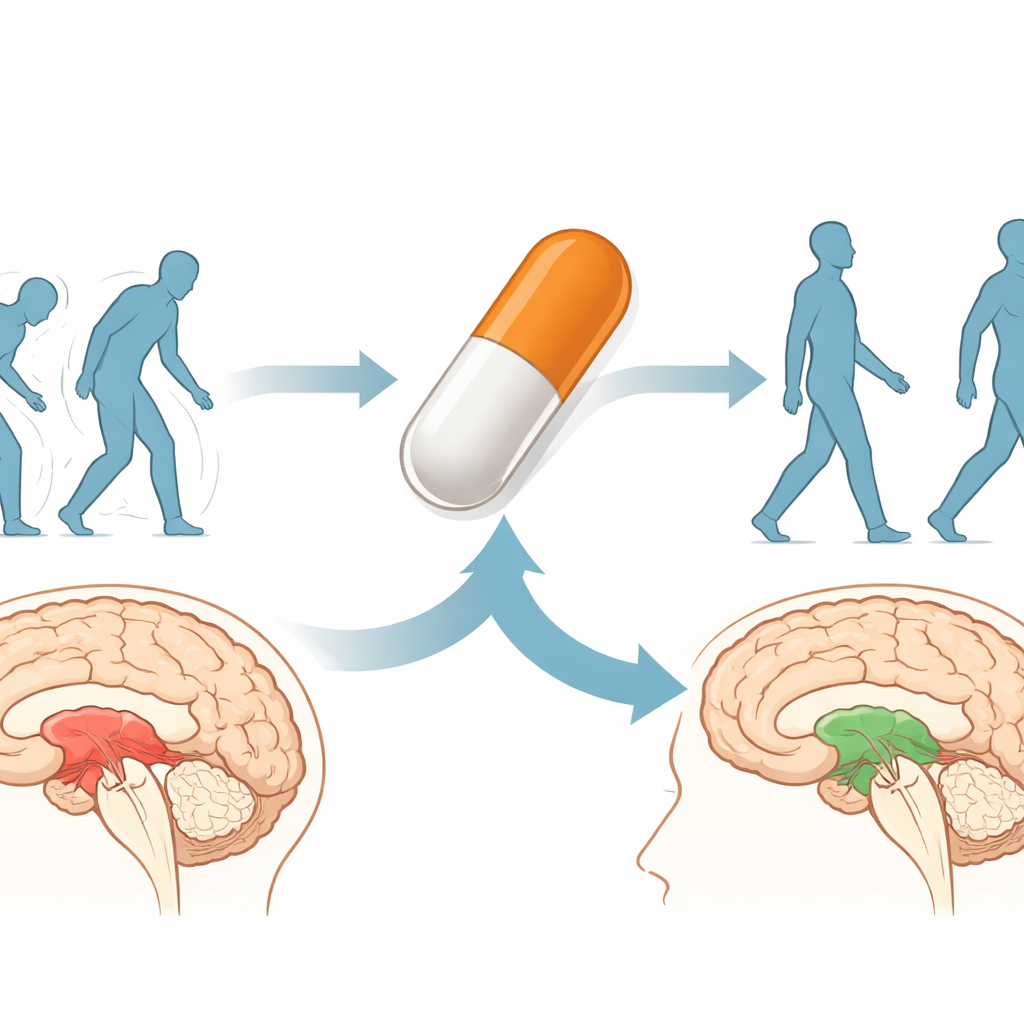
En cancerläkandekandidat hittar en ny roll
GV1001 är ett kort peptidfragment härlett från mänsklig telomeras, ett enzym som är aktivt i många cancerformer. Det har redan prövats vid flera tumörtyper och, mer nyligen, vid tillstånd som förstorad prostata och Alzheimers sjukdom, med en i stort sett god säkerhetsprofil. Tidigare arbete visade att GV1001 kan skydda hjärnceller från oxidativ skada, stödja energiproducerande mitokondrier och dämpa inflammatoriska svar i hjärnan. Den aktuella studien frågar om dessa breda skyddande effekter, plus eventuella nya verkningsmekanismer, kan göra GV1001 användbart vid sjukdomar där 4R-tau är huvudorsaken, såsom PSP.
Test av rörelse, minne och hjärnförändringar hos möss
Forskarna använde en specialkonstruerad mus som producerar en människolik 4R-tau som lätt bildar klumpar, vilket över tid leder till problem med rörelse och minne. Från sju månaders ålder fick dessa möss GV1001 under huden tre gånger i veckan i ungefär fem månader. Jämfört med obehandlade djur stannade GV1001-behandlade möss längre på en roterande stång, gick längre och snabbare i en öppen arena och visade bättre igenkänning av nya föremål, vilket tyder på förbättrad motorik och minnesfunktion. När forskarna undersökte hjärnorna fann de mindre tau-aggregat och färre kemiska markörer för ”överaktiv” tau i flera regioner, inklusive cortex, hippocampus och substantia nigra — alla områden viktiga för rörelse och kognition.
In i cellerna och dämpning av hjärninflammation
Utöver tau i sig kännetecknas PSP och närliggande sjukdomar av förlust av synapser — kontaktpunkterna mellan nervceller — och överaktivering av stödjeceller som astrocyter och mikroglia, vilka driver kronisk inflammation. Hos de behandlade mössen återgick nivåerna av viktiga synaptiska proteiner mot det normala, vilket antyder att GV1001 hjälper till att bevara nervkopplingar. Markörer för aktiverade astrocyter och mikroglia sjönk, både i mushjärnor och i humana cellinjer stimulerade för att efterlikna inflammation. Läkemedlet minskade också nivåerna av TSPO, ett protein som används i hjärnavbildning för att följa inflammation, vilket öppnar möjligheten att framtida avbildning kan övervaka GV1001:s effekt hos patienter.
Direkt inriktning på den skadliga 4R-tauformen
För att testa om GV1001 påverkar 4R-tau mer specifikt skapade teamet en cellbaserad modell av PSP genom att differentiera humana nervliknande celler och utsätta dem för annonacin, ett växtbaserat toxin som skadar mitokondrier och ökar 4R-tau. Som förväntat ökade annonacin kraftigt mängden 4R-tau utan att ändra total tau. När GV1001 tillsattes efter att denna skada börjat avta de förhöjda nivåerna av 4R-tau och kvoten 4R-tau/totalt tau tillbaka mot det normala, medan den totala tau-mängden förblev i stort sett oförändrad. Liknande selektiva minskningar av 4R-tau sågs i hjärnorna hos behandlade möss. Dessa fynd tyder på att GV1001 gör mer än att skydda celler generellt — det verkar dämpa just den tauform som är mest förknippad med PSP.
Vad detta kan innebära för framtida behandlingar
Tillsammans visar resultaten att GV1001 kan förbättra rörelse och minne, minska toxiska tauförändringar, bevara synapser och dämpa hjärninflammation i modeller som efterliknar nyckelaspekter av PSP och andra 4R tau–drivna sjukdomar. Tidig klinisk prövning hos människor med PSP har redan antytt en långsammare symtomutveckling och god tolerabilitet, även om mycket större och längre studier krävs. För patienter och familjer erbjuder detta försiktig optimism om att ett läkemedel ursprungligen designat för cancer kan återanvändas för att bromsa förloppet av en snabbt förlöpande hjärnsjukdom genom att rikta in sig på dess kärnproteinavvikelse.
Citering: Jang, KB., Kang, D.M., Lee, MH. et al. GV1001 reduces pathological 4R tau and functional deficits in models relevant to progressive supranuclear palsy. Sci Rep 16, 8638 (2026). https://doi.org/10.1038/s41598-026-42195-7
Nyckelord: progressiv supranukleär pares, tauprotein, 4R tauopati, neuroinflammation, GV1001