Clear Sky Science · sv
Multicenter klinisk‑patologisk studie av odontogena myxom‑spektrometer med kvantitativ patologi
Varför detta är viktigt för patienter och tandläkare
Djupt inne i käkbenet kan sällsynta tumörer växa tyst i månader eller år innan de upptäcks. Dessa tillväxter, kallade odontogena myxom och myxofibrom, är inte cancer, men de kan expandera, försvaga benet och komplicera kirurgi. I årtionden har patologer bedömt dem huvudsakligen med ögat, vilket lett till skillnader i hur olika sjukhus beskriver och klassificerar samma typ av lesion. Denna studie för in kraftfulla bildanalysverktyg i mikroskopet och visar hur artificiell intelligens (AI) kan hjälpa läkare att se dessa tumörer klarare och mer konsekvent.
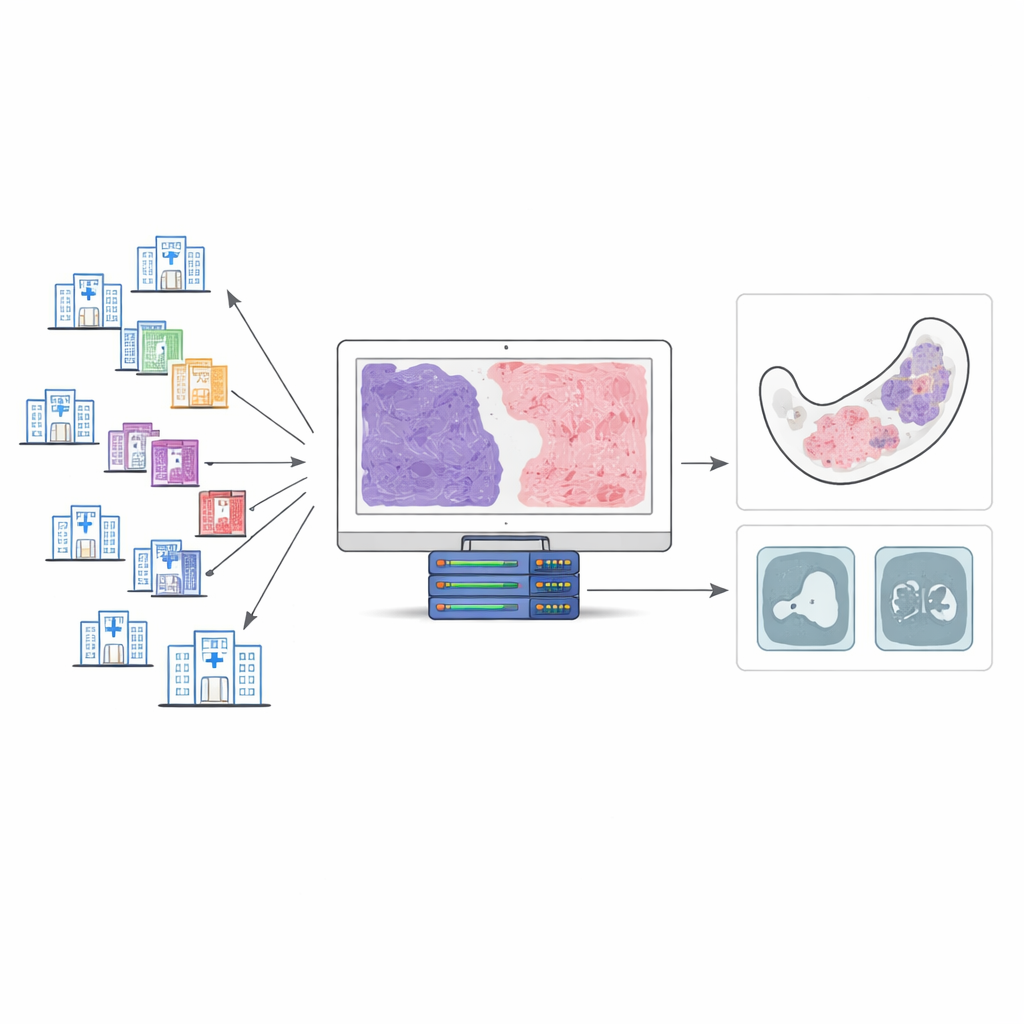
Sällsynta käktumörer som ser bedrägligt lika ut
Odontogent myxom och odontogent myxofibrom har sitt ursprung i vävnader som är involverade i tandbildning. Båda är mjuka, geléliknande tumörer som sitter i käkbenet. Under mikroskopet innehåller de en blandning av lösa, myxoida områden och tätare fibrösa band. Traditionellt har patologer försökt skilja dem åt genom att uppskatta hur mycket av tumören som är fibrös respektive myxoid. Men dessa tumörer är sällsynta, och det finns inga universellt överenskomna regler för hur mycket fibrös vävnad som krävs för att ändra en diagnos från en beteckning till en annan. Som ett resultat kan olika sjukhus ge olika namn åt mycket likartade lesioner, även när patienter har jämförbara symtom och röntgenfynd.
Att förvandla mikroskopglas till siffror
Forskargruppen samlade 143 vävnadsprov från patienter behandlade vid 34 sjukhus över två decennier, och fokuserade slutligen på 100 fall som uppfyllde strikta kvalitetskriterier. Alla prover färgades med ett speciellt färgämne (Massons trichrom) som färgar fibrös vävnad annorlunda än omgivande tumör. Två erfarna orala patologer granskade noggrant varje fall och uppskattade andelen fibrös vävnad i steg om 10 %. Dessa expertskattningar tjänade som referens för att träna ett AI‑system att utföra samma uppgift automatiskt, men på ett helt kvantitativt sätt.
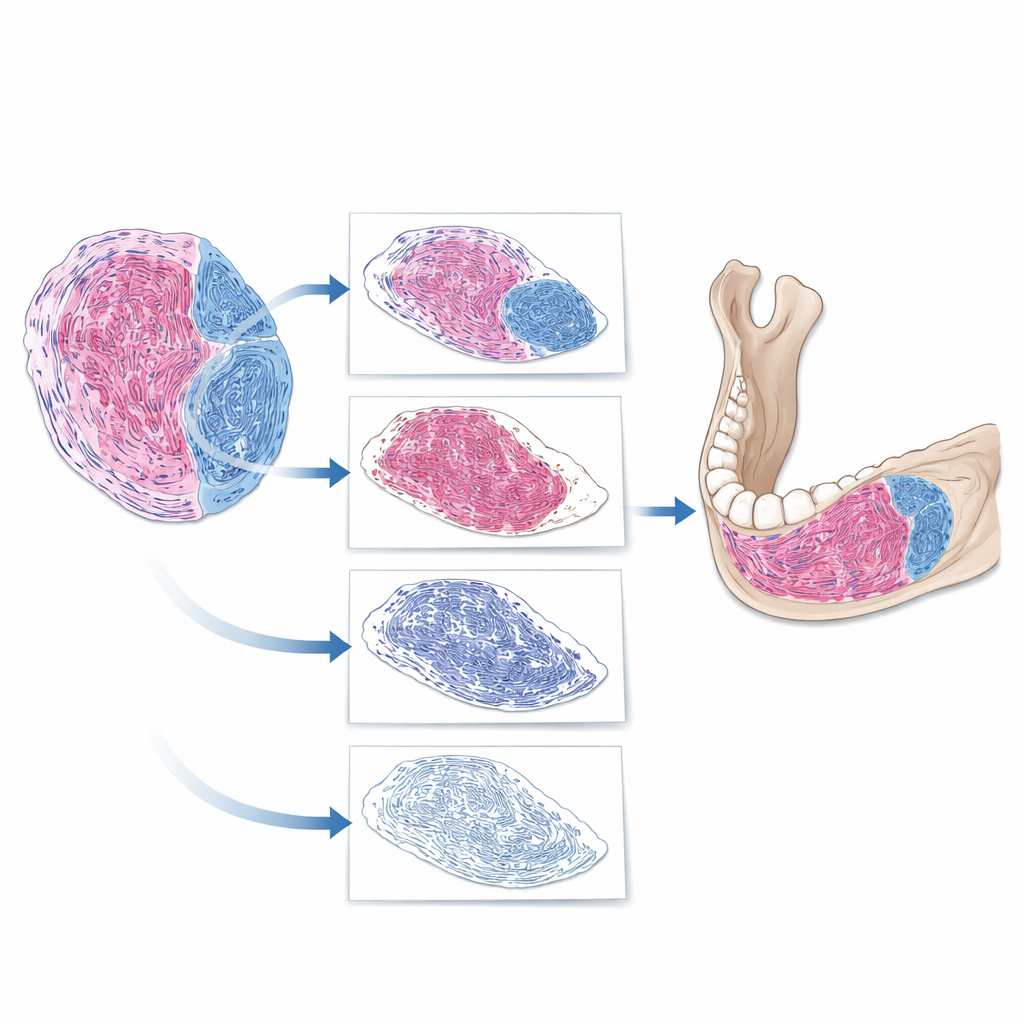
Hur AI "läser" ett tumörsnitt
Teamet byggde en steg‑för‑steg digital pipeline för att analysera helglasbilder. Först separerade programvaran verklig vävnad från tom bakgrund på glaset. Därefter isolerade den tumören från närliggande strukturer såsom ben och tänder. Slutligen, inom tumören, tog den bort cellkärnor och fokuserade på det återstående materialet, för att identifiera regioner som tagit upp det fibrösa färgämnet. Utifrån detta beräknade AI en andel fibrös vävnad: arean fibrös vävnad dividerad med total tumörarea. När forskarna jämförde AI‑genererade värden med sina egna expertskattningar var överensstämmelsen god, med bara omkring tio procentenheters spridning i de flesta enskilda fall. Det föreslog att AI kunde pålitligt spegla experternas bedömningar, samtidigt som den uttryckte dem som precisa mätningar istället för grova intryck.
Vad fibrös sammansättning berättar om tumörens utseende
Med dessa mätningar undersökte forskarna hur fibröst innehåll relaterade till kliniska och radiologiska egenskaper. De fann att mängden fibrös vävnad varierade mycket mellan institutioner, vilket speglar skillnader i hur patologer ursprungligen märkt tumörerna. När de studerade bildkarakteristika framträdde ett tydligt mönster: tumörer som framträdde som en enskild kammare på skanningar (unilokulära lesioner) tenderade att ha en högre andel fibrös vävnad än de med flera små utrymmen (multilokulära lesioner). Detta stämmer med idén att mer fibrös, tät vävnad kan bilda en mer solid, enkammrig massa, medan lösare, mer vätskerik vävnad kan dela upp sig i flera rum.
Vad detta innebär för framtida diagnostik och vård
Studien avser inte att döpa om sjukdomar eller ersätta patologer med maskiner. I stället visar den att AI‑baserad kvantitativ patologi kan erbjuda en gemensam mätstandard för sällsynta käktumörer över många sjukhus. Genom att förvandla tumörvävnadens subtila texturer till reproducerbara siffror blottlägger metoden hur mycket vardagliga diagnoser beror på subjektivt omdöme och erbjuder ett sätt att minska den variationen. För patienter kan mer konsekvent tolkning av dessa lesioner stödja tydligare behandlingsbeslut och bättre jämförelser av utfall mellan centra. När liknande metoder används för andra sällsynta tumörer kan AI‑assisterad mikroskopi tyst förändra hur patologer ser på sjukdom — göra deras bedömningar mer jämförbara och i sista hand mer användbara, oavsett var en patient behandlas.
Citering: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
Nyckelord: odontogent myxom, käktumörer, digital patologi, artificiell intelligens, andel fibröst vävnad