Clear Sky Science · sv
Genetisk analys av nyckelspelare i PI3K‑signalvägen vid kolorektalt karcinom
Varför dina gener betyder något för tarmhälsan
Kolorektal cancer är en av de vanligaste och dödligaste cancerformerna globalt, och antalet fall ökar i många länder som genomgår snabba livsstilsförändringar. Ändå drabbas inte alla med liknande kost eller vanor i samma utsträckning. Denna studie ställer en enkel men viktig fråga: kan ärftliga skillnader i centrala tillväxtreglerande gener förklara vem som utvecklar kolorektal cancer, hur aggressiv den blir och hur väl standardläkemedel fungerar—särskilt i en stor grupp patienter från Pakistan, en population som hittills varit underforskat?
En intensiv kontrolllinje inne i våra celler
Celler i tarmen tar ständigt emot signaler som talar om när de ska växa, dela sig eller självdö. En av de mest aktiva kommunikationsvägarna är PI3K–AKT–mTOR‑kaskaden—en serie molekylära strömbrytare som främjar celltillväxt, överlevnad, nybildning av blodkärl och motstånd mot celldöd. När denna väg är överaktiv kan celler börja föröka sig okontrollerat och bilda tumörer. Generna PIK3CA, AKT1 och mTOR sitter vid avgörande kontrollpunkter längs denna väg. Subtila ärftliga förändringar i dessa gener, kallade single nucleotide polymorphisms (SNPs), och starkare förändringar kända som ”hotspot”-mutationer kan rubba balansen mot cancer eller förändra hur tumörer svarar på behandling.
Skanning av DNA hos patienter och friska frivilliga
För att undersöka detta genomförde forskarna en case–control‑studie som inkluderade 495 personer med kolorektal cancer och 495 cancerfria frivilliga matchade för ålder och kön. Blodprover gav DNA som undersöktes för sju SNPs i PIK3CA, AKT1 och mTOR, tillsammans med två välkända hotspot‑mutationer kallade E542K (i PIK3CA) och E17K (i AKT1). Med riktade PCR‑metoder och DNA‑sekvensering jämförde teamet hur ofta varje genetisk variant förekom hos patienter jämfört med kontroller och kopplade sedan dessa mönster till kliniska egenskaper som ålder, familjehistoria, tarmsjukdom, tumörstadium och vilka läkemedelsregimer patienterna fått. 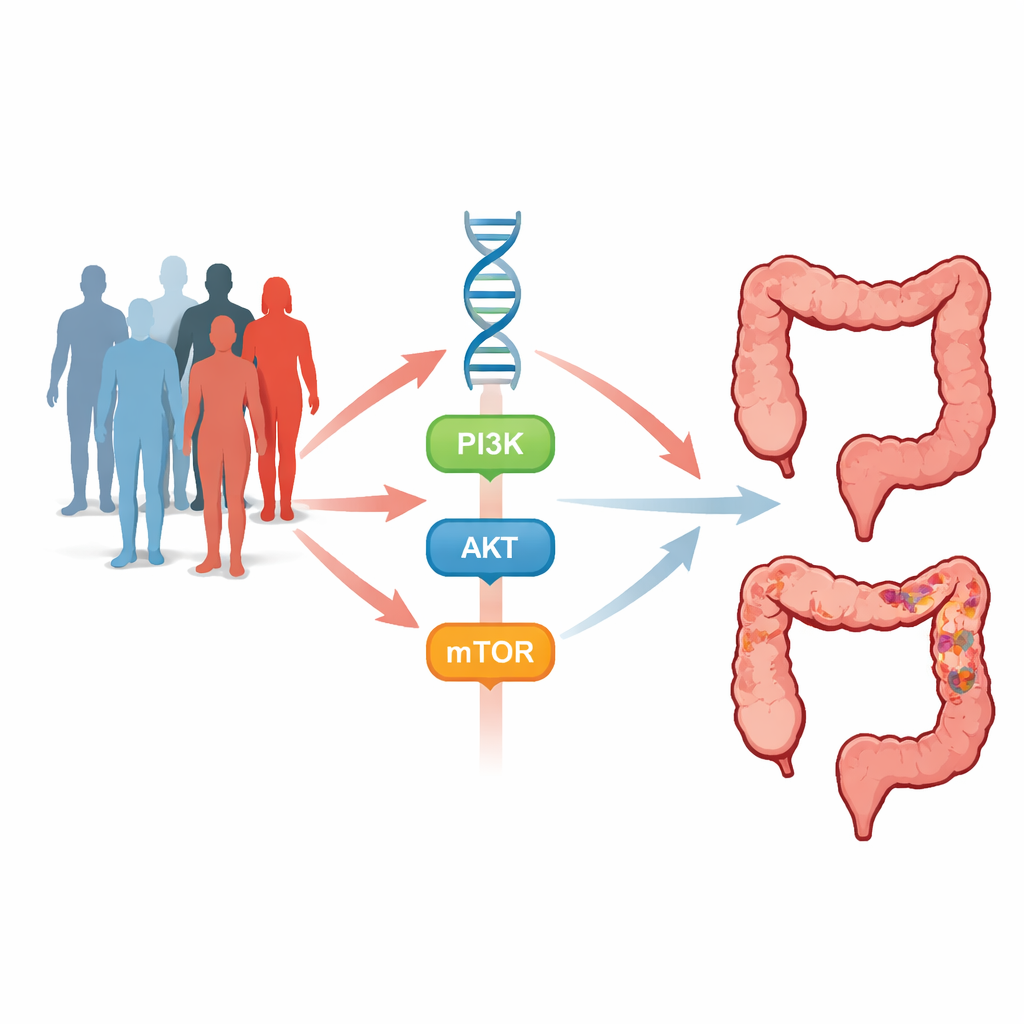
Riskabla varianter och kraftfulla mutationer
Analysen visade att de flesta av de testade varianterna var betydligt vanligare hos personer med kolorektal cancer än hos friska kontroller, vilket starkt tyder på att de bidrar till sjukdomsrisk. Flera AKT1‑ och mTOR‑varianter visade särskilt mycket högre frekvens hos patienter, medan vissa ”normala” versioner av dessa gener var vanligare hos kontroller, vilket antyder en skyddande roll. Hotspot‑mutationerna gav en ännu tydligare bild: förändringen E542K i PIK3CA förekom hos cirka 15 % av patienterna, och E17K i AKT1 hos omkring 29 %, båda mycket vanligare än hos kontroller. Datorbaserade modeller indikerade att dessa mutationer inte drastiskt förvränger proteinets övergripande form utan snarare verkar låsa vägen i ett mer ”på”-läge, vilket driver kontinuerliga tillväxtsignaler som gynnar tumörutveckling.
Från gener till behandling och överlevnad
Genetik verkar inte isolerat, så forskarna undersökte hur dessa varianter samspelar med verkliga riskfaktorer och behandlingar. Många av SNPs kopplades till rökning, inflammatorisk tarmsjukdom, familjehistoria, cancer typ och stadium, samt huruvida patienterna fått kemoterapi eller strålbehandling. När teamet följde patienterna över tid fann de att vissa genvarianter var förknippade med bättre eller sämre totalöverlevnad. Till exempel tenderade personer med normala versioner av flera AKT1‑ och mTOR‑varianter att leva längre än de med högriskvarianter. Studien jämförde också överlevnad bland patienter som fått vanliga läkemedelskombinationer. Capecitabine, ett ofta använt kemoterapipreparat i tablettform, förknippades med de bästa överlevnadsestimatet, och flera av vägvarianterna verkade påverka hur väl olika regimer fungerade, vilket antyder att ärftlig genetik kan vägleda mer personligt anpassade behandlingsval. 
Hur förändringar färdas tillsammans
Bortom enskilda varianter undersökte författarna hur grupper av förändringar tenderar att ärvas tillsammans—ett mönster känt som linkage disequilibrium. De upptäckte ett block av närliggande varianter som sträcker sig över PIK3CA och AKT1 som ärvs tillsammans oftare hos patienter än hos kontroller. Detta tyder på att kombinationer av små DNA‑skillnader längs PI3K‑vägen kan gemensamt forma en persons grundläggande risk och hur en tumör beter sig, snarare än att någon enskild förändring agerar ensam.
Vad detta betyder för patienter och precisionsmedicin
För en lekmannaläsare är slutsatsen att detta arbete stärker idén att ”en lösning passar alla” är en dålig modell för vård av kolorektal cancer. I denna pakistanska kohort följde specifika ärftliga varianter och hotspot‑mutationer i tillväxtreglerande gener tydligt med cancer‑risk, tumörkaraktär och överlevnad, och de verkade till och med påverka hur patienter klarade sig på standardkemoterapi. Även om dessa fynd behöver bekräftas i större och mer diversifierade grupper, pekar de mot en framtid där ett enkelt blodprov för PI3K–AKT–mTOR‑varianter skulle kunna hjälpa till att identifiera dem med högre risk, flagga vilka patienter som kan gynnas av särskilda läkemedel och skona andra från ineffektiva eller onödigt toxiska behandlingar.
Citering: Pervaiz, H., Masood, N., Malik, P.A. et al. Genetic analysis of key players in PI3K signaling cascade of colorectal carcinoma. Sci Rep 16, 11317 (2026). https://doi.org/10.1038/s41598-026-42006-z
Nyckelord: genetik vid kolorektal cancer, PI3K AKT mTOR‑väg, single nucleotide polymorfismer, precisionsonkologi, kemoterapisvar