Clear Sky Science · sv
Analys av extracellulära vesiklar från bronkialt epitel med konventionell, bild- och nanoskalig flödescytometri
Varför de mikroskopiska bubblorna i lungorna spelar roll
Våra lungor är beklädda med celler som ständigt kommunicerar med immunsystemet, särskilt när vi andas in damm, föroreningar eller mikrober. Mycket av denna “konversation” sker genom mikroskopiska bubblor kallade extracellulära vesiklar — paket av lipider och proteiner som frisätts av celler. Dessa vesiklar kan förvärra eller dämpa lungsjukdom, och de kan i framtiden fungera som tidiga varningssignaler för tillstånd som astma, kronisk obstruktiv lungsjukdom (KOL) och fibros. Denna studie undersöker hur man bäst mäter dessa svårfångade partiklar med olika typer av avancerade lasertekniker, med fokus på att göra mätningarna praktiska för forskning och framtida kliniska tester.
Osynliga meddelanden från luftvägsceller
Extracellulära vesiklar (EV) är små, membranomslutna paket som nästan alla celler släpper ut i vätskor som blod, urin och det tunna vätskeskiktet i våra luftvägar. EV från humant bronkialt epitel — cellerna som bekläder andningsvägarna — har redan kopplats till flera lungprocesser: de kan påverka hur allergier utvecklas, hjälpa till att bekämpa lunginfektioner, forma luftvägarnas struktur vid KOL och till och med begränsa ärrbildning i lungvävnad. Eftersom de bär med sig delar av proteiner, lipider och genetiskt material från sina ursprungsceller kan EV fungera som fingeravtryck för lungors hälsa eller sjukdom och kanske så småningom användas som behandlingar i sig. Utmaningen är att de är extremt små, mycket varierande och finns i låga mängder, vilket gör dem svåra att upptäcka och räkna noggrant.
Bortom långsamma och fragmenterade tester
Traditionellt har forskare förlitat sig på flera separata metoder för att studera EV. Ultracentrifugering eller storleksuteslutningskromatografi används för att isolera dem; nanopartikelspårningsanalys mäter hur de rör sig för att uppskatta storlek och antal; och elektronmikroskop ger detaljerade bilder. Dessa metoder är kraftfulla men är långsamma, arbetsintensiva och inte idealiska för rutinmässig eller klinisk användning. Avgörande är att de har svårt att avgöra vilka specifika proteiner varje vesikel bär. Flödescytometri — en teknik som ofta används för att analysera blod- och immunceller — erbjuder ett mer effektivt alternativ. Den för skickar partiklar en och en förbi lasrar och mäter ljusspridning (relaterat till storlek) och fluorescens (från färgämnen eller antikroppar). Nya instrumentdesigner lovar att skjuta ned gränsen för flödescytometri till de minsta vesiklarnas storlek, vilket öppnar möjligheten att ett enda instrument kan storleksbestämma, räkna och karakterisera EV i ett och samma körning.
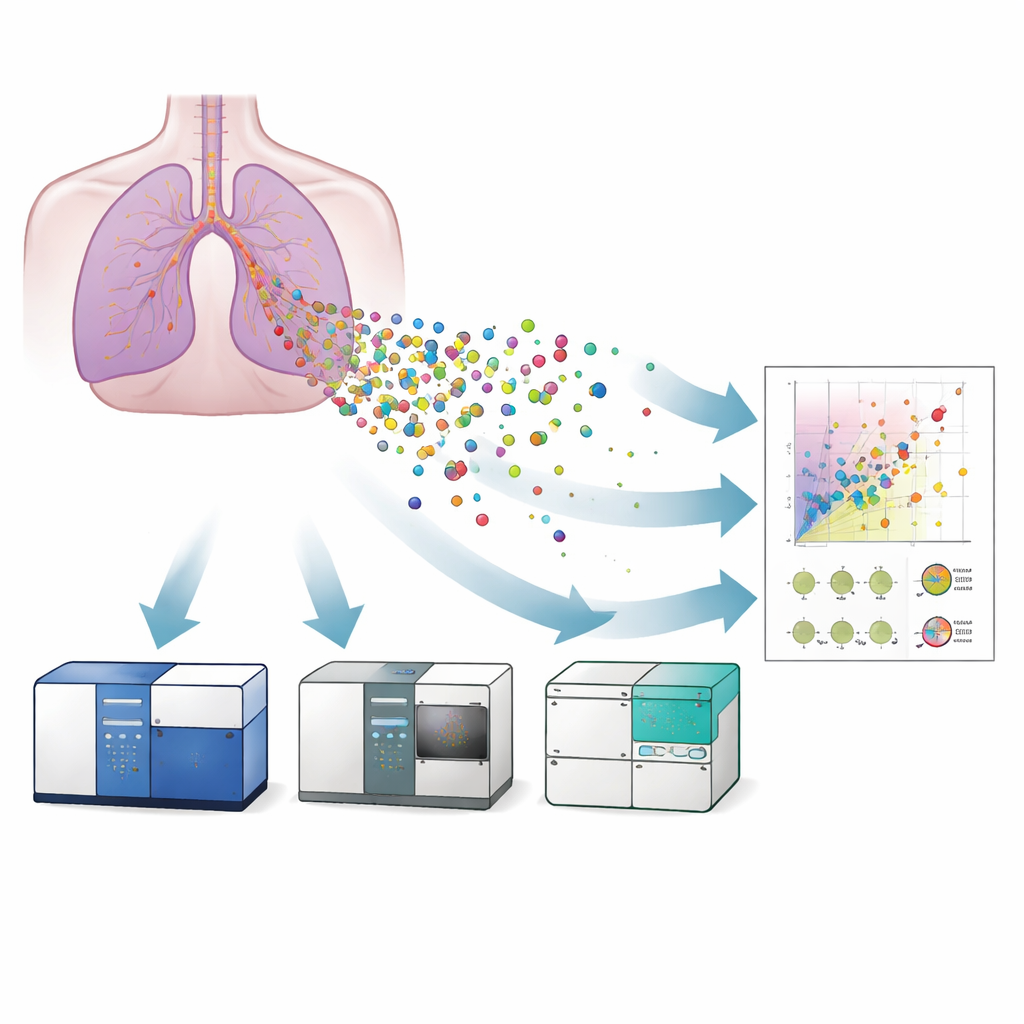
Tre instrument, ett mål
Forskarna jämförde tre varianter av flödescytometri för att studera EV som släpps ut från en laboratorieodlad modell av mänskligt bronkialepitel: en konventionell flödescytometer, en bildflödescytometer och en nanoskalig flödescytometer. Först bekräftade de vesiklarnas närvaro och typiska utseende med elektronmikroskopi och superupplösningsmikroskopi, som också visade att vesiklarna bar ytliga proteiner kända som tetraspaniner (CD9, CD63, CD81) — standardmarkörer för att identifiera EV. De använde sedan noggrant kalibrerade referenspärlor och liposomstandarder för att översätta varje instruments ljussignaler till ungefärliga vesikelstorlekar. Den nanoskaliga flödescytometern kunde upptäcka vesiklar så små som omkring 40 nanometer, bildinstrumentet ner till cirka 55 nanometer, medan den konventionella maskinen hade svårt under ungefär 120 nanometer. Det innebar att endast de känsligare systemen kunde fånga de minsta, och potentiellt mest medicinskt relevanta, vesiklarna fullt ut.
Färgmärkning och uppräkning av vesiklar
För att försäkra sig om att de mätte intakta, biologiskt aktiva vesiklar snarare än skräp använde teamet ett färgämne kallat calcein-AM. Detta färgämne lyser endast upp när det passerar ett intakt membran och bearbetas av enzymer inuti vesikeln. De finjusterade färgämneskoncentrationen så att vesiklarna markerades starkt samtidigt som bakgrundssignalen minimerades, och valde en koncentration som gav tydliga, linjära svar över utspädningar av prover. Calcein kombinerades sedan med fluorescerande antikroppar som binder tetraspaniner på vesiklarnas yta, vilket gjorde det möjligt för instrumenten att skilja vesiklar som bar olika kombinationer av dessa markörer. Gruppen mätte också hur känsligt varje instrument var för dessa fluorescensmärken — hur många antikroppsmolekyler som behövde finnas på en vesikel innan den kunde upptäckas pålitligt. Bildflödescytometri erbjöd i allmänhet lägre detektionsgränser än den konventionella cytometern, vilket gör den bättre lämpad för partiklar med endast ett litet antal markörproteiner.
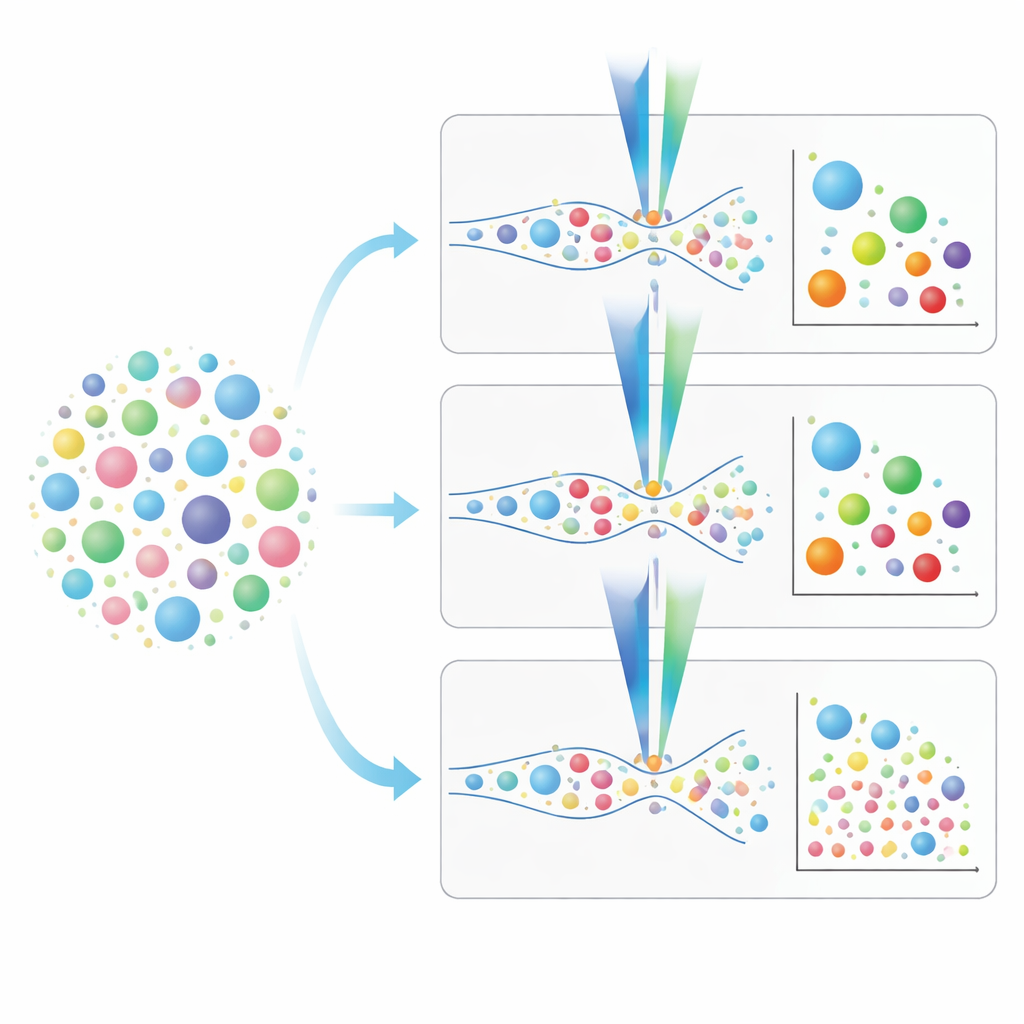
Välja rätt verktyg för studier av lungvesiklar
Ur denna jämförelse framträder en praktisk bild. Konventionella flödescytometrar är snabbare och kan analysera prover utan föregående isolering, men de missar många av de minsta vesiklarna som kan bära viktiga sjukdomssignaler. Bild- och nanoskaliga flödescytometrar, även om de är långsammare och i nano-instrumentets fall mer beroende av föregående provrensning, kan se ner till mycket mindre storlekar och möjliggör rikare “fingeravtryck” av vesiklars ytmärken. Författarna beskriver steg-för-steg färgnings- och kalibreringsstrategier, betonar vikten av att känna varje fluorescerande märkes detektionsgräns, och visar hur man undviker vilseledande signaler från färger som också märker fragment eller icke-vesikelpartiklar. Med enkla ord ger de en färdplan för forskare att avgöra vilket instrument och protokoll som passar deras frågor om lung-EV, vilket hjälper fältet närmare att använda dessa mikroskopiska budbärare som praktiska verktyg för att förstå, diagnostisera och så småningom behandla respiratoriska sjukdomar.
Citering: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
Nyckelord: extracellulära vesiklar, lungepitel, flödescytometri, lungsjukdom, biomarköranalys