Clear Sky Science · sv
Kvantitativ ex vivo‑bedömning av målstemperatur och ablationstid för protokollsoptimering av mikrovågsablation med MR‑termometri
Att följa tumörbehandlingar i realtid
När läkare bränner bort levertumörer med värme vill de se exakt vilka delar av organet som förstörs medan ingreppet pågår. Magnetresonanstomografi (MRI) erbjuder ett sätt att ”se temperatur” inuti kroppen när värme sprider sig. Denna studie undersöker hur varmt — och hur länge — läkare kan värma levertäcken under mikrovågsablation och samtidigt få tydliga, tillförlitliga temperaturkartor från MRI — ett viktigt steg mot mer precisa och mindre invasiva cancerbehandlingar.
Varför värmebaserade leverbehandlingar behöver bättre uppsikt
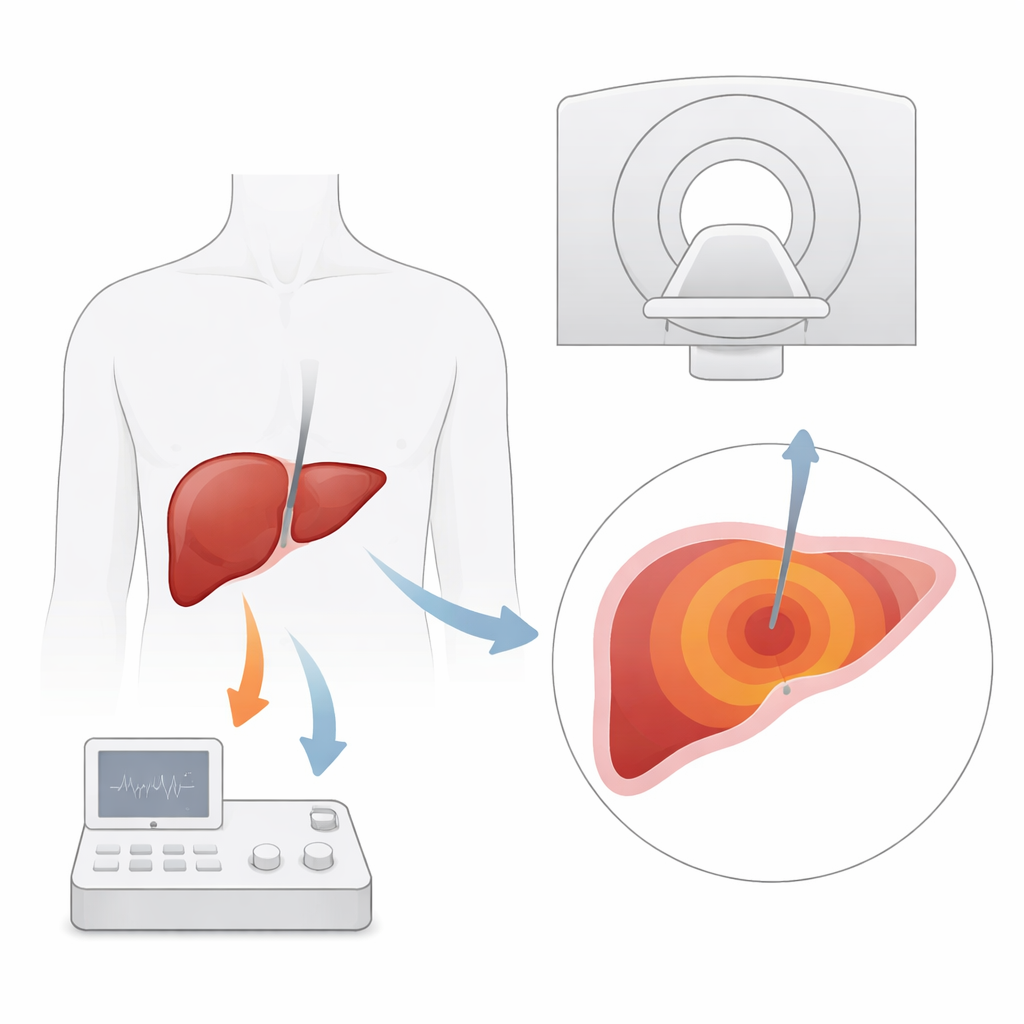
Mikrovågsablation använder en tunn nål för att leverera energi som kokar och dödar tumörvävnad i levern. Det är särskilt viktigt för patienter med levercancer eller metastaser som inte kan genomgå operation. Traditionella bildverktyg som ultraljud och CT‑skanningar styr var nålen ska placeras, men de har svårt att visa små tumörer tydligt eller att följa hur långt värmen har spridit sig under behandlingen. MRI utmärker sig eftersom det inte bara kan visa mjukvävnad i hög detalj, utan också mäta temperaturskillnader med hjälp av en egenskap hos vattenmolekyler. I teorin tillåter detta läkare att följa en värmekarta av levern i realtid och säkerställa att hela tumören, plus en säker marginal, förstörs.
När för mycket värme gör sikten dålig
I praktiken kan MRI‑temperaturkartor bli opålitliga när vävnad blir mycket varm. Vid höga temperaturer kokar vattnet i vävnaden och bildar små gasfickor som förvränger det magnetiska fältet. Dessa förvrängningar visar sig som felaktiga temperaturavläsningar och konstiga former på kartan, vilket gör det svårt att veta var den verkliga ablationszonen slutar. Forskarna misstänkte att något lägre måltemperaturer skulle ge renare, mer tillförlitliga MRI‑kartor, även om det innebar mindre behandlade områden. Målet var att hitta kombinationer av målstemperatur och uppvärmningstid som bäst balanserar bildklarhet med tillräcklig vävnadsdestruktion.
Test av värmeinställningar i donerade djurlevern
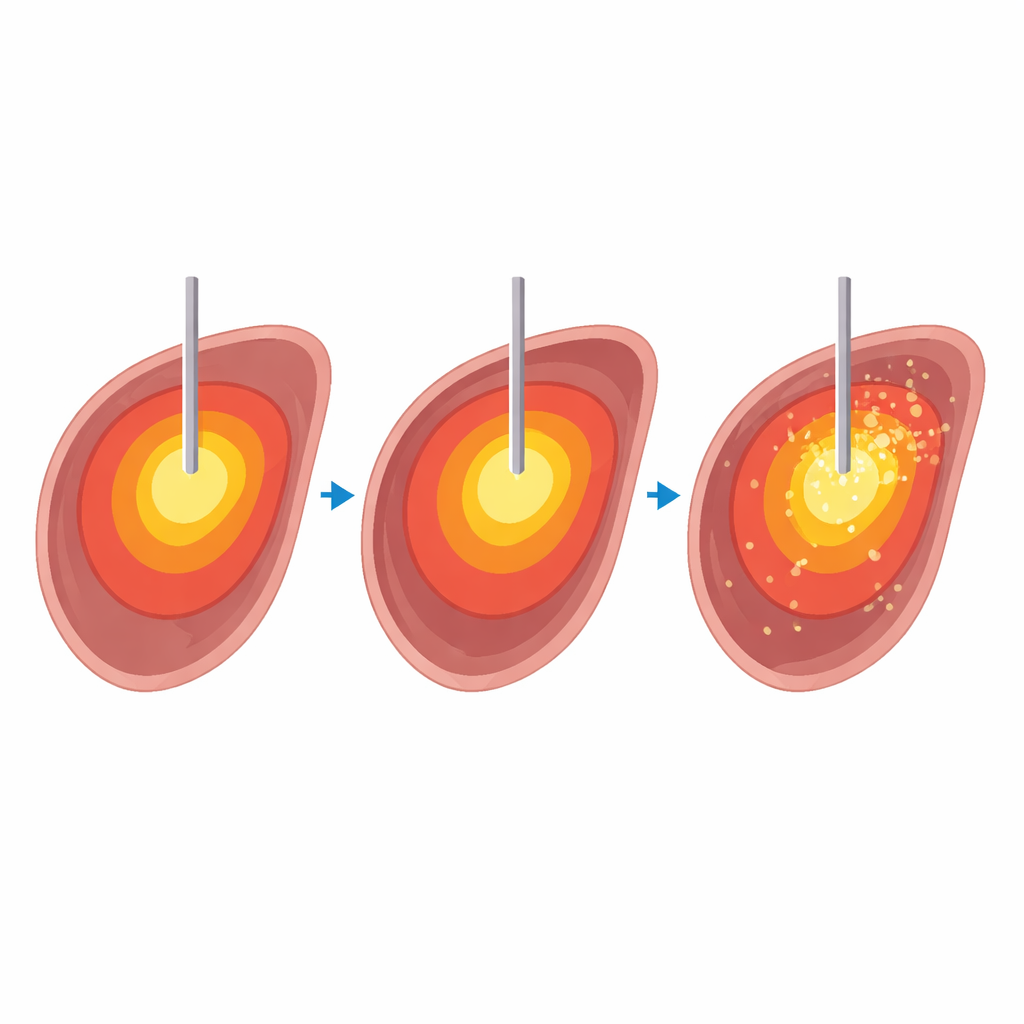
För att undersöka detta säkert och precist utförde teamet 32 mikrovågsablationer i tio nötkreaturslever som tagits bort kort efter slakt. Inuti en 1,5‑tesla MRI‑scanner värmde de levervävnad till fyra målstemperaturer — 60, 80, 100 och 120 grader Celsius — under fyra olika tidsperioder mellan 5 och 15 minuter. Under varje ablation producerade en snabb MRI‑sekvens tredimensionella temperatur‑ och ”termiska dos”‑kartor varannan sekund. Efter uppvärmningen skars levern längs nålspåret och de synliga områdena med död vävnad mättes och jämfördes med de områden som förutsägs av MRI‑kartorna. Två radiologer bedömde MRI‑kartornas kvalitet på en femgradig skala, med hänsyn till hur runda och regelbundna de uppvärmda zonerna såg ut och hur mycket artefakter från gas och nålen störde.
Kallare bränningar, klarare kartor
Experimenten visade en tydlig avvägning. Högre temperaturer gav större områden med död vävnad, vilket var väntat, men MRI‑temperaturkartorna försämrades markant över 100 grader. Vid dessa högre inställningar blev ablationsformerna mer oregelbundna och gasrelaterade förvrängningar orsakade till synes sjunkande eller till och med negativa temperaturvärden nära nålen. I kontrast var MRI‑kartorna vid 60 och 80 grader jämnare, mer cirkulära och stämde mycket bättre överens med de verkliga lesionstorlekarna som sågs i vävnadsskivorna. Statistiska analyser bekräftade stark överensstämmelse mellan MRI‑beräknade områden och faktisk nekros vid lägre temperaturer, medan korrelationerna försvagades eller försvann vid högre temperaturer. Förlängd uppvärmningstid kom delvis till rätta med lägre temperaturer när det gäller total skada, men kunde inte helt matcha de största lesionerna som sågs vid 120 grader.
En tvåstegsstrategi för säkrare, smartare ablation
Baserat på dessa fynd föreslår författarna ett praktiskt kompromissförslag för framtida MRI‑styrda behandlingar. En första uppvärmningsfas vid cirka 80 grader Celsius under 15 minuter gav en bra balans: bildkvaliteten var hög, ablationszonen var rimligt stor och vävnadsstudier visade effektiv celldöd. För fall som kräver ännu större behandlingszoner föreslår de en tvåstegsmetod: börja med en lägre temperaturfas för att få en ren termisk karta och verifiera täckningen, och öka sedan temperaturen i en andra fas för att utvidga det dödade området, med förståelsen att temperaturkartan blir mindre tillförlitlig under denna slutliga upptrappning.
Vad detta betyder för framtida patientvård
För en icke‑specialist är huvudbudskapet att ”sänkt värme lite grann” faktiskt kan göra värmebaserade cancerbehandlingar säkrare och mer precisa — åtminstone i kontrollerade laboratorieförhållanden. Lägre måltemperaturer gav mycket klarare MRI‑temperaturkartor, vilket gjorde det lättare att se var vävnad faktiskt hade förstörts. Nackdelen är att kallare bränningar ger mindre lesioner, så läkare kan behöva längre eller flerstegsbehandlingar för att täcka stora tumörer. Eftersom forskningen utfördes i avlidna djurlever utan blodflöde eller andningsrörelser krävs ytterligare studier på patienter. Ändå pekar studien mot behandlingsprotokoll som använder MRI inte bara för att rikta nålen, utan för att övervaka och finslipa bränningen i realtid, vilket potentiellt kan förbättra utfallen för personer med levertumörer.
Citering: Nardone, L., Tan, A.S.M., Bour, P. et al. Quantitative ex vivo assessment of target temperature and ablation duration for protocol optimization of microwave ablation procedures with mr thermometry. Sci Rep 16, 8153 (2026). https://doi.org/10.1038/s41598-026-41656-3
Nyckelord: mikrovågsablation, MR‑termometri, levercancer, termisk ablation, bildstyrd terapi