Clear Sky Science · sv
Utvärdering av metagenomik med långläsning för diagnostik av blodförgiftning: en pilotstudie från ett thailändskt tertiärt sjukhus
Varför snabbare tester för blodinfektioner spelar roll
När bakterier invaderar blodomloppet räknas varje timme. Läkare måste snabbt välja rätt antibiotika, men dagens laboratorietester kan ta flera dagar för att identifiera boven och avgöra vilka läkemedel som sannolikt kommer att misslyckas. Denna studie från ett stort thailändskt sjukhus undersöker ett nytt sätt att snabba upp processen genom att läsa det genetiska materialet från alla mikrober i ett blodprov på en gång, med hjälp av en bärbar DNA‑sekvenserare. Målet är att gå från att vänta flera dagar på svar till att få en detaljerad bild av infektionen inom en enda arbetsperiod.
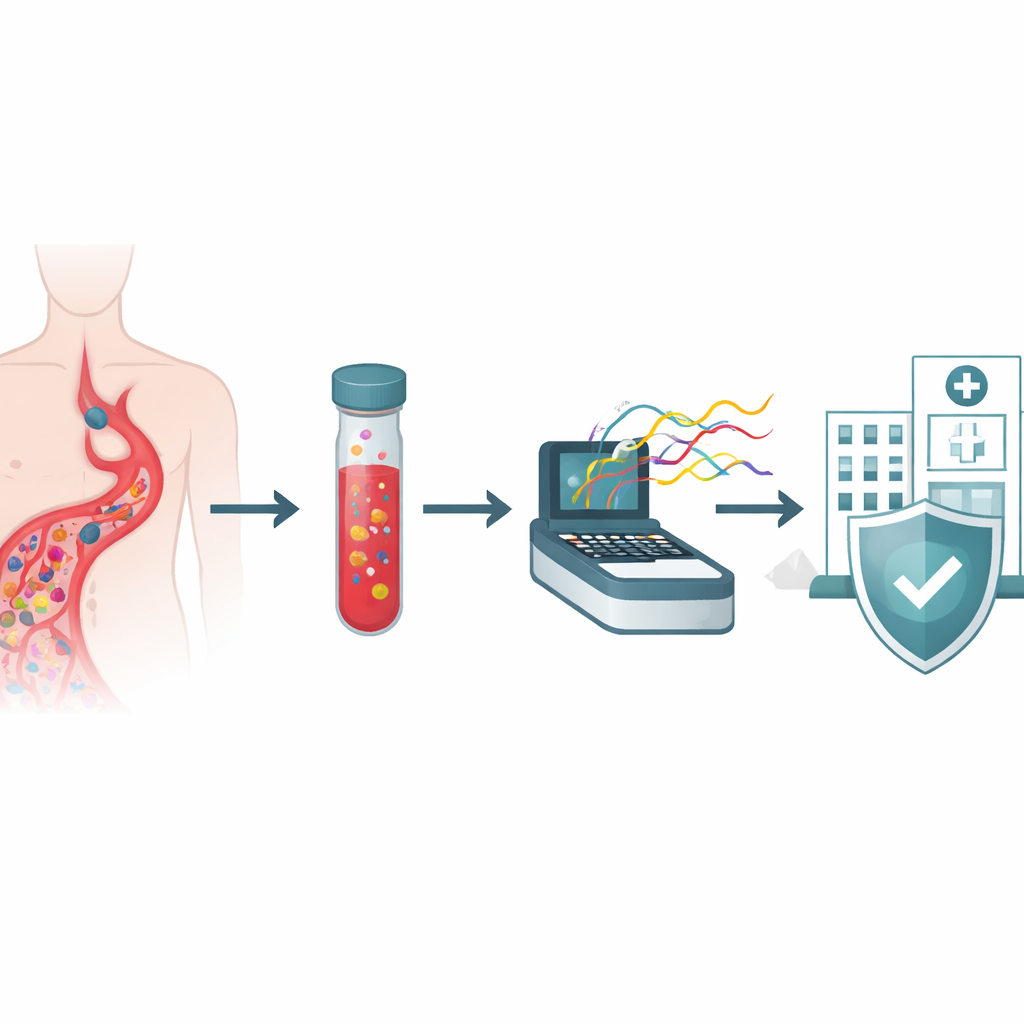
Ett nytt sätt att läsa av mikrober i blodet
Forskarnas fokus låg på patienter som redan visade tecken på bakterietillväxt i standardiserade blododlingsflaskor, vilka rutinmässigt används på sjukhus världen över. Istället för att odla varje bakterie på separata plattor och köra en serie kemiska tester, tog de vätska direkt från 40 positiva odlingsflaskor och extraherade allt mikrobiellt DNA. Detta DNA kördes sedan på en Oxford Nanopore‑sekvenserare, en apparat som drar långa strängar av genetiskt material genom små porer och läser deras sekvens i realtid. Eftersom metoden inte är beroende av att odla varje organism separat kan den i princip upptäcka många arter, deras resistensegenskaper och deras sjukdomsframkallande verktyg i ett enda strömlinjeformat arbetsflöde.
Vad som upptäcktes i thailändska blodinfektioner
Konventionell analys av samma 40 prover gav 45 bakteriella isolat, vilket återspeglar att några patienter var infekterade med mer än en art. Sjukhusens vanliga arbetsverktyg, VITEK, visade att två välkända tarmbakterier, Escherichia coli och Klebsiella pneumoniae, orsakade nästan 40 % av dessa infektioner, och att många av dessa stammar var resistenta mot flera läkemedel. Nanopore‑metoden överensstämde i stort med denna bild, genom att identifiera 43 distinkta bakteriella genom och bekräfta att medlemmar av Enterobacterales‑gruppen dominerade. Den upptäckte också några ovanliga eller felklassificerade arter, såsom en miljöbakterie kallad Ralstonia mannitolilytica och magsårsbakterien Campylobacter jejuni, som rutinmetoderna hade missat eller bara identifierat på bred nivå. I vissa blandinfektioner hade sekvenseringen dock svårt att helt separera nära besläktade mikrober när en fanns i mycket lägre mängd än den andra.
Insikter om resistens och förslagna strategier
Eftersom den nya metoden läser långa DNA‑stycken kan den mer än bara namnge bakterierna: den kan avslöja den genetiska maskineriet som hjälper dem att motstå antibiotika och orsaka sjukdom. Teamet genomsökte genomen efter kända resistensgener och efter "virulens"gener som hjälper mikrober att fästa vid vävnader, bilda skyddande biofilmer, ta järn eller producera toxiner. E. coli och K. pneumoniae bar många sådana gener, inklusive de som inaktiverar viktiga antibiotikafamiljer som beta‑laktamer och aminoglykosider. Sekvenseringen framhävde också kraftfulla resistenspaket i sjukhusförstärkta arter såsom Acinetobacter baumannii och Pseudomonas aeruginosa, vars genom var rika på pumpar och andra försvarsmekanismer. Samtidigt hade några sällsyntare blodbakterier relativt blygsamma arsenaler, vilket antyder en lägre men fortfarande betydande risk.
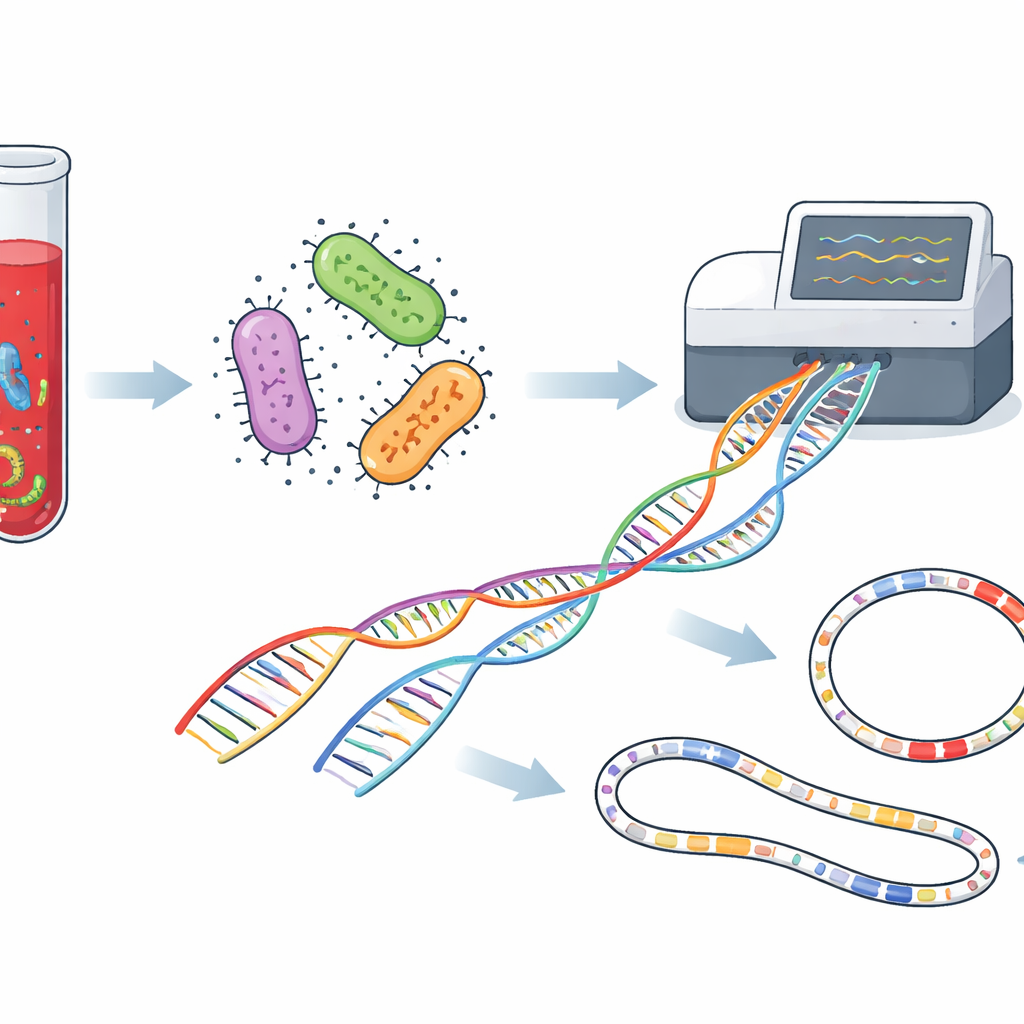
Följa resistens på mobilt DNA
En annan styrka hos långläsningssekvensering är förmågan att pussla ihop hela bakteriella kromosomer tillsammans med cirkulära DNA‑molekyler kallade plasmider, som kan hoppa mellan bakterier och sprida resistensgener. I denna studie katalogiserade forskarna flera dussin plasmidtyper. Några var starkt knutna till särskilda arter, medan andra delades mellan flera bakterietyper, vilket antyder pågående genutbyte i sjukhusmiljön. Många bar välkända drivkrafter för behandlingsmisslyckande, såsom utvidgade spektrumbeta‑laktamaser och karbapenemaser — enzymer som försvagar några av de viktigaste antibiotika. Kartläggning av dessa mobila element hjälper smittskyddsteam att förstå hur farliga egenskaper rör sig genom ett sjukhus över tid.
Skalning av svarstider för läkare och sjukhus
Tidsaspekten är där den nya metoden visar sin tydligaste fördel. Standardarbetsflöden tar ofta fem till sju dagar från det att en blododling blir positiv tills full identifiering och läkemedelskänslighetsresultat är klara. I kontrast levererade nanopore‑upplägget i denna pilotstudie tidiga artidentifieringar inom två till fyra timmar efter att körningen startat och flaggade viktiga resistensgener inom sex till åtta timmar. Medan längre sekvenseringskörningar förbättrade genomens fullständighet förändrade de inte de viktigaste kliniska slutsatserna. Även om detta var en liten, tidig studie som ännu inte kopplade resultaten till patientutfall eller mätte kostnader, tyder den på att integrering av metagenomisk sekvensering med långläsning i sjukhuslaboratorier skulle kunna ge snabbare, rikare information för att vägleda behandling, stödja antibiotikastyrning och stärka regional övervakning av läkemedelsresistenta infektioner.
Vad detta betyder för patientvården
För en lekmannaläsare är slutsatsen att läkare snart kan ha ett genetiskt "ögonblicksbild" av en blodinfektion samma dag som en odling blir positiv, i stället för att vänta nästan en vecka. Denna ögonblicksbild namnger inte bara smittämnet utan framhäver också många av dess svaga punkter och dess potential att sprida resistens till andra. Medan mer arbete krävs med större patientgrupper, striktare kontaminationskontroller och kostnadsanalyser visar denna thailändska pilotstudie att fickvänliga DNA‑sekvenserare kan föra oss närmare snabb, genomik‑informerad vård för livshotande blodinfektioner.
Citering: Yaikhan, T., Wongsurawat, T., Jenjaroenpan, P. et al. Evaluating long-read metagenomics for bloodstream infection diagnostics: a pilot study from a Thai Tertiary Hospital. Sci Rep 16, 9330 (2026). https://doi.org/10.1038/s41598-026-41247-2
Nyckelord: blodström‑infektion, antimikrobiell resistens, metagenomisk sekvensering, nanopore‑teknik, klinisk mikrobiologi