Clear Sky Science · sv
In-situ-tillväxt av heterogent Au på MoS2-nanoskikt för SERS-detektion av bröstcancerhärledda miR-210-3p och miR-9-3p
Göra små cancersignaler till tydliga varningar
Läkare har länge vetat att tumörceller avger små fragment av genetiskt material till blodomloppet, men att pålitligt detektera dessa svaga sjukdomssignaler har varit svårt. Denna studie presenterar en ny nanosensor som använder en speciell kombination av guld och ett tvådimensionellt material kallat molybden-disulfid (MoS2) för att förstärka dessa svaga signaler. Målet är att göra det enklare att upptäcka bröstcancerassocierade mikroRNA — korta RNA-bitar kopplade till hur tumörer växer och sprids — med en skonsam ljusteknik som en dag kan stödja tidigare och mer precisa diagnoser.
Varför dessa små molekyler spelar roll
MikroRNA är extremt korta strängar av genetisk kod som hjälper till att kontrollera cellernas beteende. I cancer blir vissa mikroRNA ovanligt rikliga eller sällsynta, vilket gör dem till kraftfulla biomarkörer för diagnos och prognos. Utmaningen är att de finns i mycket låga nivåer, ofta blandade i komplexa biologiska vätskor som blod eller cellextrakt. Konventionella verktyg som PCR och sekvensering kan detektera dem, men kräver speciallaboratorier, utbildad personal och tidskrävande arbetsflöden. Forskarna ville utveckla en mer direkt sensorplattform som i princip kunde vara enklare att använda samtidigt som den uppnår mycket hög känslighet och förmåga att särskilja flera mikroRNA-mål samtidigt.
Bygga ett ljusförstärkande nanoskikt
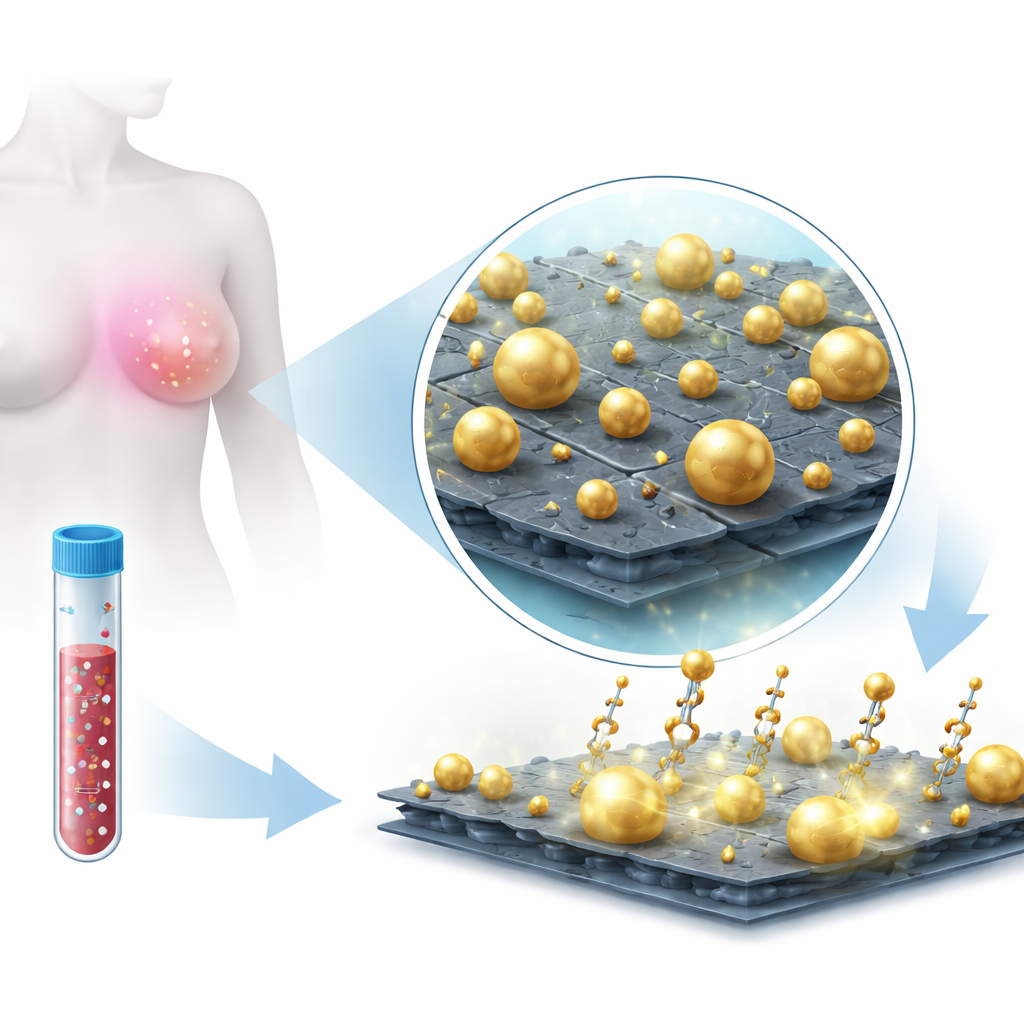
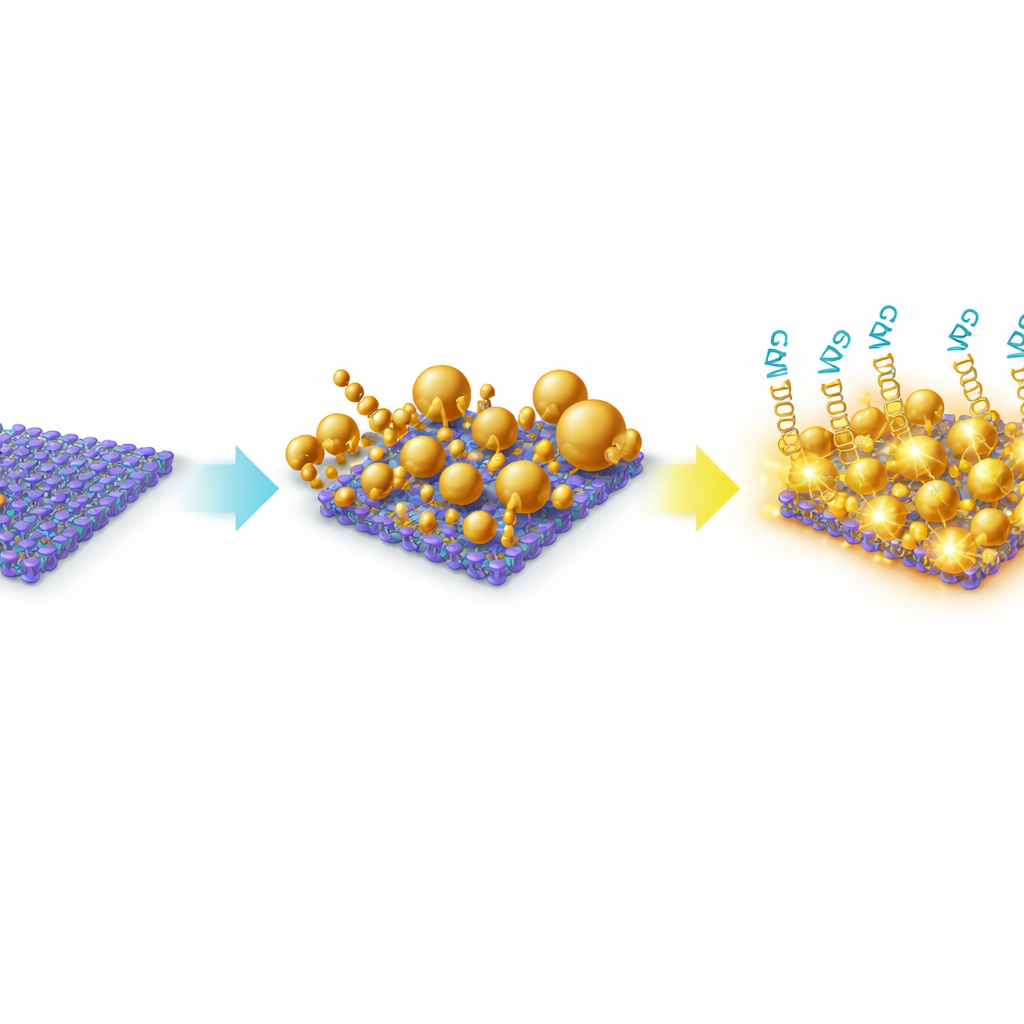
För att nå detta konstruerade teamet ett hybridmaterial gjort av tunna MoS2-nanoskikt dekorerade med guldkvantpartiklar. MoS2 är ett arkformat material bara några atomlager tjockt, vilket ger en stor yta för molekyler att fästa vid och en stark interaktion med metaller. Istället för att tillsätta förformade guldkorn odlade de guldet direkt på MoS2-ytan i lösning. Denna in-situ-tillväxt gav ett avsiktligt heterogent landskap av guldpartiklar — mestadels sfärer, men också trianglar och oregelbundna former — spridda över och längs kanterna av MoS2-bladen. Mikroskopi och spektroskopi bekräftade att guldet och MoS2 bildade ett stabilt kompositmaterial, med guldet tätt förankrat vid defektrika platser på arken. Denna oregelbundna, "råa" arkitektur är avgörande eftersom den naturligt skapar många små klyftor och skarpa egenskaper där ljus kan koncentreras starkt.
Utnyttja ljus för att läsa molekylära fingeravtryck
Plattformen använder ytförstärkt Raman-spridning (SERS), en teknik där laserljus sprids från molekyler och ger ett spektralt "fingeravtryck." I sig är ett mikroRNA för litet och svagt för att lätt höras på detta sätt. Forskarna använde i stället korta DNA-liknande prober kallade låsta nukleinsyror (LNA) som fäster vid specifika mikroRNA-sekvenser kopplade till bröstcancer, särskilt miR-210-3p och miR-9-3p. Dessa prober bar ljusstarka färgämnesmolekyler (Cy3 och Cy5.5) som ger starka Raman-fingeravtryck när de hålls nära den gulddekorerade MoS2-ytan. När ett mål-mikroRNA binder till sin matchande LNA-prob placeras färgämnet inne i guldets "hotspots", där det lokala ljusfältet förstärks mycket av den kombinerade effekten från metallspridarna och MoS2-arket. Genom att belysa med en lågenergisk nära-infraröd laser kunde teamet spela in klara Raman-spektra med distinkta toppar som speglade hur mycket mikroRNA som fanns närvarande.
Från syntetiska mål till verkliga cancerceller
Efter att ha bekräftat strukturen och stabiliteten hos deras nanokomposit testade forskarna den med syntetiska mikroRNA-sekvenser för att kalibrera och verifiera prestanda. De fann att olika spektrala toppar från varje färgämne svarade känsligt och linjärt över stora koncentrationsområden, vilket gjorde det möjligt att beräkna detektionsgränser ned till några biljoner delar av en mol (pikomolära nivåer). Viktigt var att de inte förlitade sig på en enstaka topp utan använde en multipel-topp-analys för att öka tillförlitligheten, särskilt i komplexa prover. Plattformen utmanades sedan med mikroRNA extraherade från en aggressiv bröstcancercellinje. Oberoende PCR-mätningar visade att ett mikroRNA, miR-210-3p, var mycket mer rikligt än miR-9-3p i dessa celler. Med samma SERS-upplägg kunde MoS2–guld-sensorn detektera cellhärlett miR-210-3p och miR-9-3p ner till cirka 0,1 nanomolar respektive 0,018 nanomolar, samtidigt som den sköra RNA:n bevarades med skonsam belysning.
Vad detta kan innebära för framtida cancertester
Även om detta arbete fortfarande befinner sig i laboratoriestadiet beskriver det en tydlig väg för att förvandla en omsorgsfullt konstruerad nanosurface till ett praktiskt diagnostiskt verktyg. Genom att medvetet odla guld i olika former och storlekar på MoS2 skapade forskarna ett tätt nätverk av ljusförstärkande hotspots som kan läsa av närvaron av specifika mikroRNA via deras färgämnes-taggar. Den blygsamma men välkontrollerade signalförstärkningen, kombinerad med multipel-topp-analys, möjliggör kvantitativ detektion över ett brett koncentrationsintervall i både rena och biologiskt komplexa prover. På lång sikt kan detta tillvägagångssätt stödja kompakta, multiplexade tester som övervakar flera cancerkopplade mikroRNA samtidigt, ge kliniker en rikare bild av tumörstatus från små prover och potentiellt vägleda mer personligt anpassade behandlingsbeslut.
Citering: Zablon, F.M., Pathiraja, G., Dellinger, K. et al. In-situ growth of heterogeneous Au on MoS2 nanosheets for SERS detection of breast cancer-derived miR-210-3p and miR-9-3p. Sci Rep 16, 8902 (2026). https://doi.org/10.1038/s41598-026-41084-3
Nyckelord: biomarkörer för bröstcancer, mikroRNA-detektion, SERS-nanosensorer, kompositer med guldkvantpartiklar, MoS2-baserad biosensorik